
1 de septiembre de 2011
Científicos de Salk descubren un mecanismo altamente conservado que rige el desarrollo cerebral
Científicos de Salk descubren un mecanismo altamente conservado que rige el desarrollo cerebral
LA JOLLA, CA—Si crees que la retórica política actual está exagerada, imagina lo que sucede dentro de un embrión de vertebrado. Allí, dos ejércitos con agendas opuestas se enfrentan en una batalla con consecuencias mucho más graves que si la economía se recuperará: luchan por si tú (o las ranas o los pollos) tendrán cerebro anterior.
En un estudio publicado en la edición en línea del 19 de agosto de Genes y Desarrollo, El Instituto Salk, investigadores dirigidos por Greg Lemke, Ph.D., profesor en el Laboratorio de Neurobiología Molecular, revela que un soldado de infantería de un ejército —los ventralizadores— despliega un arma que desarma al otro —los dorsalizadores—, dejando al embrión en libertad para desarrollar un cerebro adecuado. Esos hallazgos definen cómo se desarrolla el sistema nervioso embrionario y podrían arrojar luz sobre los mecanismos que subyacen al cáncer de colon.
El laboratorio Lemke tiene un interés a largo plazo en cómo los diferentes tipos de células que emergen a lo largo del eje dorsal/ventral, o “de arriba abajo”, del sistema nervioso son determinados por la competencia entre dos factores secretados, u “morfógenos”: el dorsalizador Wnt, que desciende del “polo norte” del cerebro o del ojo, y su oponente ventralizador Sonic Hedgehog, que asciende desde el “sur”.
“Los gradientes de morfógenos opuestos regulan genes que deben expresarse en la parte superior o inferior del cerebro para que ocurra un desarrollo normal —dice Lemke—. Esas mismas señales deben controlarse cuidadosamente más adelante en los tejidos maduros. Un ejemplo importante es el cáncer, donde la señalización Wnt hiperactiva a menudo se relaciona con la formación de tumores”.“
El laboratorio de Lemke demostró previamente que un par de proteínas Vax, que se unen al ADN y regulan la expresión génica, se expresan en un gradiente opuesto a las Wnt: alto en el polo sur, o ventral, del cerebro u ojo, y menor a medida que se avanza hacia el norte. Esto los llevó a proponer que, en respuesta a la señalización de Sonic Hedgehog, las proteínas Vax ventralizan los tejidos al bloquear las señales Wnt.
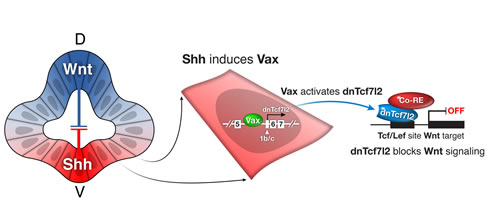
Wnt y Sonic hedgehog (Shh) son proteínas de señalización que definen los extremos dorsal (D) y ventral (V), los polos Norte y Sur, del cerebro embrionario. Wnt y Shh compiten recíprocamente en el embrión y reprimen fuertemente las actividades del otro. Vacik y otros. describe un nuevo mecanismo simple pero poderoso para esta represión recíproca: los factores de transcripción Vax, cuya expresión es activada por Shh, a su vez activan la expresión de dnTcf7l2, que funciona como un inhibidor potente de la señalización Wnt.
Es probable que este descubrimiento tenga amplias implicaciones, ya que las vías competidoras Shh y Wnt funcionan en muchos otros ámbitos de la biología, incluida la progresión del cáncer de colon y el desarrollo de la diabetes tipo II.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
Para probar esta idea, establecieron una pantalla genómica para buscar inhibidores de Wnt activados por Vax. Descubrieron que Vax se unía a una secuencia de ADN, o promotor, inusualmente ubicada en medio de un gen, en lugar de flanquearlo. Y ese gen, designado Tcf7l2, codificaba un factor de transcripción que normalmente utiliza Wnt para dorsalizar el tejido diana.
La paradoja se explicó cuando el grupo demostró que Vax activaba la expresión de un señuelo molecular, a saber, un fragmento de la proteína Tcf7l2 al que le faltaba su extremo frontal, la parte necesaria para activar la expresión génica. Cuando se unía al ADN, el fragmento reclutaba proteínas represoras para silenciar las señales de dorsalización. “Las células que expresaban el inhibidor serían ciegas a la señalización Wnt”, dice Lemke.
Las proteínas Tcf7l2 de cuerpo completo se emparejan con un activador llamado ß-catenina. Pero la Tcf7l2 truncada carece de la región de interacción con ß-catenina, lo que interrumpe su función. Los científicos llaman a estas proteínas interferentes “negativos dominantes”.”
Tomas Vacik, Ph.D., un becario postdoctoral en el laboratorio de Lemke y primer autor del estudio, reevaluó los patrones de expresión génica en ratones que el laboratorio había diseñado para carecer de Vax2. “Descubrimos que Vax2 era necesario para la expresión de un grupo de antagonistas de Wnt en el ojo del ratón, incluido el Tcf7l2 dominante negativo”, dice.
El análisis bioinformático de la secuencia de ADN de Tcf7l2 unida por Vax reveló otra sorpresa. Aproximadamente 700 pares de bases, o nucleótidos, del genoma del ratón alrededor del sitio de unión de Vax en Tcf7l2 mostraron una asombrosa identidad del 99% entre ratones, humanos y pollos, y una identidad del 85% con peces, una conservación que Lemke califica de “excepcional en el extremo”.
“Esto significa que durante varios millones de años de evolución, la Madre Naturaleza dice que no puedes cambiar un solo nucleótido”, dice. “Eso te dice de inmediato que esta secuencia de ADN cumple una función reguladora muy importante”.”
Las búsquedas en bases de datos revelaron que la Tcf7l2 truncada se expresa en células del cerebro humano, y el propio análisis del grupo reveló construcciones similares en las cabezas de embriones de rana. “Estos resultados sugieren que la dnTcf7l2 se ha conservado mucho durante la evolución por su capacidad para reprimir potentemente los genes diana de Wnt”, dice Vacik.
Previamente, otros investigadores descubrieron que los ratones que albergan mutaciones en genes inhibidores de Wnt a menudo exhiben cerebros anteriores severamente truncados. Por lo tanto, el grupo se preguntó si la pérdida del Tcf7l2 dominante negativo alteraría la formación de la cabeza. Para probarlo, inyectaron embriones de rana con un ARN corto e inhibitorio diseñado para degradar artificialmente la versión de rana del Tcf7l2 truncado.
Los embriones resultantes carecían esencialmente de cabeza, mostrando la pérdida completa de estructuras delante del mesencéfalo, el punto exacto donde la señalización Wnt se detiene abruptamente en embriones normales de ratón o rana, debido al morfógeno ventral opuesto sonic hedgehog y su secuaz Vax. Este es el primer estudio que proporciona una explicación de cómo se traza esta línea molecular divisoria.
“Nuestros resultados ilustran un principio muy básico: si tienes el poder de encender algo, debes tener la capacidad de apagarlo. De lo contrario, se crea una situación de señalización incontrolada”, dice Lemke.
El resultado desastroso de una señalización descontrolada también se ilustra por el hecho de que las células cancerosas a menudo muestran una reactivación aberrante de los factores que rigen el desarrollo normal. Algunos tumores de cáncer de colon, por ejemplo, muestran altos niveles de la proteína ß-catenina, compañera de Tcf7l2, y la señalización descontrolada resultante de Wnt causa la enfermedad. De manera más intrigante, la incapacidad de las células tumorales para producir una forma corta e inhibitoria de un factor relacionado con Tcf7l2 también se asocia con la tumorigénesis.
“Así que Wnts y sonic hedgehog podrían estar en competencia en el cáncer de colon, al igual que lo están en el cerebro”, dice Lemke. “Nuestro trabajo podría ofrecer una perspectiva sobre cómo sucede eso a nivel mecánico”.”
También contribuyó a este estudio Jennifer Stubbs, Ph.D., ex becaria postdoctoral en el Laboratorio de Neurobiología Molecular, ahora en Pathway Genomics en San Diego.
La financiación para el estudio provino de los Institutos Nacionales de Salud.
Sobre los Institutos Nacionales de Salud (NIH):
La Agencia Nacional de Investigación Médica de los Estados Unidos (NIH, por sus siglas en inglés) está compuesta por 27 institutos y centros y forma parte del Departamento de Salud y Servicios Humanos de los EE. UU. Es la principal agencia federal para la realización y el apoyo de la investigación médica básica, clínica y traslacional, e investiga las causas, tratamientos y curas de enfermedades comunes y raras. Para obtener más información sobre los NIH y sus programas, visite www.nih.gov.
Acerca del Instituto Salk de Estudios Biológicos:
El Instituto Salk de Estudios Biológicos es una de las instituciones de investigación básica más destacadas del mundo, donde un cuerpo docente de prestigio internacional investiga cuestiones fundamentales de las ciencias de la vida en un entorno único, colaborativo y creativo. Centrados tanto en el descubrimiento como en la formación de las futuras generaciones de investigadores, los científicos del Salk realizan contribuciones revolucionarias a nuestra comprensión del cáncer, el envejecimiento, el Alzheimer, la diabetes y las enfermedades infecciosas mediante el estudio de la neurociencia, la genética, la biología celular y vegetal, y otras disciplinas relacionadas.
Los logros del cuerpo docente han sido reconocidos con numerosos galardones, entre los que se incluyen premios Nobel y la pertenencia a la Academia Nacional de Ciencias. Fundado en 1960 por el Dr. Jonas Salk, pionero en la vacuna contra la poliomielitis, el Instituto es una organización independiente sin fines de lucro y un hito arquitectónico.
Para más información:
Genes y Desarrollo
Edición 25: en prensa
Autores: Tomas Vacik, Jennifer L. Stubbs y Greg Lemke
Un mecanismo novedoso para la regulación transcripcional de la señalización Wnt en el desarrollo
Oficina de Comunicaciones
Tel.: (858) 453-4100
press@salk.edu