
10 de noviembre de 2008
La Jolla, CA – En un estudio que podría tener consecuencias significativas para las estrategias de trasplante de tejido neural, investigadores del Salk Institute for Biological Studies informan que la inactivación de un gen específico en células madre neurales adultas hace que las células nerviosas que emergen de esas células precursoras formen conexiones en la parte equivocada del cerebro adulto.
En un artículo publicado en la edición del 11 de noviembre de PLoS Biología, el equipo, liderado por Fred H. Gage, Ph.D., profesor en el Laboratorio de Genética, descubrió que una proteína llamada cdk5 es necesaria tanto para la correcta elaboración de antenas altamente ramificadas y complejas, conocidas como dendritas, que son extendidas por las neuronas, como para la migración adecuada de las células que portan dichas antenas.
Las funciones previamente descritas de cdk5 son múltiples, entre ellas la migración neuronal y la orientación de las dendritas de las neuronas nacidas durante el desarrollo embrionario. “El elemento sorprendente fue que las dendritas de las células granulares recién nacidas en el hipocampo adulto que carecían de cdk5 se estiraron en la dirección incorrecta y formaron sinapsis con las células equivocadas”, explica Gage. Las sinapsis son los puntos de contacto especializados donde las dendritas reciben información de los largos procesos, o axones, de las neuronas vecinas.
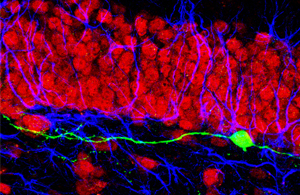
Las neuronas recién nacidas que carecen de cdk5 (verde) extienden dendritas aberrantes que, no obstante, se integran sinápticamente en el circuito del giro dentado preexistente que contiene neuronas (rojo) y células gliales (azul).
Imagen: Cortesía del Dr. Sebastian Jessberger, Instituto Federal de Tecnología, Zúrich, Suiza.
Estos hallazgos ofrecen información extremadamente valiosa, aunque imprevista, para los investigadores cuyo objetivo es desarrollar estrategias de trasplante para tratar lesiones cerebrales o neurodegeneración.
“Nuestros datos muestran que las células que no logran encontrar su ‘lugar correcto’ podrían integrarse en el cerebro e interferir con el procesamiento normal de la información”, afirma el autor principal del estudio, Sebastian Jessberger, M. D., ex postdoctorado en el laboratorio de Gage y ahora profesor asistente en el Instituto Federal Suizo de Tecnología de Zúrich, Suiza.
Gage coincide en que esta es una posibilidad, señalando que la focalización terapéutica de tejido nuevo —que presumiblemente se derivaría de células madre— al cerebro o la médula espinal puede exigir una precisión extrema. “Nuestros hallazgos reflejan la necesidad de enfoques terapéuticos que aseguren que las células utilizadas en medicina regenerativa se coloquen estratégicamente para que establezcan conexiones apropiadas en lugar de promiscuas”.”
En el estudio, los investigadores primero inyectaron retrovirus en una parte del cerebro de ratones adultos conocida como el hipocampo, que es necesaria para la formación de la memoria, para etiquetar y eliminar la actividad de cdk5 en las neuronas de gránulos recién nacidas. Con el tiempo, observaron que las neuronas recién nacidas no solo no se movieron a su posición correcta en el cerebro, sino que también presentaron dendritas atrofiadas y mal dirigidas.
Jessberger explica que uno podría haber predicho lo contrario: que si las neuronas inmaduras en el cerebro adulto orientaban accidentalmente sus antenas en la dirección equivocada, podrían no conectarse con las células de esa red, o incluso morir. Que formaran puntos de contacto sináptico fue muy inesperado. “Descubrimos que las dendritas de las células que carecían de cdk5 parecían integrarse en el cerebro sin importar la dirección en que crecieran”, dice.
De hecho, las conexiones sinápticas inapropiadas establecidas por las células deficientes en cdk5 persistieron durante meses después del tratamiento con retrovirus que antagonizan la cdk5. “Uno podría haber predicho que las neuronas inmaduras aberrantes serían expulsadas del circuito más adelante”, informa Jessberger, quien siguió el comportamiento de las nuevas células granulares en ratones tratados mucho después de que se eliminara la actividad de la cdk5. “Incluso después de un año, algunas de esas células permanecieron en la parte incorrecta del hipocampo”.”
El PLoS Biología el artículo es parte de un extenso cuerpo de trabajo aportado por el laboratorio de Gage al campo de la neurogénesis adulta. Hace una década, Gage se convirtió en uno de los primeros investigadores en el mundo en demostrar la aparición de nuevas neuronas en el cerebro de mamíferos adultos, incluidos los humanos. El estudio actual extiende específicamente una investigación de 2005 PNAS estudio en el que el laboratorio buscó en todo el genoma puntos calientes cromosómicos asociados con la neurogénesis adulta.
Ese estudio, que fue iniciado por el ex becario postdoctoral Gerd Kempermann, M.D., coautor en el PLoS Biología papel y, actualmente profesor en el Centro de Terapias Regenerativas de Dresde (CRTD), había identificado una gran región del cromosoma 5 de ratón como un área de interés, y cdk5 era un gen incrustado dentro de ese locus.
“La parte interesante de esta historia es que surgió de un enfoque de genética de sistemas”, dice Gage. “Continúa nuestro esfuerzo por aplicar el análisis genético para encontrar regiones cromosómicas que albergan genes que pueden desempeñar un papel crítico en la neurogénesis”.”
También contribuyeron al estudio, del laboratorio Gage, Stefan Aigner, Ph.D., Gregory D. Clemenson, Jr., Nicolas Toni, Ph.D., y D. Chichung Lie, M.D. Özlem Karalay de ETH y Rupert Overall de CRTD también fueron autores del artículo.
El estudio fue financiado por la Fundación Nacional Suiza para la Ciencia y la Deutsche Forschungsgemeinschaft y subvenciones de los National Institutes of Health, el Lookout Fund, la Christopher and Dana Reeve Foundation, la Picower Foundation, la James S. McDonnell Foundation, y la Damon Runyon Cancer Research Foundation.
El Instituto Salk de Estudios Biológicos en La Jolla, California, es una organización independiente sin fines de lucro dedicada a descubrimientos fundamentales en las ciencias de la vida, la mejora de la salud humana y la formación de futuras generaciones de investigadores. Jonas Salk, M.D., cuya vacuna contra la polio prácticamente erradicó la paralizante poliomielitis en 1955, fundó el Instituto en 1960 con un donativo de terrenos de la Ciudad de San Diego y el apoyo financiero de la March of Dimes.
Oficina de Comunicaciones
Tel.: (858) 453-4100
press@salk.edu