
21 de febrero de 2018
Investigadores de Salk utilizan tecnologías de vanguardia para revelar las diferencias en el control neural de brazos y piernas
Investigadores de Salk utilizan tecnologías de vanguardia para revelar las diferencias en el control neural de brazos y piernas
LA JOLLA—Las piernas y los brazos desempeñan funciones muy diferentes. Nuestras piernas son responsables principalmente de la locomoción repetitiva, como caminar y correr. Nuestros brazos y manos, por el contrario, deben ser capaces de ejecutar muchas tareas altamente especializadas: recoger un bolígrafo y escribir, sostener un tenedor o tocar el violín, por nombrar solo tres.
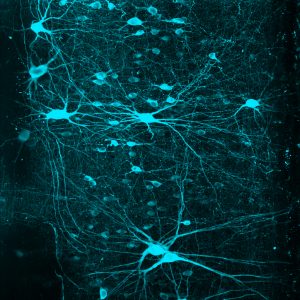
Haga clic aquí para obtener una imagen en alta resolución.
Crédito: Instituto Salk
Pero la regulación neuronal por las regiones de la médula espinal que se conectan a los brazos y aquellas que se conectan a las piernas no se comprende bien. Ahora, un estudio del Salk Institute en ratones ha revelado contrastes en las neuronas que subyacen a estos diversos tipos de control motor. Los resultados, que algún día podrían conducir a tratamientos personalizados basados en células madre para reparar lesiones de la médula espinal, se publicaron en la revista Neurona el 21 de febrero de 2018.
“La forma clásica de pensar sobre la médula espinal es que es una columna continua de neuronas que se conecta al cerebro o a los músculos”, dice Samuel Pfaff, investigador del Instituto Médico Howard Hughes en Salk y autor principal del estudio. “Si miras imágenes de secciones transversales de la médula espinal, podría haber variaciones sutiles en la forma entre las áreas que controlan los brazos y las que controlan las piernas, pero no es obvio que haya diferencias importantes”.”
Gracias a un puñado de tecnologías de laboratorio de vanguardia, los investigadores ahora pueden descifrar las distinciones que conducen a la especialización del control motor en los dos pares de extremidades.
Una de estas técnicas es el uso de marcadores moleculares para identificar subpoblaciones de células. En el estudio actual, los investigadores se enfocaron en un grupo de neuronas llamadas V2a que expresan el gen CHX10 (pronunciado “chex ten”). “Ya sabíamos que estas neuronas contribuyen al movimiento en todos los niveles de la columna vertebral”, dice Pfaff, quien ostenta la Cátedra Benjamin H. Lewis. “Pero esto planteó una situación paradójica: ¿qué podría ser diferente en las neuronas V2a a nivel cervical, que controla los brazos, en comparación con el nivel lumbar, que controla las piernas?”.”

Haga clic aquí para una imagen de alta resolución
Crédito: Instituto Salk
Resulta que, aunque las neuronas V2a están presentes en toda la columna vertebral, no todas expresan CHX10 en los mismos niveles. Primero, el equipo utilizó una tecnología llamada secuenciación de ARN para estudiar las diferencias en la expresión génica de las neuronas V2a entre las áreas de los brazos y las áreas de las piernas (que se cree que son equivalentes a las extremidades anteriores y posteriores en los animales). Marito Hayashi, asociado de investigación postdoctoral y primer autor, descubrió que en la médula espinal del ratón dos poblaciones principales de estas neuronas están graduadas, pasando de una población a otra. En la región cervical (brazo), las neuronas se dividen 50-50 entre las que expresan el gen y las que no, mientras que en la región lumbar (pierna), la mayoría de las neuronas V2a lo expresan.
Los investigadores utilizaron una tecnología llamada optogenética (donde la luz se usa para activar y desactivar selectivamente células) para observar cómo las neuronas V2a se conectaban a las neuronas que controlan los músculos. Descubrieron que cuando se estimulaban las neuronas V2a a nivel cervical, las conexiones con las neuronas motoras eran débiles, mientras que en la región lumbar, las conexiones eran fuertes y rápidas.
Empleando posteriormente una técnica de laboratorio en la que se utiliza un virus de la rabia modificado para rastrear circuitos neuronales, el equipo reveló que en la región cervical, muchas de las neuronas V2a que no expresan la CHX10 los genes estaban conectados al cerebro. En cambio, en la región lumbar, donde la mayoría de las neuronas V2a expresan el gen, estas estaban fuertemente conectadas a neuronas motoras y entre sí. Esto tiene sentido, según Pfaff, porque los movimientos de manos y brazos necesitan ser cuidadosamente coordinados con el cerebro, mientras que los movimientos de las piernas son más automatizados.
“Históricamente, la gente ha tratado a las neuronas V2a como una población idéntica en todas las regiones —agrega Hayashi—. Pero descubrimos que, dependiendo del segmento dentro de la médula espinal, su perfil molecular, y por lo tanto su función, era diferente”.“
El equipo de Salk, incluido el especialista en bioinformática Shawn Driscoll, investigó si había más de dos poblaciones principales de neuronas V2a empleando la secuenciación de ARN de célula única, una tecnología que permite la identificación de genes únicos expresados a nivel de resolución de células individuales. Esta investigación condujo a la identificación adicional de 11 grupos únicos de neuronas V2a.
El trabajo futuro se centrará más en las diferencias moleculares entre estas neuronas.
“Esperamos realizar un análisis más detallado para conectar diferentes neuronas con sus funciones”, dice Hayashi. Si sus hallazgos también son ciertos en humanos, este trabajo podría algún día conducir a tratamientos personalizados para reparar lesiones de la médula espinal, posiblemente con el uso de células madre.
“En este momento, usar células madre para reparar lesiones de la médula espinal es algo que aún no sabemos cómo lograr”, dice Pfaff. “Uso la analogía de intentar corregir un problema en el sistema eléctrico de un auto abriendo el capó y simplemente arrojando un montón de cables. Con este trabajo, estamos un paso más cerca de descubrir qué hacen realmente todos esos cables diferentes”.”
Los otros autores del artículo fueron Christopher Hinckley, Niall Moore, Kathryn Hilde y Ariel Levine del Salk, y Kamal Sharma de la Universidad de Illinois en Chicago. Hinckley está ahora en Biogen, Levine está ahora en el Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares, y Hilde está ahora en la Universidad de Míchigan.
La investigación fue apoyada por fondos del Howard Hughes Medical Institute y el Sol Goldman Charitable Trust.
DIARIO
Neurona
AUTORES
Marito Hayashi, Christopher A. Hinckley, Shawn P. Driscoll, Niall J. Moore, Ariel J. Levine, Kathryn L. Hilde, Kamal Sharma y Samuel L. Pfaff
Oficina de Comunicaciones
Tel.: (858) 453-4100
press@salk.edu
El Instituto Salk es un centro de investigación independiente y sin fines de lucro fundado en 1960 por Jonas Salk, creador de la primera vacuna segura y eficaz contra la poliomielitis. La misión del Instituto es impulsar una investigación fundamental, colaborativa y audaz que aborde los retos más acuciantes de la sociedad, entre ellos el cáncer, la enfermedad de Alzheimer y la vulnerabilidad agrícola. Esta ciencia fundamental sustenta todos los esfuerzos traslacionales, generando conocimientos que permiten el desarrollo de nuevos medicamentos e innovaciones en todo el mundo.