
13 de agosto de 2014
Los investigadores de Salk descubren un gen maestro responsable de los ciclos de sueño y vigilia, lo que ofrece la esperanza de un fármaco que podría ayudar a restablecer el sueño
Los investigadores de Salk descubren un gen maestro responsable de los ciclos de sueño y vigilia, lo que ofrece la esperanza de un fármaco que podría ayudar a restablecer el sueño
LA JOLLA–Los científicos del Instituto Salk de Estudios Biológicos han identificado un gen que regula los ritmos de sueño y vigilia.
El descubrimiento del papel de este gen, llamado Lhx1, proporciona a los científicos un objetivo terapéutico potencial para ayudar a los trabajadores del turno de noche o a los viajeros con jet lag a adaptarse a las diferencias horarias más rápidamente. Los resultados, publicados en ELIFE, puede señalar estrategias de tratamiento para los problemas del sueño causados por una variedad de trastornos.
“Es posible que la gravedad de muchas demencias provenga de trastornos del sueño”, dice panda satchidananda, profesor asociado de Salk que dirigió el equipo de investigación. “Si podemos restaurar el sueño normal, podemos abordar la mitad del problema”.
Cada célula del cuerpo tiene un "reloj": una gran cantidad de proteínas que bajan o suben rítmicamente durante aproximadamente 24 horas. El reloj maestro responsable de establecer estos ritmos circadianos cíclicos y mantener sincronizadas todas las células del cuerpo es el núcleo supraquiasmático (SCN), una pequeña región densamente poblada de aproximadamente 20,000 neuronas alojadas en el hipotálamo del cerebro.
Más que en otras áreas del cerebro, las neuronas del SCN están en estrecha y constante comunicación entre sí. Esta estrecha interacción, combinada con la exposición a la luz y la oscuridad a través de los circuitos de visión, mantiene este reloj maestro sincronizado y permite que las personas sigan esencialmente el mismo horario todos los días. El estrecho acoplamiento de estas células también ayuda a que sean colectivamente resistentes al cambio. La exposición a la luz restablece menos de la mitad de las células SCN, lo que resulta en largos períodos de desfase horario.
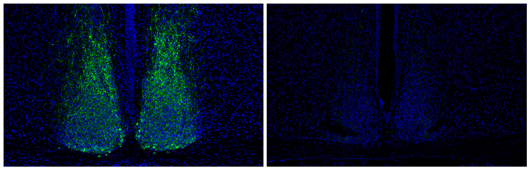
Un péptido responsable de la comunicación celular en el cerebro, Vip (verde) se reduce en los cerebros de ratones que tienen poco o nada de Lhx1 (derecha).
Haga clic aquí para una imagen de alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
En el nuevo estudio, los investigadores interrumpieron los ciclos de luz y oscuridad en ratones y compararon los cambios en la expresión de miles de genes en el SCN con otros tejidos de ratón. Identificaron 213 cambios en la expresión génica que eran exclusivos del SCN y se concentraron en 13 de estos que codificaban moléculas que activan y desactivan otros genes. De esos, solo uno fue suprimido en respuesta a la luz: Lhx1.
"Nadie había imaginado que Lhx1 podría estar tan intrincadamente involucrado en la función SCN", dice Shubhroz Gill, investigador postdoctoral y coautor del artículo. Lhx1 es conocido por su papel en el desarrollo neuronal: es tan importante que los ratones sin el gen no sobreviven. Pero esta es la primera vez que se identifica como un regulador maestro de los genes del ciclo de luz y oscuridad.
Al registrar la actividad eléctrica en el SCN de animales con cantidades reducidas de la proteína Lhx1, los investigadores vieron que las neuronas del SCN no estaban sincronizadas entre sí, a pesar de que parecían rítmicas individualmente.
"Se trataba de comunicación: las neuronas no se comunicaban entre sí sin esta molécula", dice Ludovic Mure, investigador postdoctoral y autor del artículo. El próximo paso en el trabajo será comprender exactamente cómo Lhx1 afecta la expresión de los genes que crean esta sincronicidad.
Al estudiar una versión de ratón del desfase horario, un cambio de 8 horas en su ciclo de día y noche, los científicos descubrieron que aquellos con poco o nada de Lhx1 se reajustaron mucho más rápido al cambio que los ratones normales. Esto sugiere que debido a que estas neuronas están menos sincronizadas entre sí, pueden cambiar más fácilmente a un nuevo horario, aunque les resulta difícil mantener ese horario, dice Panda.
Estos ratones también exhibieron una actividad reducida de ciertos genes, incluido uno que crea el péptido intestinal vasoactivo o Vip, una molécula que tiene funciones importantes en el desarrollo y como hormona en el intestino y la sangre. En el cerebro, Vip afecta la comunicación celular, pero nadie sabía que Lhx1 lo regulaba hasta ahora, dice Panda. Curiosamente, el equipo también descubrió que agregar Vip restauró la sincronía celular en el SCN.
“Este enfoque nos ayudó a cerrar esa brecha de conocimiento y demostrar que Vip es una proteína muy importante, al menos para SCN”, dice Panda. "Puede compensar la pérdida de Lhx1".
Por otro lado, reducir el consumo de Vip podría ser otra forma de tratar el desfase horario. Vip podría ser un objetivo farmacológico aún más fácil en comparación con Lhx1 porque Vip se secreta desde las células en lugar de dentro de las células, dice Panda. “Si encontramos un fármaco que bloquee el receptor Vip o de alguna manera rompa Vip, entonces tal vez eso nos ayude a reiniciar el reloj mucho más rápido”, agrega.
Los nuevos resultados llevan al grupo un paso más cerca de su objetivo de crear terapias de regeneración celular que restauren el SCN y mejoren los problemas del sueño. Los científicos han puesto a disposición sus datos de expresión génica a través de una interfaz web de búsqueda en http://scn.salk.edu, brindando a otros investigadores una forma práctica de explorar el efecto de la luz y la oscuridad en los genes del SCN y otros tejidos.
Otros investigadores del estudio fueron Megumi Hatori, ahora en la Facultad de Medicina de la Universidad de Keio en Tokio, y Martin Goulding y Dennis DM O'Leary de Salk.
El trabajo fue apoyado por becas de La Sociedad Japonesa para la Promoción de la Ciencia, Messinger Vida Sana, el Fundación Fyssen y Catharina, Fundación Mary K. Chapman, El Fondo Benéfico Leona M. y Harry B. Helmsley, el Los Institutos Nacionales de Salud, Fundación Hearst y Fundación Glenn.
Sobre el Instituto Salk de Estudios Biológicos:
El Instituto Salk de Estudios Biológicos es una de las instituciones de investigación básica más importantes del mundo, donde profesores de renombre internacional investigan cuestiones fundamentales de las ciencias de la vida en un entorno único, colaborativo y creativo. Centrados tanto en el descubrimiento como en la orientación de futuras generaciones de investigadores, los científicos de Salk realizan contribuciones innovadoras a nuestra comprensión del cáncer, el envejecimiento, el Alzheimer, la diabetes y las enfermedades infecciosas mediante el estudio de la neurociencia, la genética, la biología celular y vegetal y disciplinas relacionadas.
Los logros de la facultad han sido reconocidos con numerosos honores, incluidos premios Nobel y membresías en la Academia Nacional de Ciencias. Fundado en 1960 por el pionero de la vacuna contra la polio Jonas Salk, MD, el Instituto es una organización independiente sin fines de lucro y un hito arquitectónico.
REVISTA
ELIFE
AUTORES
Megumi Hatori, Shubhroz Gill, Ludovic S. Mure, Martyn Goulding, Dennis DM O'Leary, Satchidananda Panda
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu