
15 de diciembre de 2016
Nueva técnica rejuveneció órganos y ayudó a los animales a vivir más tiempo
Nueva técnica rejuveneció órganos y ayudó a los animales a vivir más tiempo
LA JOLLA—Cabello canoso, patas de gallo, una lesión que está tardando más en sanar que cuando teníamos 20 años—frente a los signos inconfundibles del envejecimiento, la mayoría de nosotros ha tenido al menos una fantasía de volver atrás en el tiempo. Ahora, los científicos del Instituto Salk han descubierto que la expresión intermitente de genes normalmente asociados con un estado embrionario puede revertir las características de la vejez.
Este enfoque, que no solo hizo que las células de la piel humana en un plato se vieran y se comportaran jóvenes nuevamente, también resultó en el rejuvenecimiento de ratones con una enfermedad de envejecimiento prematuro, contrarrestando los signos del envejecimiento y aumentando la vida útil de los animales en un 30 por ciento. El trabajo en etapa inicial proporciona información tanto sobre los impulsores celulares del envejecimiento como sobre posibles enfoques terapéuticos para mejorar la salud y la longevidad humanas.
“Nuestro estudio muestra que es posible que el envejecimiento no tenga que avanzar en una sola dirección”, dice Juan Carlos Izpisúa Belmonte, profesor del Laboratorio de Expresión Génica de Salk y autor principal del artículo que aparece en la edición del 15 de diciembre de 2016 de Celular. “Tiene plasticidad y, con una modulación cuidadosa, el envejecimiento podría revertirse”.
A medida que las personas en las sociedades modernas viven más tiempo, aumenta el riesgo de desarrollar enfermedades relacionadas con la edad. De hecho, los datos muestran que el mayor factor de riesgo de enfermedades cardíacas, cáncer y trastornos neurodegenerativos es simplemente la edad. Una pista para detener o revertir el envejecimiento radica en el estudio de la reprogramación celular, un proceso en el que la expresión de cuatro genes conocidos como factores de Yamanaka permite a los científicos convertir cualquier célula en células madre pluripotentes inducidas (iPSC). Al igual que las células madre embrionarias, las iPSC son capaces de dividirse indefinidamente y convertirse en cualquier tipo de célula presente en nuestro cuerpo.
Haga clic aquí para una imagen de alta resolución
Crédito: Instituto Salk
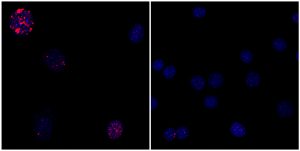
“Lo que nosotros y otros laboratorios de células madre hemos observado es que cuando induces la reprogramación celular, las células se ven más jóvenes”, dice Alejandro Ocampo, investigador asociado y primer autor del artículo. "La siguiente pregunta era si podíamos inducir este proceso de rejuvenecimiento en un animal vivo".
Si bien el rejuvenecimiento celular ciertamente suena deseable, un proceso que funciona para células de laboratorio no es necesariamente una buena idea para un organismo completo. Por un lado, aunque la división celular rápida es crítica en los embriones en crecimiento, en los adultos ese crecimiento es una de las características del cáncer. Por otro lado, hacer que un gran número de células vuelvan al estado embrionario en un adulto podría provocar una falla orgánica y, en última instancia, conducir a la muerte. Por estas razones, el equipo de Salk se preguntó si podrían evitar el cáncer y mejorar las características del envejecimiento mediante la inducción de los factores de Yamanaka durante un corto período de tiempo.
Para averiguarlo, el equipo recurrió a una rara enfermedad genética llamada progeria. Tanto los ratones como los humanos con progeria muestran muchos signos de envejecimiento, incluidos daños en el ADN, disfunción de órganos y una vida útil drásticamente más corta. Además, las marcas químicas en el ADN responsables de la regulación de los genes y la protección de nuestro genoma, conocidas como marcas epigenéticas, se desregulan prematuramente en ratones y humanos con progeria. Es importante destacar que las marcas epigenéticas se modifican durante la reprogramación celular.
Haga clic aquí para una imagen de alta resolución.
Crédito: Instituto Salk
Utilizando células de la piel de ratones con progeria, el equipo indujo los factores de Yamanaka durante un período breve. Cuando examinaron las células utilizando métodos de laboratorio estándar, las células mostraron una reversión de múltiples características del envejecimiento sin perder su identidad de células de la piel.
"En otros estudios, los científicos han reprogramado por completo las células hasta volverlas a un estado similar al de las células madre", dice el coautor principal Pradeep Reddy, también investigador asociado de Salk. "Pero mostramos, por primera vez, que al expresar estos factores durante un período breve se puede mantener la identidad de la célula mientras se revierten las características asociadas con la edad".
Alentados por este resultado, el equipo utilizó el mismo método de reprogramación breve durante períodos cíclicos en ratones vivos con progeria. Los resultados fueron sorprendentes: en comparación con los ratones no tratados, los ratones reprogramados parecían más jóvenes; su función cardiovascular y de otros órganos mejoró y, lo más sorprendente de todo, vivieron un 30 por ciento más, pero no desarrollaron cáncer. A nivel celular, los animales mostraron la recuperación de las características moleculares del envejecimiento que se ven afectadas no solo en la progeria, sino también en el envejecimiento normal.
"Este trabajo muestra que los cambios epigenéticos están impulsando el envejecimiento, al menos parcialmente", dice la coautora principal Paloma Martínez-Redondo, otra investigadora asociada de Salk. "Nos brinda información emocionante sobre qué vías podrían abordarse para retrasar el envejecimiento celular".

Haga clic aquí para una imagen de alta resolución.
Crédito: Instituto Salk
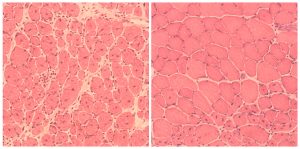
Por último, los científicos de Salk centraron sus esfuerzos en ratones normales envejecidos. En estos animales, la inducción cíclica de los factores de Yamanaka condujo a una mejora en la capacidad de regeneración del páncreas y el músculo. En este caso, el páncreas y el músculo lesionados se curaron más rápido en ratones viejos que fueron reprogramados, lo que indica una clara mejora en la calidad de vida por la reprogramación celular.
“Obviamente, los ratones no son humanos y sabemos que será mucho más complejo rejuvenecer a una persona”, dice Izpisua Belmonte. “Pero este estudio muestra que el envejecimiento es un proceso muy dinámico y plástico y, por lo tanto, será más susceptible a las intervenciones terapéuticas de lo que pensábamos anteriormente”.
Los investigadores de Salk creen que la inducción de cambios epigenéticos a través de productos químicos o moléculas pequeñas puede ser el enfoque más prometedor para lograr el rejuvenecimiento en humanos. Sin embargo, advierten que, debido a la complejidad del envejecimiento, estas terapias pueden tardar hasta 10 años en llegar a los ensayos clínicos.
Otros autores incluyeron: Aida Platero-Luengo, Fumiyuki Hatanaka, Tomoaki Hishida, Mo Li, David Lam, Masakazu Kurita, Ergin Beyret, Toshikazu Araoka, Eric Vazquez-Ferrer, David Donoso, Jose Luis Roman, Jinna Xu y Concepcion Rodriguez of the Salk Instituto; Estrella Núñez Delicado de Universidad Católica San Antonio de Murcia; Gabriel Núñez de la Escuela de Medicina de la Universidad de Michigan; Josep María Campistol de Hospital Clínico de Barcelona e Isabel Guillén y Pedro Guillén de Fundación Dr. Pedro Guillén.
El trabajo y los investigadores involucrados fueron apoyados en parte por una Premio del Servicio Nacional de Investigación Ruth L. Kirschstein de los Institutos Nacionales de Salud Beca posdoctoral individual, la Asociación de Distrofia Muscular, Fundación Alfonso Martín Escudero, la Fundación Hewitt, la Fundación Uehara Memorial, la Fundación Nomis, Beca posdoctoral JSPS para investigación en el extranjero, la Universidad de California, San Diego, la Fundación benéfica G. Harold y Leila Y. Mathers, La Fundación Benéfica Leona M. y Harry B. Helmsley (2012-PG-MED002), La Fundación Glenn, Universidad Católica San Antonio de Murcia (UCAM) y Fundación Dr. Pedro Guillén.
PERIODICO
Celular
TÍTULO
In vivo mejora de las características asociadas con la edad mediante la reprogramación parcial
AUTORES
Alejandro Ocampo, Pradeep Reddy, Paloma Martinez-Redondo, Aida Platero-Luengo, Fumiyuki Hatanaka, Tomoaki Hishida, Mo Li, David Lam, Masakazu Kurita, Ergin Beyret, Toshikazu Araoka, Eric Vazquez-Ferrer, David Donoso, Jose Luis Roman, Jinna Xu, Concepción Rodríguez, Gabriel Núñez, Estrella Núñez-Delicado, Josep M. Campistol, Isabel Guillén, Pedro Guillén, and Juan Carlos Izpisua Belmonte.
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
Descubrir los secretos de la vida misma es la fuerza impulsora detrás del Instituto Salk. Nuestro equipo de científicos galardonados de clase mundial traspasa los límites del conocimiento en áreas como neurociencia, investigación del cáncer, envejecimiento, inmunobiología, biología vegetal, biología computacional y más. Fundado por Jonas Salk, desarrollador de la primera vacuna contra la polio segura y eficaz, el Instituto es una organización de investigación independiente y sin fines de lucro y un hito arquitectónico: pequeño por elección, íntimo por naturaleza y valiente ante cualquier desafío.