
30 de agosto de 2017
La síntesis hiperactiva de proteínas que se encuentra en la enfermedad del envejecimiento prematuro también puede desempeñar un papel en el envejecimiento normal
La síntesis hiperactiva de proteínas que se encuentra en la enfermedad del envejecimiento prematuro también puede desempeñar un papel en el envejecimiento normal
LA JOLLA—Puede parecer paradójico, pero estudiar lo que va mal en las enfermedades raras puede proporcionar información útil sobre la salud normal. Los investigadores que investigan el trastorno de envejecimiento prematuro progeria de Hutchinson-Gilford han descubierto un proceso de proteína errante en la enfermedad que podría ayudar a las personas sanas, así como a las personas que padecen progeria, a vivir más tiempo.
Los científicos del Instituto Salk descubrieron que la síntesis de proteínas es hiperactiva en personas con progeria. La obra, descrita en Nature Communications el 30 de agosto de 2017, se suma a un creciente cuerpo de evidencia de que la reducción de la síntesis de proteínas puede prolongar la vida útil y, por lo tanto, puede ofrecer un objetivo terapéutico útil para contrarrestar el envejecimiento prematuro y normal.
“La producción de proteínas es un proceso extremadamente intensivo en energía para las células”, dice Martín Hetzer, vicepresidente y director científico del Instituto Salk y autor principal del artículo. “Cuando una célula dedica valiosos recursos a la producción de proteínas, es posible que se descuiden otras funciones importantes. Nuestro trabajo sugiere que un impulsor del envejecimiento anormal y normal podría ser la renovación acelerada de proteínas”.
Haga clic aquí para una imagen de alta resolución.
Crédito: Instituto Salk
La progeria de Hutchinson-Gilford es una enfermedad genética muy rara que hace que las personas envejezcan de 8 a 10 veces más rápido que el resto de nosotros y conduce a una muerte prematura. La rara mutación ocurre en una de las proteínas estructurales del núcleo celular, la lámina A, pero no ha quedado claro cómo una sola proteína defectuosa en el núcleo causa la miríada de características de envejecimiento rápido que se observan en la enfermedad.
Inicialmente, la científica del personal de Salk, Abigail Buchwalter, primera autora del artículo, estaba interesada en saber si la mutación estaba haciendo que la proteína lamina A fuera menos estable y de vida más corta. Después de medir el recambio de proteínas en células cultivadas de biopsias de piel tanto de pacientes con progeria como de personas sanas, descubrió que no solo la lamina A estaba afectada por la enfermedad.
"Analizamos todas las proteínas del núcleo y, en lugar de ver una rotación rápida solo en la lamina A mutante y tal vez en algunas proteínas asociadas con ella, vimos un cambio muy amplio en la estabilidad general de la proteína en las células de progeria", dice Buchwalter. "Esto indicó un cambio en el metabolismo de las proteínas que no esperábamos".
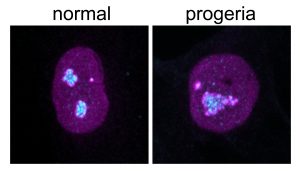
Junto con la rápida renovación de las proteínas, el equipo descubrió que el nucléolo, que produce las estructuras de ensamblaje de proteínas llamadas ribosomas, se agrandaba en las células que envejecían prematuramente en comparación con las células sanas.
Haga clic aquí para una imagen de alta resolución
Crédito: Instituto Salk
Aún más intrigante, el equipo descubrió que el tamaño del nucléolo aumentaba con la edad en las células sanas, lo que sugiere que el tamaño del nucléolo no solo podría ser un biomarcador útil del envejecimiento, sino también un objetivo potencial de las terapias para contrarrestar el envejecimiento prematuro y normal.
El trabajo respalda otra investigación que aparece en el mismo número que muestra que la disminución de la síntesis de proteínas prolonga la vida útil en gusanos redondos y ratones. El laboratorio de Hetzer planea continuar estudiando cómo el tamaño del nucléolo puede servir como un biomarcador confiable para el envejecimiento.
“Siempre asumimos que el envejecimiento es un proceso lineal, pero no lo sabemos con certeza”, dice Hetzer, quien también ocupa la cátedra de la Fundación Jesse y Caryl Philips. “Un biomarcador como este que rastrea el envejecimiento sería muy útil y podría abrir nuevas formas de estudiar y comprender el envejecimiento en humanos”.
El trabajo fue financiado por la Los Institutos Nacionales de Salud, el Fundación Nomis, y la Centro Glenn para la Investigación del Envejecimiento.
PERIODICO
Nature Communications
AUTORES
Abigail Buchwalter y Martin W. Hetzer
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
Descubrir los secretos de la vida misma es la fuerza impulsora detrás del Instituto Salk. Nuestro equipo de científicos galardonados de clase mundial traspasa los límites del conocimiento en áreas como neurociencia, investigación del cáncer, envejecimiento, inmunobiología, biología vegetal, biología computacional y más. Fundado por Jonas Salk, desarrollador de la primera vacuna contra la polio segura y eficaz, el Instituto es una organización de investigación independiente y sin fines de lucro y un hito arquitectónico: pequeño por elección, íntimo por naturaleza y valiente ante cualquier desafío.