
Sábado, Junio 25, 2015
El Instituto Salk y el Instituto de Descubrimiento Médico Sanford Burnham Prebys crearon un compuesto que detiene un proceso de reciclaje celular
El Instituto Salk y el Instituto de Descubrimiento Médico Sanford Burnham Prebys crearon un compuesto que detiene un proceso de reciclaje celular
LA JOLLA–A medida que crece un tumor, sus células cancerosas aceleran un proceso de recolección de energía para apoyar su desarrollo acelerado. Este proceso, llamado autofagia, normalmente lo utiliza una célula para reciclar orgánulos y proteínas dañados, pero también es cooptado por las células cancerosas para satisfacer sus mayores demandas metabólicas y de energía.
Instituto Salk y Instituto de descubrimiento médico de Sanford Burnham Prebys (SBP) científicos han desarrollado un fármaco que evita que este proceso se inicie en las células cancerosas. Publicado el 25 de junio de 2015 en Célula molecular, el nuevo estudio identifica un fármaco de molécula pequeña que bloqueó específicamente el primer paso de la autofagia, cortando efectivamente los nutrientes reciclados que las células cancerosas necesitan para vivir.
“El hallazgo abre la puerta a una nueva forma de atacar el cáncer”, dice Rubén Shaw, autor principal del artículo, profesor en la Laboratorio de Biología Molecular y Celular en el Instituto Salk y un Instituto Médico Howard Hughes Científico de carrera temprana. "El inhibidor probablemente encontrará la mayor utilidad en combinación con terapias dirigidas".
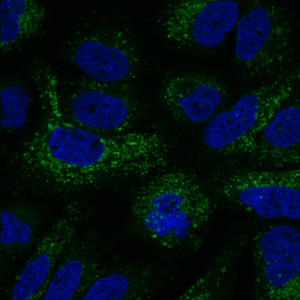
El reciclaje celular (que se muestra en verde) es elevado en las células de cáncer de pulmón tratadas con un medicamento contra el cáncer establecido. El reciclaje se suprime con el tratamiento conjunto con un inhibidor enzimático recién descubierto.
Haga clic aquí para una imagen de alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
Además del cáncer, los defectos en la autofagia se han relacionado con enfermedades infecciosas, neurodegeneración y problemas cardíacos. En un estudio de 2011 en la revista Science, Shaw y su equipo descubrieron cómo las células privadas de nutrientes activan la molécula clave que inicia la autofagia, una enzima llamada ULK1.
Con el razonamiento de que la inhibición de ULK1 podría eliminar algunos tipos de cáncer al sofocar un suministro de energía principal que proviene del proceso de reciclaje, el grupo de Shaw y otros querían encontrar un medicamento que inhibiera la enzima. Solo una fracción de esos inhibidores que se muestran prometedores en un tubo de ensayo terminan funcionando bien en las células vivas. El grupo de Shaw pasó más de un año estudiando cómo funciona ULK1 y desarrollando nuevas estrategias para evaluar su función en las células.
Un avance clave se produjo cuando Shaw conoció al otro autor principal del artículo, Nicholas Cosford, profesor en el Centro de Cáncer Designado por el NCI en SBP. Cosford había estado investigando ULK1 usando química médica y biología química, y había identificado algunos compuestos principales prometedores usando un diseño racional. Los dos laboratorios combinaron esfuerzos para seleccionar cientos de moléculas potenciales para la inhibición de ULK1, reduciendo la lista a unas pocas docenas y, finalmente, a una.
“La clave del éxito de este proyecto surgió cuando combinamos el profundo conocimiento de Reuben sobre la biología fundamental de la autofagia con nuestra experiencia química”, dice Cosford. “Esto nos permitió encontrar un fármaco dirigido a ULK1 no solo en un tubo de ensayo, sino también en células tumorales. Otro desafío fue encontrar moléculas que se dirigieran selectivamente a la enzima ULK1 sin afectar las células sanas. Nuestro trabajo proporciona la base para un fármaco novedoso que tratará el cáncer resistente cortando un proceso principal de supervivencia de las células tumorales”.
El resultado fue un fármaco altamente selectivo al que llamaron SBI-0206965, que eliminó con éxito varios tipos de células cancerosas, incluidas las células de cáncer de pulmón humano y de ratón y las células de cáncer de cerebro humano, algunas de las cuales se demostró que dependían particularmente del reciclaje celular.
Curiosamente, algunos medicamentos contra el cáncer (como los inhibidores de mTOR) activan aún más el reciclaje celular al bloquear la capacidad de esas células para absorber nutrientes, haciéndolas más dependientes del reciclaje para proporcionar todos los componentes básicos que las células necesitan para mantenerse con vida. La rapamicina, por ejemplo, actúa bloqueando el crecimiento y la división celular. En respuesta, las células entran en modo de reciclaje al activar ULK1, lo que puede ser una de las razones por las que, en lugar de morir, algunas células cancerosas parecen entrar en un estado latente y regresar, a menudo más resistentes a los medicamentos, después de que se detiene el tratamiento.

Matthew Chun, Nicholas Cosford y Reuben Shaw
Haga clic aquí para una imagen de alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
"La inhibición de ULK1 eliminaría este último mecanismo de supervivencia en las células cancerosas y podría hacer que los tratamientos contra el cáncer existentes sean mucho más efectivos", dice Matthew Chun, uno de los autores principales del estudio y becario postdoctoral en el laboratorio Shaw en Salk.
De hecho, la combinación de SBI-0206965 con inhibidores de mTOR lo hizo más efectivo, matando de dos a tres veces más células de cáncer de pulmón que SBI-0206965 solo o los inhibidores de mTOR solos.
Ya se ha intentado drogar la vía de la autofagia para combatir el cáncer, pero los únicos medicamentos que actualmente bloquean el reciclaje celular funcionan al atacar el orgánulo celular conocido como lisosoma, que funciona en la etapa final de la autofagia. Aunque estas terapias lisosomales se están probando en ensayos clínicos en etapas iniciales, inhiben otras funciones lisosomales más allá de la autofagia y, por lo tanto, pueden tener efectos secundarios adicionales.
Al comparar concentraciones equivalentes del fármaco lisosomal cloroquina con SBI-0206965, en combinación con inhibidores de mTOR, los científicos descubrieron que SBI-0206965 era mejor que la cloroquina para matar las células cancerosas.
El grupo ahora está probando el fármaco en modelos de ratón con cáncer. “Un próximo paso importante será probar este fármaco en otros tipos de cáncer y con otras combinaciones terapéuticas”, dice Shaw, subdirector del Centro Oncológico Designado por el NCI de Salk. “Mientras tanto, este descubrimiento brinda a los investigadores una nueva y emocionante caja de herramientas para la inhibición y medición del reciclaje celular”.
Otros autores del estudio incluyen al coautor principal Daniel Egan del Laboratorio de Biología Molecular y Celular de Salk; Mitchell Vamos, Haixia Zou, Juan Rong, Dhanya Raveendra-Panickar, Douglas Sheffler y Peter Teriete del Programa de Investigación de Redes de Supervivencia y Muerte Celular en el Centro de Cáncer Designado por el NCI en SBP; Chad Miller, Hua Jane Lou y Benjamin Turk del Departamento de Farmacología de la Facultad de Medicina de la Universidad de Yale; John Asara de la División de Transducción de Señales del Centro Médico Beth Israel Deaconess y del Departamento de Medicina de la Facultad de Medicina de Harvard; y Chih-Cheng Yang del Núcleo de Genómica Funcional de SBP.
La investigación fue apoyada por Los Institutos Nacionales de Salud, la Departamento de Defensa, y la Leona M. y Harry B. Helmsley Charitable Trust.
Acerca del Instituto de Descubrimiento Médico Sanford Burnham Prebys:
Sanford Burnham Prebys Medical Discovery Institute (SBP) es una organización de investigación independiente sin fines de lucro que combina la investigación fundamental de vanguardia con el descubrimiento sólido de fármacos para abordar las necesidades clínicas no satisfechas en las áreas de cáncer, neurociencia, inmunidad y trastornos metabólicos. El Instituto invierte en talento, tecnología y asociaciones para acelerar la traducción de los descubrimientos de laboratorio que tendrán el mayor impacto en los pacientes. Reconocido por su Centro de cáncer de clase mundial designado por el NCI y el Centro Conrad Prebys de genómica química, SBP emplea a más de 1,100 científicos y personal en San Diego (La Jolla), California, y Orlando (Lake Nona), Florida. Para obtener más información información, visítenos en SBPdiscovery.org. El Instituto también se puede encontrar en Facebook en facebook.com/SBPdiscovery y en Twitter @SBPdiscovery.
PERIODICO
Célula molecular
TÍTULO
Inhibición de moléculas pequeñas de la autofagia quinasa ULK1 e identificación de sustratos de ULK1
AUTORES
Daniel F. Egan, Matthew GH Chun, Mitchell Vamos, Haixia Zou, Juan Rong, Chad J. Miller, Hua Jane Lou, Dhanya Raveendra-Panickar, Chih-Cheng Yang, Douglas J. Sheffler, PeterTeriete, John M. Asara, Benjamin E. Turk, Nicholas DP Cosford y Reuben J. Shaw
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
Descubrir los secretos de la vida misma es la fuerza impulsora detrás del Instituto Salk. Nuestro equipo de científicos galardonados de clase mundial traspasa los límites del conocimiento en áreas como neurociencia, investigación del cáncer, envejecimiento, inmunobiología, biología vegetal, biología computacional y más. Fundado por Jonas Salk, desarrollador de la primera vacuna contra la polio segura y eficaz, el Instituto es una organización de investigación independiente y sin fines de lucro y un hito arquitectónico: pequeño por elección, íntimo por naturaleza y valiente ante cualquier desafío.