
16 de noviembre.
Los investigadores de Salk han descubierto, por primera vez, cómo colocar el ADN en ubicaciones específicas en células que no se dividen
Los investigadores de Salk han descubierto, por primera vez, cómo colocar el ADN en ubicaciones específicas en células que no se dividen
LA JOLLA—Los investigadores del Instituto Salk han descubierto el santo grial de la edición de genes: la capacidad de, por primera vez, insertar ADN en una ubicación objetivo en las células que no se dividen y que constituyen la mayoría de los órganos y tejidos adultos. La técnica, que el equipo demostró que podía restaurar parcialmente las respuestas visuales en roedores ciegos, abrirá nuevas vías para la investigación básica y una variedad de tratamientos, como enfermedades de la retina, del corazón y neurológicas.
“Estamos muy entusiasmados con la tecnología que descubrimos porque es algo que no se podía hacer antes”, dice Juan Carlos Izpisúa Belmonte, profesor del Laboratorio de Expresión Génica de Salk y autor principal del artículo publicado el 16 de noviembre de 2016 en Nature. “Por primera vez podemos entrar en células que no se dividen y modificar el ADN a voluntad. Las posibles aplicaciones de este descubrimiento son muy amplias”.
Hasta ahora, las técnicas que modifican el ADN, como el sistema CRISPR-Cas9, han sido más eficaces en la división de células, como las de la piel o el intestino, utilizando los mecanismos de copia normales de las células. La nueva tecnología Salk es diez veces más eficiente que otros métodos para incorporar nuevo ADN en cultivos de células en división, lo que la convierte en una herramienta prometedora tanto para la investigación como para la medicina. Pero, lo que es más importante, la técnica de Salk representa la primera vez que los científicos logran insertar un nuevo gen en una ubicación precisa del ADN en células adultas que ya no se dividen, como las del ojo, el cerebro, el páncreas o el corazón, ofreciendo nuevas posibilidades para aplicaciones terapéuticas en estas células.
Para lograr esto, los investigadores de Salk se enfocaron en una vía celular de reparación de ADN llamada NHEJ (por "unión de extremos no homólogos"), que repara las roturas rutinarias de ADN al volver a unir los extremos de las hebras originales. Combinaron este proceso con la tecnología de edición de genes existente para colocar con éxito el nuevo ADN en una ubicación precisa en células que no se dividen.
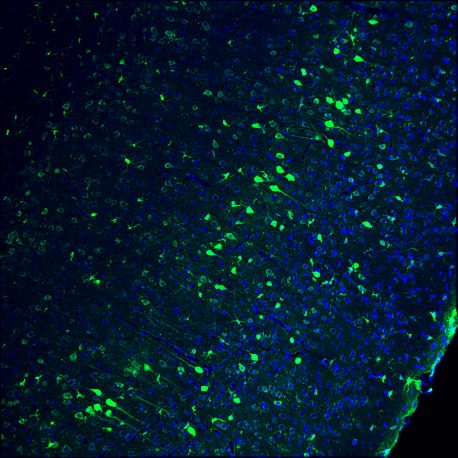
Haga clic aquí para una imagen de alta resolución
Crédito: Instituto Salk
"Usar esta vía NHEJ para insertar ADN completamente nuevo es revolucionario para editar el genoma en organismos adultos vivos", dice Keiichiro Suzuki, investigador asociado senior en el laboratorio Izpisua Belmonte y uno de los autores principales del artículo. “Nadie ha hecho esto antes”.
Primero, el equipo de Salk trabajó en la optimización de la maquinaria NHEJ para su uso con el sistema CRISPR-Cas9, que permite insertar ADN en ubicaciones muy precisas dentro del genoma. El equipo creó un paquete de inserción personalizado compuesto por un cóctel de ácidos nucleicos, al que llamaron HITI, o integración dirigida independiente de la homología. Luego usaron un virus inerte para entregar el paquete de instrucciones genéticas de HITI a las neuronas derivadas de células madre embrionarias humanas.
"Ese fue el primer indicio de que HITI podría funcionar en células que no se dividen", dice Jun Wu, científico del personal y coautor principal. Con esa hazaña en su haber, el equipo entregó con éxito la construcción a los cerebros de ratones adultos. Finalmente, para explorar la posibilidad de usar HITI para la terapia de reemplazo de genes, el equipo probó la técnica en un modelo de rata para la retinitis pigmentosa, una condición de degeneración retiniana hereditaria que causa ceguera en humanos. Esta vez, el equipo usó HITI para entregar a los ojos de ratas de 3 semanas de edad una copia funcional de Mertk, uno de los genes dañados en la retinosis pigmentaria. El análisis realizado cuando las ratas tenían 8 semanas de edad mostró que los animales podían responder a la luz y pasaron varias pruebas que indicaban curación en las células de la retina.
"Pudimos mejorar la visión de estas ratas ciegas", dice la coautora principal Reyna Hernandez-Benitez, investigadora asociada de Salk. "Este éxito temprano sugiere que esta tecnología es muy prometedora".
Los próximos pasos del equipo serán mejorar la eficiencia de entrega de la construcción HITI. Al igual que con todas las tecnologías de edición del genoma, obtener suficientes células para incorporar el nuevo ADN es un desafío. La belleza de la tecnología HITI es que es adaptable a cualquier sistema de ingeniería genómica objetivo, no solo a CRISPR-Cas9. Por lo tanto, a medida que mejoren la seguridad y la eficiencia de estos sistemas, también lo hará la utilidad de HITI.

Haga clic aquí para una imagen de alta resolución.
Crédito: Instituto Salk
“Ahora tenemos una tecnología que nos permite modificar el ADN de células que no se dividen, para reparar genes rotos en el cerebro, el corazón y el hígado”, dice Izpisua Belmonte. “Nos permite por primera vez poder soñar con curar enfermedades que antes no podíamos, lo cual es emocionante”.
Otros investigadores del estudio fueron Euiseok J. Kim, Fumiyuki Hatanaka, Mako Yamamoto, Toshikazu Araoka, Masakazu Kurita, Tomoaki Hishida, Mo Li, Emi Aizawa, April Goebl, Rupa Devi Soligalla, Concepcion Rodriguez Esteban, Travis Berggren y Edward M. Callaway. del Instituto Salk; Yuji Tsunekawa y Fumio Matsuzaki de Centro RIKEN de Biología del Desarrollo; Pierre Magistretti de Universidad Rey Abdullah de Ciencia y Tecnología; Jie Zhu, Tingshuai Jiang, Xin Fu, Maryam Jafari y Kang Zhang de Instituto de ojos Shiley y Instituto de Medicina Genómica, Universidad de California en San Diego; Zhe Li, Shicheng Guo, Song Chen y Kun Zhang de Instituto de Ingeniería en Medicina, Universidad de California San Diego; Jing Qu y Guang-Hui Liu de Academia China de Ciencias; Jerónimo Lajara, Estrella Nuñez y Pedro Guillén de Universidad Católica San Antonio de Murcia; y Josep M. Campistol de la Universidad de Barcelona.
El trabajo y los investigadores involucrados fueron apoyados en parte por el Los Institutos Nacionales de Salud, La Fundación Benéfica Leona M. y Harry B. Helmsley, Fundación benéfica G. Harold y Leila Y. Mathers, La Fundación McKnight, La Fundación Moxie, Fundación Dr. Pedro Guillén y Universidad Católica San Antonio de Murcia, España.
REVISTA
Nature
AUTORES
Keiichiro Suzuki, Yuji Tsunekawa, Reyna Hernandez-Benitez, Jun Wu, Jie Zhu, Euiseok J. Kim, Fumiyuki Hatanaka, Mako Yamamoto, Toshikazu Araoka, Zhe Li, Masakazu Kurita, Tomoaki Hishida, Mo Li, Emi Aizawa, Shicheng Guo, Song Chen, April Goebl, Rupa Devi Soligalla, Jing Qu, Tingshuai Jiang, Xin Fu, Maryam Jafari, Concepción Rodríguez Esteban, Travis Berggren, Jeronimo Lajara, Estrella Nuñez, Pedro Guillén, Josep M. Campistol, Fumio Matsuzaki, Guang-Hui Liu, Pierre Magistretti, Kun Zhang, Edward M. Callaway, Kang Zhang y Juan Carlos Izpisua Belmonte
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
El Instituto Salk es un instituto de investigación independiente y sin fines de lucro fundado en 1960 por Jonas Salk, creador de la primera vacuna segura y eficaz contra la polio. Su misión es impulsar una investigación fundamental, colaborativa y arriesgada que aborde los desafíos más urgentes de la sociedad, como el cáncer, el Alzheimer y la vulnerabilidad agrícola. Esta ciencia fundamental sustenta todos los esfuerzos translacionales, generando conocimientos que facilitan el desarrollo de nuevos medicamentos e innovaciones en todo el mundo.