
7 de diciembre de 2011
Nueva técnica de edición de genes curaría a los pacientes con sus propias células
Nueva técnica de edición de genes curaría a los pacientes con sus propias células
LA JOLLA, CA—Los investigadores del Instituto Salk de Estudios Biológicos han desarrollado una forma de usar las propias células de los pacientes para curar potencialmente la enfermedad de células falciformes y muchos otros trastornos causados por mutaciones en un gen que ayuda a producir hemoglobina en la sangre.
La técnica utiliza células de la piel de un paciente para generar células madre pluripotentes inducidas (iPSC), que son capaces de convertirse en varios tipos de tejidos maduros, incluida la sangre. Los científicos dicen que su método, que repara el gen de la globina beta (HBB), evita las técnicas de terapia génica que pueden introducir genes potencialmente dañinos en las células.
La nueva técnica, que pronto se probará como terapia en animales, también parece ser mucho más eficiente que otros métodos probados hasta la fecha, dicen los investigadores.
"Nuestros hallazgos sientan las bases para el desarrollo de terapias basadas en iPSC para trastornos genéticos devastadores como la enfermedad de células falciformes", dice el investigador principal del estudio, Juan Carlos Izpisúa Belmonte, profesor de Salk en el Laboratorio de Expresión Génica.
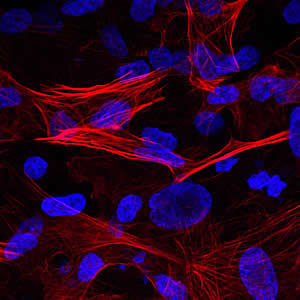
Los investigadores de Salk reprogramaron células de la piel extraídas de un paciente con enfermedad de células falciformes en células madre pluripotentes inducidas (iPSC), células inmaduras capaces de convertirse en cualquier tipo de tejido corporal.
Para asegurarse de que las células de la piel se reprogramaran de hecho en células madre, los investigadores las persuadieron para que se convirtieran en células musculares, como lo indica la presencia de proteínas específicas del músculo (en rojo) en esta imagen. Los núcleos celulares, los compartimentos centrales que contienen el ADN, se ven en azul.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
La enfermedad de células falciformes es un grupo de trastornos sanguíneos hereditarios causados por mutaciones genéticas en el gen HBB, lo que da como resultado una hemoglobina anormal, la proteína que contiene hierro y que normalmente permite que las células sanguíneas transporten oxígeno. Esto hace que los glóbulos rojos se vuelvan duros y pegajosos y se parezcan a una herramienta agrícola curva llamada "hoz". En los dos principales trastornos causados por mutaciones HBB, la anemia de células falciformes y la beta talasemia, los glóbulos rojos no pueden transportar oxígeno de manera efectiva.
Los síntomas de la enfermedad de células falciformes incluyen hinchazón de las manos y los pies, dolor debido a la obstrucción de los vasos sanguíneos, anemia y accidente cerebrovascular.
Los trastornos son más comunes entre las personas de ascendencia africana, mediterránea y del Medio Oriente. Uno de cada 500 afroamericanos y uno de cada 30,000 hispanoamericanos nacen con anemia drepanocítica, según los Centros para el Control y la Prevención de Enfermedades.
La enfermedad se puede curar con trasplantes de células madre o de médula ósea, pero existe un alto riesgo de que los receptores de trasplantes rechacen la médula o las células donadas, lo que puede provocar efectos secundarios graves e incluso la muerte.
Los investigadores de Salk, que incluyen a los coautores Mo Li y Keiichiro Suzuki, ambos investigadores asociados en el laboratorio de Belmonte, se propusieron diseñar un método seguro para usar iPSC para corregir el gen HBB en pacientes que tienen copias defectuosas del gen.
Debido a que las iPSC provienen del propio cuerpo del paciente, deberían conllevar menos riesgo de rechazo del trasplante. Además, se han identificado alrededor de otras 500 mutaciones causantes de enfermedades en el gen HBB, por lo que corregir el gen podría potencialmente curar una multitud de enfermedades relacionadas con HBB en todo el mundo.
Sin embargo, las técnicas tradicionales de generación de iPSC y terapia génica han demostrado ser potencialmente inseguras, según los investigadores.
Muchos han usado virus para convertir células adultas en células madre y para llevar un gen HBB normal para infectar y reparar células madre hematopoyéticas, células madre que dan lugar a todas las células sanguíneas.
Pero cuando estas células madre reparadas se devuelven a los pacientes, pueden incluir transgenes, genes no deseados que se han insertado en el genoma del huésped y alteran la función normal del ADN. La técnica también es ineficiente, ya que corrige solo un pequeño porcentaje de mutaciones genéticas, y el éxito del trasplante ha demostrado ser raro en los ensayos clínicos que prueban la terapia génica para tratar la beta talasemia.
“Queríamos arreglar la mutación de tal manera que no dejara rastros no deseados en el genoma de un paciente”, dice Suzuki.
Para hacer eso, los investigadores utilizaron un enfoque de dos pasos. Primero, tomaron células adultas de la piel de un paciente con una mutación HBB que causa la enfermedad de células falciformes. Usaron seis genes para persuadir a estas células a volver a iPSC, que luego podrían convertirse en células sanguíneas. Los genes se introdujeron en las células utilizando una técnica que evita el uso de virus y la inserción de transgenes en el genoma de las células.
Su siguiente paso fue reparar la mutación del gen HBB en las células madre. Para intercambiar el gen defectuoso con una copia normal en las iPSC, los investigadores utilizaron un adenovirus modificado (virus del resfriado común) que, a diferencia de los virus utilizados en otros métodos, no se replica en el cuerpo y no altera el ADN de las células huésped. Los genes virales fueron eliminados y reemplazados con una secuencia de ADN que contenía un gen HBB normal.
Luego, el virus modificado entregó el nuevo material genético dentro de las iPSC, donde la región de ADN que contenía el gen roto se reemplazó con la secuencia que contenía el gen normal. “Ocurre naturalmente, funciona como una cremallera”, dice Li. “El gen bueno simplemente encaja perfectamente, expulsando al malo”.
Al reemplazar una región relativamente grande de ADN, la técnica permite a los científicos corregir muchas mutaciones genéticas a la vez, lo que sugiere que el método podría proporcionar una forma de tratar cientos de tipos de enfermedades relacionadas con HBB. La corrección del gen HBB mutante también fue muy eficiente y el equipo de investigación realizó múltiples pruebas para garantizar que no se integraran genes errantes en el genoma.
Los científicos de Salk ahora planean producir células sanguíneas a partir de las células madre reparadas y probar su eficacia en animales. Si tiene éxito, esto puede conducir a terapias para humanos en las que las células madre de un paciente se reviertan en iPSC, luego se reparen genéticamente y se vuelvan a trasplantar a la médula ósea del mismo paciente. Si tiene éxito, la médula ósea producirá todas las células sanguíneas nuevas, incluida la hemoglobina normal.
Si la técnica resulta efectiva, dicen los investigadores, podría usarse para tratar otros tipos de enfermedades causadas por mutaciones de un solo gen.
El estudio fue financiado por subvenciones de G. Harold and Leila Y. Mathers Charitable Foundations, Sanofi-Aventis, Fundación Médica Ellison, La Fundación Benéfica Leona M. y Harry B. Helmsley, MICINN y Fundación Cellex (JCIB). El estudio aparece en la edición de diciembre de 2011 de Investigación celular.
Sobre el Instituto Salk de Estudios Biológicos:
El Instituto Salk de Estudios Biológicos es una de las instituciones de investigación básica más importantes del mundo, donde profesores de renombre internacional investigan cuestiones fundamentales de las ciencias de la vida en un entorno único, colaborativo y creativo. Centrados tanto en el descubrimiento como en la orientación de futuras generaciones de investigadores, los científicos de Salk realizan contribuciones innovadoras a nuestra comprensión del cáncer, el envejecimiento, el Alzheimer, la diabetes y las enfermedades infecciosas mediante el estudio de la neurociencia, la genética, la biología celular y vegetal y disciplinas relacionadas.
Los logros de la facultad han sido reconocidos con numerosos honores, incluidos premios Nobel y membresías en la Academia Nacional de Ciencias. Fundado en 1960 por el pionero de la vacuna contra la polio Jonas Salk, MD, el Instituto es una organización independiente sin fines de lucro y un hito arquitectónico.
Para más información:
Investigación celular
Autores: Mo Li, Keiichiro Suzuki, Jing Qu, Preeti Saini, Ilir Dubova, Fei Yi, Jungmin Lee, Ignacio Sancho-Martinez, Guang-Hui Liu y Juan Carlos Izpisua Belmonte
Corrección eficiente de mutaciones causantes de hemoglobinopatía mediante recombinación homóloga en iPSC de pacientes sin integración
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu