
17 de noviembre.
Los hallazgos pueden conducir a terapias muy necesarias para la enfermedad renal
Los hallazgos pueden conducir a terapias muy necesarias para la enfermedad renal
LA JOLLA, CA—Las enfermedades que afectan los riñones representan un problema de salud importante y sin resolver en todo el mundo. Los riñones rara vez recuperan su función una vez que están dañados por una enfermedad, lo que destaca la necesidad urgente de un mejor conocimiento del desarrollo y la fisiología renal.
Ahora, un equipo de investigadores dirigido por científicos del Instituto Salk de Estudios Biológicos ha desarrollado una plataforma novedosa para estudiar enfermedades renales, abriendo nuevas vías para la aplicación futura de estrategias de medicina regenerativa para ayudar a restaurar la función renal.
Por primera vez, los investigadores de Salk han generado estructuras renales tridimensionales a partir de células madre humanas, abriendo nuevas vías para estudiar el desarrollo y las enfermedades de los riñones y para el descubrimiento de nuevos fármacos dirigidos a las células renales humanas. Los hallazgos fueron informados el 17 de noviembre de 2013 en Nature Cell Biology.
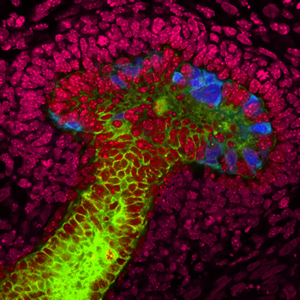
Por primera vez, los científicos de Salk han cultivado células madre humanas en brotes ureterales en etapa temprana, estructuras renales responsables de reabsorber agua después de que se hayan filtrado las toxinas. En el laboratorio, utilizaron células de riñón embrionario de ratón (que se ven aquí en rojo) para persuadir a las células madre humanas para que crecieran y se convirtieran en brotes nacientes en forma de hongo (azul y verde). Su descubrimiento es un paso importante en el desarrollo de técnicas regenerativas para el cultivo de riñones humanos de reemplazo.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
Los científicos habían creado precursores de células renales usando células madre tan recientemente como el verano pasado, pero el equipo de Salk fue el primero en persuadir a las células madre humanas para que formaran estructuras celulares tridimensionales similares a las que se encuentran en nuestros riñones.
"Los intentos de diferenciar las células madre humanas en células renales han tenido un éxito limitado", dice el autor principal del estudio. Juan Carlos Izpisúa Belmonte, profesor en Salk's Laboratorio de Expresión Génica y titular de la Cátedra Roger Guillemin. “Hemos desarrollado un método simple y eficiente que permite la diferenciación de células madre humanas en estructuras 3D bien organizadas de la yema ureteral (UB), que luego se desarrolla en el sistema de conductos colectores”.
Los hallazgos de Salk demuestran por primera vez que las células madre pluripotentes (PSC, por sus siglas en inglés), células capaces de diferenciarse en los muchos tipos de células y tejidos que componen el cuerpo, pueden convertirse en células similares a las que se encuentran en la yema ureteral, una primera estructura de desarrollo de los riñones, y luego diferenciarse aún más en estructuras tridimensionales en cultivos de órganos. Las células UB forman las primeras etapas de los órganos reproductivos y urinarios humanos durante el desarrollo y luego se convierten en un conducto para el drenaje de orina desde los riñones. Los científicos lograron esto con células madre embrionarias humanas y células madre pluripotentes inducidas (iPSC), células humanas de la piel que han sido reprogramadas a su estado pluripotente.
Después de generar iPSC que demostraron propiedades pluripotentes y pudieron diferenciarse en mesodermo, una capa de células germinales a partir de la cual se desarrollan los riñones, los investigadores utilizaron factores de crecimiento que se sabe que son esenciales durante el desarrollo natural de nuestros riñones para el cultivo de iPSC y células madre embrionarias. La combinación de señales de estos factores de crecimiento, moléculas que guían la diferenciación de las células madre en tejidos específicos, fue suficiente para comprometer las células hacia progenitores que muestran características claras de las células renales en solo cuatro días.
Luego, los investigadores guiaron estas células para que se diferenciaran aún más en estructuras de órganos similares a las que se encuentran en la yema ureteral cultivándolas con células renales de ratones. Esto demostró que las células de ratón podían proporcionar las señales de desarrollo adecuadas para permitir que las células madre humanas formaran estructuras tridimensionales del riñón.

Desde la izquierda: los investigadores de Salk Ilir Dubova, Ignacio Sancho Martinez, Yun Xia, Juan Carlos Izpisua Belmonte y Emmanuel Nivet
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
Además, el equipo de Izpisua Belmonte probó su protocolo en iPSC de un paciente diagnosticado clínicamente con enfermedad renal poliquística (PKD), un trastorno genético caracterizado por múltiples quistes llenos de líquido que pueden provocar una disminución de la función renal e insuficiencia renal. Descubrieron que su metodología podría producir estructuras renales a partir de iPSC derivadas de pacientes.
Debido a las numerosas manifestaciones clínicas de la enfermedad, ni las terapias basadas en genes ni las basadas en anticuerpos son enfoques realistas para tratar la poliquistosis renal. La técnica del equipo de Salk podría ayudar a sortear este obstáculo y brindar una plataforma confiable para las compañías farmacéuticas y otros investigadores que estudian terapias basadas en medicamentos para la PKD y otras enfermedades renales.
“Nuestras estrategias de diferenciación representan la piedra angular de los estudios de modelado de enfermedades y descubrimiento de fármacos”, dice el autor principal del estudio, Ignacio Sancho-Martínez, investigador asociado en el laboratorio de Izpisua Belmonte. “Nuestras observaciones ayudarán a guiar futuros estudios sobre las implicaciones celulares precisas que la PKD podría tener en el contexto del desarrollo renal. ”
Otros investigadores del estudio fueron Yun Xia, Emmanuel Nivet, Thomas Gallegos, Keiichiro Suzuki, Daiji Okamura, Min-Zu Wu, Ilir Dubova y Concepion Rodriguez Esteban, del Instituto Salk; Nuria Montserrat del Centro de Medicina Regenerativa de Barcelona, España; y Josep Maria Campistol del Hospital Clinic de Barcelona.
El trabajo fue apoyado por el Instituto de California para la medicina regenerativa, la Fundación Nomis, la Fundación Cellex, la Fundación benéfica G. Harold y Leila Y. Mathers, el Leona M. y Harry B. Helmsley Charitable Trust, Fundació La Marató de TV3, CIBER BBN e ISCIII-TERCEL-MINECO.
Sobre el Instituto Salk de Estudios Biológicos:
El Instituto Salk de Estudios Biológicos es una de las instituciones de investigación básica más importantes del mundo, donde profesores de renombre internacional investigan cuestiones fundamentales de las ciencias de la vida en un entorno único, colaborativo y creativo. Centrados tanto en el descubrimiento como en la orientación de futuras generaciones de investigadores, los científicos de Salk realizan contribuciones innovadoras a nuestra comprensión del cáncer, el envejecimiento, el Alzheimer, la diabetes y las enfermedades infecciosas mediante el estudio de la neurociencia, la genética, la biología celular y vegetal y disciplinas relacionadas.
Los logros de la facultad han sido reconocidos con numerosos honores, incluidos premios Nobel y membresías en la Academia Nacional de Ciencias. Fundado en 1960 por el pionero de la vacuna contra la polio Jonas Salk, MD, el Instituto es una organización independiente sin fines de lucro y un hito arquitectónico.
PERIODICO
Nature Cell Biology
AUTORES
Yun Xia, Emmanuel Nivet, Ignacio Sancho-Martinez, Thomas Gallegos, Keiichiro Suzuki, Daiji Okamura, Min-Zu Wu, Ilir Dubova, Concepción Rodríguez Estban, Nuria Montserrat, Josep Maria Campistol y Juan Carlos Ispisua Belmonte
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu