
17 de Octubre de 2019
El modelo de embrión sintético de ratón Salk podría abrir nuevas vías para comprender el desarrollo temprano, entre muchas otras aplicaciones para la salud humana
El modelo de embrión sintético de Salk podría abrir nuevas vías para comprender el desarrollo temprano, entre muchas otras aplicaciones para la salud humana
LA JOLLA—Aunque graduarse de la escuela, un primer trabajo y el matrimonio pueden ser eventos importantes en la vida, algunos de los eventos más significativos suceden mucho antes: en los primeros días después de que un espermatozoide fertiliza un óvulo y la célula comienza a dividirse.
La forma en que las primeras 100 células (colectivamente denominadas blastocisto) se organizan tiene profundas implicaciones para determinar si un embarazo es exitoso, cómo se forman los órganos y potencialmente incluso para enfermedades posteriores en la vida, como el Alzheimer. Sin embargo, los científicos no han tenido una buena manera de modelar cómo se forma un blastocisto, hasta ahora.
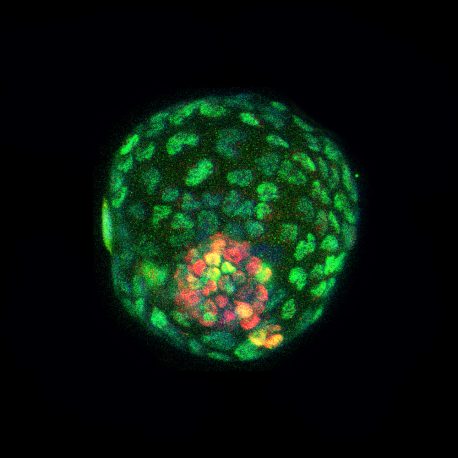
Haga clic aquí para una imagen de alta resolución.
Crédito: Salk Institute/Waitt Advanced Biophotonics Core Facility
Por primera vez, investigadores del Instituto Salk y el Centro Médico Southwestern de la Universidad de Texas han creado estructuras similares a blastocistos de ratón, o "blastoides", a partir de una sola célula cultivada, eludiendo la necesidad de embriones naturales. Como informaron el 17 de octubre de 2019, en la revista Celular, estos blastoides cultivados tienen la misma estructura que los blastocistos naturales e incluso pueden implantarse en el útero, y podrían ayudar a avanzar en la investigación sobre el desarrollo, así como informar sobre cuestiones relacionadas con el embarazo, la infertilidad o los problemas de salud más adelante en la vida de la descendencia.
“Estos estudios nos ayudarán a comprender mejor los comienzos mismos de la vida; qué tan temprano en la vida una sola célula puede dar lugar a millones de células y cómo se ensamblan en el espacio y el tiempo para dar lugar a un organismo completamente desarrollado. Es importante destacar que este trabajo evita el uso de embriones naturales y es escalable”, dice Juan Carlos Izpisúa Belmonte, profesor en el Laboratorio de Expresión Génica de Salk.
Los blastocistos naturales, que pueden convertirse en embriones una vez que se implantan en el útero, han resultado difíciles de estudiar. El problema es que los modelos animales, como los ratones, solo producen estas estructuras en pequeñas cantidades, y los científicos no pueden probar fácilmente los efectos de la desnutrición o la exposición a toxinas o una variedad de mutaciones genéticas en el desarrollo a un nivel suficiente para el estudio.
"Somos optimistas de que este trabajo permitirá una investigación importante sobre los defectos del desarrollo temprano", dice el profesor asistente Jun Wu de UT Southwestern, quien codirigió el estudio.
Los equipos de Salk y UT Southwestern desarrollaron los blastoides utilizando embriones y, lo que es más importante, células de ratón adultas. Las células adultas se colocaron en una solución química que las llevó a convertirse en células madre pluripotentes inducidas, o iPSC, que pueden convertirse en casi cualquier tipo de tejido del cuerpo.

Haga clic aquí para una imagen de alta resolución.
Crédito: Instituto Salk
Para alentar a las células iPS a formar blastoides, los investigadores las colocaron en pequeños grupos en un medio de cultivo especial donde pronto formaron conexiones entre sí. Esto era exactamente lo que los investigadores esperaban ver: las células comenzaban a formar estructuras similares a la etapa de desarrollo antes de que un óvulo fertilizado se convierta en un blastocisto.
Con el tiempo, las células conectadas comenzaron a formar una bola con una capa interna y otra externa. Las células que miran hacia adentro acumularon proteínas que las diferenciaron de las células externas. Las células que miran hacia afuera también comenzaron a activar una proteína llamada YAP, que ingresó al núcleo celular y comenzó el proceso de inducir la expresión de proteínas para construir lo que eventualmente podría convertirse en una placenta.
"La formación de blastoides imita el proceso de desarrollo natural", dice Ronghui Li, coautor del estudio y becario postdoctoral en el laboratorio Izpisua Belmonte.
Los blastoides contenían los mismos tres tipos de células primordiales (de las que proceden todas las células de un organismo adulto) que se encuentran en los blastocistos naturales. También tenían un tamaño similar al de los blastocistos naturales y mostraban una firma genética similar. Otros experimentos indicaron que los blastoides podrían desarrollarse aún más en estructuras que se asemejan a embriones tempranos posteriores a la implantación.
"Creo que este tipo de recurso será muy poderoso para estudiar el desarrollo temprano en los mamíferos", dice Cuiqing Zhong, coautor del estudio y becario postdoctoral en el laboratorio Izpisua Belmonte.
A continuación, el equipo planea utilizar herramientas de edición de genes para comprender cómo los cambios genéticos en los blastoides afectan a los tres tipos de células diferentes. Los blastoides también proporcionan un nuevo modelo para probar fármacos y productos químicos para futuras terapias.
Los blastoides aún no pueden convertirse en embriones funcionales; en cambio, las células se convierten en tejido desorganizado. Pero los científicos creen que los blastoides pueden revelar detalles sobre etapas posteriores del desarrollo embrionario.
“Con una mayor optimización, esta tecnología podría conducir a la generación de blastoides completamente funcionales capaces de desarrollarse hasta las etapas en las que se forman diferentes primordios de órganos y, por lo tanto, ser las semillas de organoides que podrían usarse como fuentes invaluables para el trasplante de órganos”, agrega Belmonte. .
“El destacado físico Richard Feynman dijo una vez: 'Lo que no puedo crear, no lo entiendo'. Cómo comienza la vida a partir de un óvulo fertilizado sigue siendo un misterio, y nuestro enfoque blastoide ayudará a los investigadores a obtener nuevos conocimientos sobre este proceso”. dice Wu.
Otros autores incluyeron a Yang Yu (co-primer autor) de Salk and Peking University Third Hospital; Haisong Liu, Lei Shi, Yuta Takahashi, Hsin-Kai Liao y Concepción Rodríguez Esteban de Salk; Zheying Min y Jie Qiao del Tercer Hospital de la Universidad de Pekín; Masahiro Sakurai y Leqian Yu de UT Southwestern; Yulei Wei de UT Southwestern y la Universidad de Wuyi; y Estrella Nuñez Delicado de la Universidad Católica San Antonio de Murcia.
Este trabajo fue financiado por Larry L. Hillblom Foundation, Paul F. Glenn Foundation, National Key R&D Program of China (2016YFC1000601), G. Harold and Leila Y. Mathers Charitable Foundation, Moxie Foundation, Leona M. y Harry B. Helmsley Charitable Trust (2012-PG-MED002), la Fundación Hewitt, los Institutos Nacionales de Salud (5 DP1 DK113616) y la Universidad Católica San Antonio de Murcia.
DOI: 10.1016 / j.cell.2019.09.029
PERIODICO
Celular
AUTORES
Ronghui Li, Cuiqing Zhong, Yang Yu, Haisong Liu, Masahiro Sakurai, Leqian Yu, Zheying Min, Lei Shi, Yulei Wei, Yuta Takahashi, Hsin-Kai Liao, Jie Qiao, Estrella Nuñez Delicado, Concepción Rodríguez Esteban, Jun Wu, Juan Carlos Izpisúa Belmonte
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
Descubrir los secretos de la vida misma es la fuerza impulsora detrás del Instituto Salk. Nuestro equipo de científicos galardonados de clase mundial traspasa los límites del conocimiento en áreas como neurociencia, investigación del cáncer, envejecimiento, inmunobiología, biología vegetal, biología computacional y más. Fundado por Jonas Salk, desarrollador de la primera vacuna contra la polio segura y eficaz, el Instituto es una organización de investigación independiente y sin fines de lucro y un hito arquitectónico: pequeño por elección, íntimo por naturaleza y valiente ante cualquier desafío.