
29. Oktober 2015
Salk-Team findet E. coli im Mikrobiom, das den Körper vor Infektionskrankheiten schützen kann, kann helfen, antibiotikaresistente Superkeime zu verhindern
Salk-Team findet E. coli im Mikrobiom, die den Körper vor Infektionskrankheiten schützen kann und möglicherweise zur Vorbeugung von antibiotikaresistenten Superbugs beiträgt
LA JOLLA – Angesichts wachsender Bedenken hinsichtlich tödlicher antibiotikaresistenter ‘Superbug’-Bakterienstämme bieten Wissenschaftler am Salk Institute eine mögliche Lösung für das Problem: ‘Superhelden’-Bakterien, die im Darm leben und sich in andere Körperteile bewegen, um lebensbedrohliche Nebenwirkungen von Infektionen zu lindern.
In einer am 30. Oktober 2015 veröffentlichten Arbeit in Wissenschaft, die Forscher des Salk-Instituts berichteten, einen Stamm von Mikroben gefunden zu haben Escherichia coli Bakterien in Mäusen, die die Toleranz der Tiere gegenüber Infektionen der Lunge und des Darms verbessern können, indem sie Auszehrung verhindern – ein häufiger und potenziell tödlicher Verlust von Muskelgewebe, der bei schweren Infektionen auftritt. Wenn ein ähnlich schützender Stamm beim Menschen gefunden wird, könnte dies einen neuen Weg zur Bekämpfung von Muskelschwund eröffnen, der Patienten mit Sepsis und nosokomialen Infektionen befällt, von denen viele inzwischen antibiotikaresistent sind.
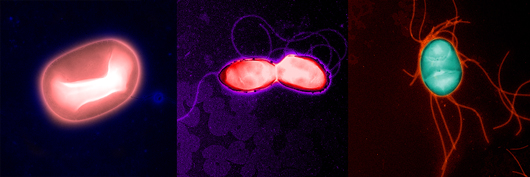
Salk-Wissenschaftler fanden einen Stamm von E. coli Bakterien (links), die Muskelschwund bei Mäusen stoppen konnten, die mit einem der beiden infiziert waren Salmonellen Typhimurium (rechts) und Burkholderia thailandensis (Mitte).
Klicken Sie hier für ein hochauflösendes Bild.
Bild: Mit freundlicher Genehmigung des Salk Institute for Biological Studies
“Behandlungen für Infektionen konzentrieren sich seit langem auf die Ausrottung des schädlichen Mikroorganismus, aber was die Menschen tatsächlich tötet, sind nicht die Bakterien selbst – es sind die Kollateralschäden, die sie dem Körper zufügen”, sagt Janelle Ayres, ein Salk-Assistenzprofessor in der Nomis Foundation Laboratorien für Immunbiologie und mikrobielle Pathogenese und leitender Forscher der Studie.
“Unsere Ergebnisse legen nahe, dass die Verhinderung von Schäden – in diesem Fall Muskelschwund – die lebensbedrohlichsten Aspekte einer Infektion abwehren kann”, fügt sie hinzu. “Und indem man nicht versucht, den Erreger zu töten, fördert man nicht die Evolution der tödlichen antibiotikaresistenten Stämme, die Menschen auf der ganzen Welt töten. Möglicherweise können wir Superkeime mit ‘Superheldenkäfern’ bekämpfen.”
Einst die mächtigsten und revolutionärsten Medikamente, scheinen Antibiotika an ihre Grenzen gestoßen zu sein, da Bakterien schnell Resistenzen gegen die Medikamente entwickeln können. Die Zunahme von Antibiotikaresistenzen stellt eine ernste Bedrohung für Menschen auf der ganzen Welt dar, da Krankheiten, die einst leicht kontrolliert werden konnten, allen Behandlungsversuchen widerstehen. Eine kürzlich durchgeführte Studie ergab, dass bis zur Hälfte der Bakterien, die Infektionen in US-Krankenhäusern nach einer Operation verursachen, gegen Standardantibiotika resistent sind.
Allein in den Vereinigten Staaten infizieren sich jährlich zwei Millionen Menschen mit Bakterien, die gegen Antibiotika resistent sind, und mindestens 23.000 Menschen sterben jedes Jahr an den direkten Folgen dieser Infektionen, so die U.S. Centers for Disease Control.

Michelle Lee, Alexandria Palaferri Schieber und Janelle Ayres
Klicken Sie hier für ein hochauflösendes Bild.
Bild: Mit freundlicher Genehmigung des Salk Institute for Biological Studies
“Antibiotika waren ein großer Schritt für die Medizin, aber das Modell, Bakterien mit Medikamenten abzutöten, hat eindeutig seine Schwächen”, sagt Alexandria Palaferri Schiebe, wissenschaftliche Mitarbeiterin in Ayres’ Labor und Co-Erstautorin der neuen Studie. “Die meisten Forscher sind auf der Suche nach neuen Antibiotika, aber das heizt das Wettrüsten zwischen Ärzten und Bakterien an. Die Konzentration auf Krankheitstoleranz - die Verhinderung von Schäden durch die Krankheit - statt auf die Ausrottung von Mikroben ist ein neues Paradigma für die Therapie von Infektionskrankheiten.”
In der Hoffnung, neue Methoden zur Bekämpfung von Infektionen zu finden, wandte sich Ayres’ Team dem Mikrobiom zu, der Gemeinschaft von Mikroben, die - in der Regel harmonisch - in unserem Körper leben. Im menschlichen Körper sind die Mikroben 10-mal zahlreicher als die Zellen und machen bis zu 3 Prozent des Körpergewichts aus. Trotzdem weiß man relativ wenig darüber, wie diese winzigen Passagiere mit unserer Entwicklung, unserem Stoffwechsel und unserem Immunsystem interagieren.
Ayers begann als Doktorand mit dem Studium der Krankheitsresistenz und stellte die Hypothese auf, dass das Darmmikrobiom Bakterien enthalten könnte, die vor Schäden durch Infektionen schützen. “Es gibt viele Beweise, die diese Idee stützen, aber bisher hatte niemand einen solchen Stamm identifiziert oder den Mechanismus gezeigt, durch den ein Bakterium Krankheitsresistenz bieten würde”, sagt Ayres.
Das Salk-Team identifizierte eine Population von Labormäusen, die resistent gegen Muskelschwund zu sein schienen. Durch den Vergleich der Zusammensetzung des Darmmikrobioms dieser Mäuse mit dem von Mäusen, denen diese Resistenz fehlte, identifizierte das Team einen Stamm von E. coli das nur bei den wasting-resistenten Mäusen vorhanden war. Wurde normalen Mäusen eine orale Behandlung mit diesem nützlichen E. coli Stamm haben sie die Fähigkeit erlangt, ihre Muskel- und Fettmasse während einer Darminfektion mit dem Bakterium Salmonellen Typhimurium und durch das Bakterium verursachte Lungenentzündung Burkholderia thailandensis.
Der nächste Schritt war herauszufinden, wie die Bakterien diese Toleranz den Mäusen verliehen. In Zusammenarbeit mit dem Labor von Salk Professor Ronald Evans, Das Team von Ayres entdeckte, dass bei einer Infektion mit den pathologischen Bakterien die E. coli verließ den Darm und wanderte in das Fettgewebe, um Schutzreaktionen auszulösen, die die Muskeln ernähren.
Normalerweise verzeichnen Mäuse mit Lungen- und Darminfektionen einen Rückgang eines Hormons namens Insulin-like Growth Factor 1 (IGF-1), einem Molekül, das dem Körper signalisiert, Muskelmasse zu erhalten. Aber der Schutz E. coli aktivierte den IGF-1-Signalweg im Fettgewebe, wodurch normale IGF-1-Spiegel aufrechterhalten werden konnten und die Muskulatur des Tieres trotz der pathogenen Infektionen erhalten blieb.
Das Salk-Team fand außerdem heraus, dass die E. coli belastete den IGF-1-Muskelerhaltungs-Signalweg durch ein Zwischenprodukt, einen molekularen Komplex in Zellen, der als Inflammasom bekannt ist. Als Teil des angeborenen Immunsystems des Körpers reagiert das Inflammasom auf eine Infektion, indem es eine Entzündung in dem infizierten Bereich auslöst, um die schädlichen Mikroben zu zerstören. Das E. coli nutzten dasselbe Alarmsystem, um dem Körper mitzuteilen, dass er den IGF-1-Spiegel und damit die Muskelmasse aufrechterhalten soll.
Ob ein solcher mikrobieller ‘Superheld’ dem Menschen bei Infektionen zu Hilfe kommen könnte, bleibt abzuwarten. Ayres’ Team untersucht derzeit, wie lange die E. coli Dass der Stamm die Krankheitserreger in Schach halten kann und ob das Immunsystem des Körpers die schädlichen Bakterien schließlich vollständig ausrotten wird. Sie beginnen auch zu untersuchen, ob ein solcher Mikroorganismus beim Menschen vorkommt.
“Es gibt noch viel, das wir verstehen müssen, aber dies ist ein sehr vielversprechendes Zeichen dafür, dass Mikroben als Medizin eingesetzt werden könnten”, sagt Ayres. “Es könnte einen völlig neuen Behandlungsansatz für Infektionen bieten, selbst für solche, die resistent gegen Antibiotika sind, und gleichzeitig die Entstehung neuer resistenter Stämme verhindern.”
Die Forschung wurde unterstützt durch die Nationale Gesundheitsinstitute, die NOMIS-Stiftung, die Searle-Stipendiaten-Stiftung, der Ray Thomas Edward Stiftung, der Die gemeinnützige Stiftung von Leona M. und Harry B. Helmsley, der Samuel Waxman Krebsforschungsstiftung, Ipsen Bioscience und die Howard Hughes Medical Institute.
Weitere Mitwirkende an der Forschung waren Max Chang, Mathias Leblanc, Brett Collins und Michael Downes, alle vom Salk Institute.
JOURNAL
Wissenschaft
AUTOREN
Alexandria M. Palaferri Schieber, Yujung Michelle Lee, Max W. Chang, Mathias Leblanc, Brett Collins, Michael Downes, Ronald M. Evans, Janelle S. Ayres
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Die Aufgabe des Instituts besteht darin, grundlegende, kooperative und risikofreudige Forschung voranzutreiben, die sich mit den dringendsten Herausforderungen der Gesellschaft befasst, darunter Krebs, Alzheimer und die Gefährdung der Landwirtschaft. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und führt zu Erkenntnissen, die neue Medikamente und Innovationen weltweit ermöglichen.