
7. September 2011
Forscher entdecken, dass ein Gen kritischen Bereich des Genoms stillhält
Forscher entdecken, dass ein Gen kritischen Bereich des Genoms stillhält
LA JOLLA, CA—Mehr als 230.000 Frauen in den Vereinigten Staaten werden in diesem Jahr mit Brustkrebs diagnostiziert, von denen fast 10% Mutationen in den Genen BRCA1 oder 2 aufweisen werden. Es ist bekannt, dass das BRCA1-Gen und sein Protein eine wichtige Rolle bei der Verhinderung der Entstehung von Brust- und Eierstockkrebs spielen, aber wie genau sie dies tun, war lange Zeit ein umstrittenes, ja sogar kontroverses Thema. Nun wurde in der Ausgabe vom 8. September des Natur, Forscher des Salk Institute haben möglicherweise eine Antwort gefunden – und diese deutet darauf hin, dass die bisherigen unterschiedlichen vorherrschenden Theorien allesamt ein wenig richtig lagen.
Wenn BRCA1 fehlt, werden Gene, die normalerweise stummgeschaltet sind, jetzt aktiviert, “und sie können viele der Dinge tun, die Wissenschaftler mutiertem BRCA1 zuschreiben, was das Krebsrisiko erhöht”, sagt Salk-Forschungsmitarbeiter Gerald Pao, Ph.D., einer der Hauptautoren der Studie. “Zellen können ihre DNA nicht effizient reparieren, und es gibt Probleme mit der Genexpression und Transkription, fehlerhafter Zellteilung und chromsomalen Instabilität, unter anderem.”
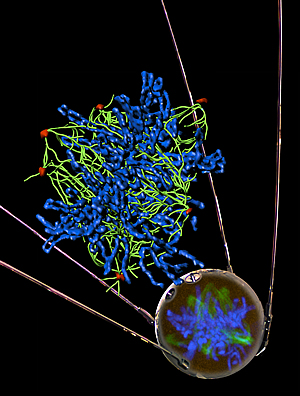
Defekte BRCA1 verursachen eine abweichende Expression von nicht-kodierender Satelliten-RNA, die zu genomischer Instabilität führt und dadurch die Krebsentstehung fördert. Das Bild zeigt, dass eine Überproduktion von Satelliten-RNA zu einer abnormalen Anzahl von Zentrosomen in einer normalen menschlichen Epithelzelle führt.
Zentrosomen sind in Rot, Tubulin in Grün und Chromosomen in Blau abgebildet. Das “gespiegelte” Bild im Sputnik-Satelliten ist ein konfokales Mikroskopiebild.
Zentrum: eine mathematische Rekonstruktion des konfokalen Bildes zur Auflösung der Tubulinfasern und der einzelnen Chromosomen.
Bild: Mit freundlicher Genehmigung von Dr. Quan Zhu (konfokales Bild); Jamie Simon (Zusammenstellung), Salk Institute for Biological Studies; Dr. James Fitzpatrick (rekonstruiertes Bild) Waitt Advanced Biophotonics Center.
Die Wissenschaftler entdeckten, dass BRCA1 die regulatorische Kontrolle über eine große Anzahl von Genen ausübt, indem es diese DNA dicht zu einer Struktur namens Heterochromatin im Zellkern gebündelt hält, sodass sie unzugänglich und transkriptionell völlig still ist. Innerhalb dieser Struktur befinden sich sogenannte Satelliten-DNA-Wiederholungen, ein Teil des Genoms, der lange Zeit weitgehend ignoriert und sogar als “Müll” betrachtet wurde.”
“Aus unseren Erkenntnissen leiten wir ab, dass die Rolle von BRCA1 bei der Aufrechterhaltung der globalen Heterochromatin-Integrität viele seiner tumorunterdrückenden Funktionen erklärt, und wenn dieses entscheidende Protein fehlt, kann Krebs entstehen”, sagt Pao.
“Vor einigen Jahren hatte unser Labor gezeigt, dass das BRCA1-Protein eine enzymatische Aktivität besitzt, die H2A, ein allgemeines DNA-verpackendes Protein, modifizieren kann. Diese Aktivität ist ein Hotspot für Mutationen bei menschlichen Brustkrebspatientinnen”, sagt Inder Verma, “In Abwesenheit eines funktionellen BRCA1-Proteins wird H2A nicht modifiziert und kann daher nicht an die heterochromatische DNA binden, und die Transkription von RNAs aus den Satelliten-DNAs setzt ein.
“Unsere Ergebnisse könnten Ärzten eine Möglichkeit geben, Krebs früher als bisher möglich zu erkennen”, sagt er. “Es könnte machbar sein, die Expression von Satelliten-RNA im Blut von Patienten als frühen Krebsmarker nachzuweisen.”
Die Entdeckung gelang, nachdem die Forscher eine Maus erzeugten, bei der das BRCA1 im Gehirn fehlte, und feststellten, dass ihre Neuronen einen Defekt bei der Verpackung der DNA aufwiesen. Die DNA-Fäden, die jedes Chromosom bilden, müssen stark zu Paketen kondensiert werden, um in den Zellkern zu passen. Dazu wickelt sich die DNA um spulenförmige Proteine, sogenannte Histone, und diese Histone werden weiter zu Chromatin verdichtet. “Jedes Chromosom ist in Chromatin verpackt, und innerhalb dieses Chromatins gibt es Heterochromatin, das noch weiter kondensiert ist, um sicherzustellen, dass die darin enthaltenen Gene wirklich still sind”, sagt Pao. Die Forscher entdeckten bei ihren Versuchsmäusen, dass das Heterochromatin defekt und lockerer war, als es hätte sein sollen.
Laut Quan Zhu, Ph.D., Co-Autorin der Arbeit, befindet sich diese Struktur in der Mitte der “X”-förmigen Gestalt, die entsteht, wenn ein Chromosom kurz vor der Zellteilung repliziert wird. Dieser Bereich, bekannt als Zentromer, enthält eine Region, in der Satelliten-DNA-Abschnitte vielfach wiederholt werden, damit die Zelle das Zentrum des duplizierten Chromosoms erkennen kann. Dieser Bereich wird benötigt, um die Chromosomen auseinanderzuziehen, sagt sie.
Interessanterweise stellten die Salk-Forscher fest, dass die De-Repression von Satelliten sowohl bei Brustkrebs in Mäusen als auch in Menschen mit BRCA1-Mangel beobachtet wurde und dass die Wiederherstellung von BRCA1 die Expression der Satellitengene um etwa das 20-fache unterdrückte. Die de-reprimierten Satelliten-RNAs verursachten Chromosomenschäden, indem sie diese unangemessen verschmolzen und brachen, was als genomische Instabilität bezeichnet wird – ein katastrophales Ereignis für die Zelle während der Zellteilung, das zu Krebs führen kann.
“Die Frage, was BRCA1 tut, war von Kontroversen geprägt, weil es immer wieder überall gefunden wurde und kein einheitliches Bild davon gab, was es tat”, sagt Verma. “Wir hoffen, dass diese Studie nun eine neue, kohäsive Richtung für die BRCA1-Forschung vorgibt, damit wir die grundlegenden Fragen beantworten können, wie dieses Gen Krebs fördert und wie wir möglicherweise eine frühere Diagnose verbessern und Krebs, der durch BRCA1 verursacht wird, effektiver behandeln können.”
Zu den Studienmitautoren gehören Alexis Huynh MD, Hoonkyo Suh Ph.D., Nina Tonnu BS und Fred Gage PhD vom Salk Institute sowie Petra Nederlof, M.D., vom Netherlands Cancer Institute.
Diese Arbeit wurde teilweise unterstützt durch ein NIH-Stipendium R37AI048034 des National Institute of Allergy and Infectious Diseases, die Leducq Foundation, die Merieux Foundation, Ipsen/Biomeasure, Sanofi Aventis und die H.N. and Frances C. Berger Foundation.
Über die National Institutes of Health (NIH):
Die Nationale Medizinische Forschungsagentur umfasst 27 Institute und Zentren und ist Teil des US-Gesundheitsministeriums. Sie ist die wichtigste Bundesbehörde zur Durchführung und Unterstützung medizinischer Grundlagenforschung, klinischer Forschung und translationaler Forschung und untersucht Ursachen, Behandlungen und Heilungen für häufige und seltene Krankheiten. Weitere Informationen über das NIH und seine Programme finden Sie unter www.nih.gov.
Über das Salk Institute for Biological Studies:
Das Salk Institute for Biological Studies ist eine der weltweit führenden Institutionen für Grundlagenforschung, an der international renommierte Fakultätsmitglieder grundlegende Fragen der Biowissenschaften in einem einzigartigen, kollaborativen und kreativen Umfeld untersuchen. Mit dem Fokus auf Entdeckungen und die Ausbildung zukünftiger Forschergenerationen leisten Salk-Wissenschaftler bahnbrechende Beiträge zu unserem Verständnis von Krebs, Alterung, Alzheimer, Diabetes und Infektionskrankheiten durch die Untersuchung von Neurowissenschaften, Genetik, Zell- und Pflanzenbiologie sowie verwandten Disziplinen.
Die Leistungen der Fakultät wurden mit zahlreichen Auszeichnungen gewürdigt, darunter Nobelpreise und Mitgliedschaften in der National Academy of Sciences. Das 1960 vom Polio-Impfstoff-Pionier Dr. Jonas Salk gegründete Institut ist eine unabhängige gemeinnützige Organisation und ein architektonisches Wahrzeichen.
Für weitere Informationen:
Natur
Band 477, Ausgabe 7363 (08. September 2011)
Autoren: Quan Zhu, Gerald M. Pao1, Alexis M. Huynh, Hoonkyo Suh, Nina Tonnu, Petra M. Nederlof, Fred H. Gage und Inder M. Verma
BRCA1-Tumorsuppression erfolgt über heterochromatinvermittelte Stilllegung
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu