
11. Juni 2020
Die Influenza-Studie von Salk und Yale könnte als Grundlage für Impfstoffe gegen COVID-19 und andere Lungenerkrankungen dienen
Die Influenza-Studie von Salk und Yale könnte als Grundlage für Impfstoffe gegen COVID-19 und andere Lungenerkrankungen dienen
LA JOLLA – Eine bedeutende Schadensstelle während einer COVID-19-Infektion ist die Lunge. Zu verstehen, wie die Immunzellen der Lunge auf Virusinfektionen reagieren, könnte Wissenschaftlern bei der Entwicklung eines Impfstoffs helfen.
Jetzt ein Forscherteam unter der Leitung von Salk-Professor Susan Kaech hat herausgefunden, dass die Zellen, die für die langfristige Immunität in der Lunge verantwortlich sind, leichter aktiviert werden können als bisher angenommen. Die Einsicht, veröffentlicht in der Zeitschrift für experimentelle Medizin am 11. Juni 2020 könnte zur Entwicklung universeller Impfstoffe gegen Influenza und das neuartige Coronavirus beitragen.
„In unserer Lunge befinden sich langlebige Killer-T-Zellen, die bestimmte Viren erkennen und uns vor einer erneuten Infektion schützen, falls wir dem Virus erneut begegnen. Unsere Ergebnisse haben aufgeklärt, wie diese Zellen das Virus bei einer erneuten Infektion „sehen“ und für eine schnelle Immunität sorgen“, sagt Kaech, Direktor des NOMIS-Zentrums für Immunbiologie und mikrobielle Pathogenese in Salk. „Es kann uns auch helfen, die langfristige Immunität im Zusammenhang mit dem Coronavirus zu verstehen.“
Wenn wir zum ersten Mal Bakterien oder Viren wie der Grippe ausgesetzt sind, zerstört eine Art unserer Immunzellen, sogenannte Killer-T-Zellen, infizierte Zellen, um die Ausbreitung der Krankheit zu verhindern. Sobald der Erreger beseitigt ist, verbleiben diese erfahrenen Killer-T-Zellen (auch Killer-„Gedächtnis“-T-Zellen genannt) langfristig in unserem Körper und „erinnern“ sich an frühere Eindringlinge. Diese Killer-Gedächtnis-T-Zellen ermöglichen es unserem Immunsystem, schneller auf einen zweiten Angriff zu reagieren und effektiv eine langfristige schützende Immunität gegen den Eindringling bereitzustellen – ein grundlegendes Konzept der Impfung.
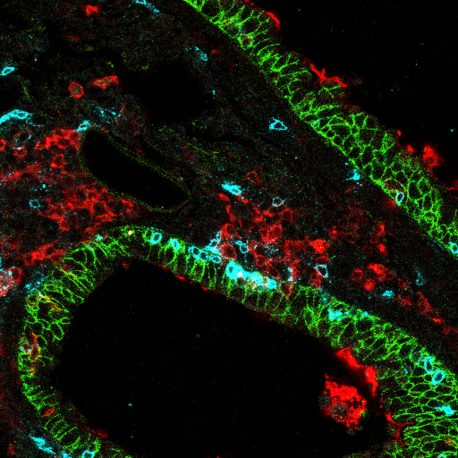
Zu den offenen Stellen für ein hochauflösendes Bild.
Bildnachweis: Salk Institute
Wissenschaftler wissen viel darüber, wie Killer-Gedächtnis-T-Zellen in lymphatischen Organen (z. B. Lymphknoten) aktiviert werden. Immun-Botenzellen, sogenannte dendritische Zellen, präsentieren der Killer-Gedächtnis-T-Zelle Fragmente des Virus, ähnlich wie ein Hundeführer einem Hund einen Duft präsentiert, um seine Killerfunktion zu lizenzieren.
Bisherige Studien hatten diese Wechselwirkung in lebenswichtigen Organen wie der Lunge jedoch nicht untersucht. Die Lunge ist eine häufige Eintrittspforte für Krankheitserreger wie Influenza und Coronaviren. Deshalb wollte das Team bestätigen, ob dieses lange gehegte Dogma auf Killer-Gedächtnis-T-Zellen zutrifft, die sich in der Lunge befinden.
Kaech und der damalige Doktorand Jun Siong Low, Erstautor der Arbeit, gingen davon aus, dass dendritische Zellen erforderlich wären, um Killer-Gedächtnis-T-Zellen zu reaktivieren, um einen zweiten Virusangriff abzuwehren. Deshalb löschten sie bei Mäusen nacheinander verschiedene Arten von Botenzellen aus, um zu sehen, ob die Killer-Gedächtnis-T-Zellen eine zweite Influenza-Infektion noch erkennen würden. Die Forscher verwendeten ein grün fluoreszierendes Reporterprotein, um die Killer-Gedächtnis-T-Zellen zum Leuchten zu bringen, wenn sie das Virus erkannten. Doch jedes Mal, wenn die Forscher einen bestimmten Zelltyp löschten, leuchteten die Killer-Gedächtnis-T-Zellen in der Lunge weiter.
„Zuerst waren unsere Ergebnisse enttäuschend, weil es den Anschein hatte, als ob unsere Experimente nicht funktionierten; Die Killer-Gedächtnis-T-Zellen in der Lunge erkannten das Virus weiterhin, nachdem viele verschiedene Botenzelltypen gelöscht wurden“, sagt Low, jetzt Postdoktorand am Institut für biomedizinische Forschung (IRB) der Università della Svizzera Italiana in der Schweiz . „Wir erkannten bald, dass diese in der Lunge ansässigen Killer-Gedächtnis-T-Zellen etwas Besonderes waren, weil sie nicht auf einen einzelnen Typ von Botenzellen angewiesen waren. Stattdessen konnten sie die zweite Influenza-Infektion durch eine Vielzahl verschiedener Botenzellen „sehen“, darunter auch nicht-immune Zellen wie Lungenepithelzellen, was eine bemerkenswert aufregende Entdeckung war.“

Zu den offenen Stellen für ein hochauflösendes Bild.
Bildnachweis: Salk Institute
Als die Forscher dagegen die Killer-Gedächtnis-T-Zellen in den Lymphknoten untersuchten – Drüsen, die bei Infektionen anschwellen – stellten sie fest, dass die Killer-Gedächtnis-T-Zellen dendritische Zellen benötigten, um den zweiten Virusangriff zu erkennen. Dies deutet darauf hin, dass die anatomische Lage der Killer-Gedächtnis-T-Zellen bestimmt, wie sie reaktiviert werden, was das seit langem vertretene Dogma in Frage stellt, dass Killer-Gedächtnis-T-Zellen für ihre Reaktivierung dendritische Zellen benötigen. Die Ergebnisse tragen dazu bei, das Paradigma der Aktivierung von Killer-Gedächtnis-T-Zellen neu zu gestalten.
Da in der Lunge lebende Killer-Gedächtnis-T-Zellen von fast jedem Zelltyp an der Eintrittsstelle des Krankheitserregers schnell reaktiviert werden können, wird die Identifizierung von Impfstoffen, die diese in der Lunge lebenden Killer-Gedächtnis-T-Zellen erzeugen können, wahrscheinlich von entscheidender Bedeutung für eine überlegene Immunität gegen Virusinfektionen der Lunge sein .
„Diese Erkenntnisse werden wir in unsere nächste Studie einfließen lassen und untersuchen, ob sich nach einer Coronavirus-Infektion lungenresidente Killer-Gedächtnis-T-Zellen bilden“, sagt Kaech, Inhaber des NOMIS-Lehrstuhls. „Da nicht alle Infektionen Killer-Gedächtnis-T-Zellen induzieren, werden wir feststellen, ob sich diese Zellen nach einer Coronavirus-Infektion bilden und ob sie vor zukünftigen Coronavirus-Infektionen schützen können.“
Zu den weiteren Autoren gehörten Yagmur Farsakoglu aus Salk; Esen Sefik, Christian CD Harman, Ruaidhri Jackson, Justin Shyer, Xiaodong Jiang und Richard A. Flavell von der Yale University School of Medicine; Maria Carolina Amezcua Vesely von der Universidad Nacional de Córdoba in Argentinien; Joseph B. Kelly von der Stony Brook University und Linda S. Cauley vom University of Connecticut Health Center.
Die Arbeit wurde von der NOMIS Foundation unterstützt; die National Institutes of Health (R01 AI123864, R37 AI066232, S10 OD020142, P30 CA106359-39); A*STAR National Science Scholarship PhD; ein Early Postdoc Mobility Fellowship des Schweizerischen Nationalfonds (P2BEP3_178444); ein Stipendium der George E. Hewitt Foundation; das Howard Hughes Medical Institute; das Yale Center for Research Computing; das Yale Center for Genome Analysis; und der Waitt Advanced Biophotonics Core am Salk Institute for Biological Studies.
DOI: doi.org/10.1084/jem.20192291
JOURNAL
Zeitschrift für experimentelle Medizin
AUTOREN
Jun Siong Low, Yagmur Farsakoglu, Maria Carolina Amezcua Vesely, Esen Sefik, Joseph B. Kelly, Christian CD Harman, Ruaidhri Jackson, Justin Shyer, Xiaodong Jiang, Linda S. Cauley, Richard A. Flavell und Susan M. Kaech.
Büro für Kommunikation
Tel: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Das Institut hat es sich zur Aufgabe gemacht, grundlegende, kooperative und risikoreiche Forschung zu betreiben, die sich mit den drängendsten gesellschaftlichen Herausforderungen wie Krebs, Alzheimer und der Anfälligkeit der Landwirtschaft auseinandersetzt. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und generiert Erkenntnisse, die weltweit die Entwicklung neuer Medikamente und Innovationen ermöglichen.