
December 23, 2010
LA JOLLA, Kalifornien – Forscher am Salk Institute for Biological Studies haben herausgefunden, wie AMPK, ein metabolischer Hauptschalter, der in Gang kommt, wenn den Zellen die Energie ausgeht, ein zelluläres Recyclingprogramm in Gang setzt, um in Zeiten der Not wichtige molekulare Bausteine freizusetzen .
In einem Artikel, der in der Ausgabe vom 23. Dezember 2010 veröffentlicht wurde Wissenschafts-Express, ein Team unter der Leitung von Reuben Shaw, PhD., Nachwuchswissenschaftler am Howard Hughes Medical Institute und Assistenzprofessor am Salk's Molecular and Cell Biology Laboratory, berichtet, dass AMPK einen zellulären Recyclingprozess namens Autophagie aktiviert, indem es ein Enzym namens ATG1 aktiviert, das den Prozess in Gang setzt.
Der neu entdeckte direkte molekulare Zusammenhang zwischen AMPK und ATG1 ist von Bedeutung, da Funktionsstörungen sowohl der AMPK-Signalübertragung als auch der Autophagie mit einer Vielzahl altersbedingter Krankheiten in Zusammenhang stehen, darunter Typ-II-Diabetes, Krebs und neurodegenerative Erkrankungen wie Parkinson und Alzheimer.
Trotz des ominösen Namens, der sich von „selbst“ (auto) und „essend“ (Phagie) ableitet, nutzen Zellen die Autophagie, um Trümmer zu beseitigen, bevor sie giftig genug werden, um eine Zelle abzutöten. „Autophagie ist ein uralter Prozess, der sich entwickelt hat, um Komponenten, die Zellen nicht brauchen, abzubauen, um Dinge zu schaffen, die sie wirklich brauchen“, sagt Dan Egan, ein Doktorand in Shaws Labor und Erstautor der Studie.
Zuvor hatte Shaws Labor nicht nur gezeigt, dass AMPK bei bestimmten Krebsarten dereguliert ist, sondern auch, dass das Enzym ein kritisches Ziel des Typ-2-Diabetes-Medikaments Metformin ist. „Die Einnahme eines Medikaments, das diesen Signalweg aktiviert, wie Metformin, ist das Äquivalent zur Einnahme mehrerer verschiedener Medikamente“, sagt Shaw und zählt eine Liste von Antitumor- und Antidiabetes-Signalwegen auf, die durch AMPK aktiviert werden. „Jetzt können wir dieser Liste die Regulierung der Autophagie hinzufügen.“
Shaws Labor hat Autophagie bisher noch nicht untersucht, interessiert sich aber seit langem für AMPK, das erkennt, wenn die Energie niedrig ist, und das Zellwachstum verlangsamt. „Da AMPK eine so zentrale Rolle bei der Regulierung des Energiehaushalts unserer Zellen spielt, wollten wir wissen, wie es seine Macht auf so viele zelluläre Prozesse ausübt“, sagt Shaw.
Sein Team leitete die Studie ein, indem es eine einzigartige Targeting-Sequenz definierte, die AMPK zur Übertragung seiner Signale verwendet, und dann mithilfe von Bioinformatik und Biochemie Proteine identifizierte, die als AMPK-Ziele fungieren. Einer der Hauptverdächtigen, die dabei identifiziert wurden, war das Protein Atg1/ULK1, ein Faktor, der bei Hefen Autophagie auslöst.
Um die Auswirkungen der Deregulierung dieser Enzyme auf die Autophagie zu testen, konzentrierte sich die Gruppe auf große intrazelluläre Strukturen, sogenannte Mitochondrien, deren Aufgabe es ist, Energie zu erzeugen. „Mitochondrien werden in entgiftenden Geweben wie der Leber leicht beschädigt“, erklärt Shaw. „Eine entscheidende Möglichkeit, defekte Mitochondrien auszutauschen, ist eine spezielle Form der Autophagie, die Mitophagie genannt wird.“
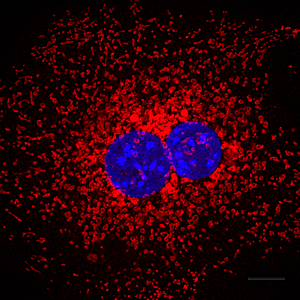
Wenn der Prozess der Autophagie fehlerhaft ist, sind Zellen nicht in der Lage, Zellorganellen wie Mitochondrien (in Rot dargestellt) zu recyceln, um bei Bedarf molekulare Bausteine zu erzeugen. Zellkerne sind blau dargestellt.
Bild: Mit freundlicher Genehmigung von Daniel Egan, Salk Institute for Biological Studies
In diesem Fall würden Zellen ihre ungesunden Mitochondrien mit einer Membran umhüllen, sie in eine zelluläre Säuregrube werfen und die Überreste recyceln. Wenn AMPK den Prozess auslöste, könnten gentechnisch veränderte Zellen, denen AMPK fehlt, im Vergleich zu normalen Zellen einen veränderten mitochondrialen Umsatz aufweisen.
Und genau das sahen die Forscher: Leberzellen, in denen AMPK eliminiert worden war, enthielten zu viele Mitochondrien, von denen viele dürr aussahen, was darauf hindeutete, dass sie sterbend waren, und bestätigte, dass AMPK die autophagische Abfallentsorgung steuerte. „Wir fanden heraus, dass die Fähigkeit, ihre defekten Mitochondrien zu recyceln, es den Zellen ermöglichte, den Hunger besser zu überstehen“, sagt Shaw.
Um alles zusammenzubringen, verwendeten die Forscher den Spulwurm C. elegans, einem beliebten Modellsystem in der Alterungsforschung, um zu zeigen, dass aktiviertes AMPK die Autophagie durch ein Signal, das von der Wurmversion von Atg1/ULK1 weitergeleitet wird, direkt aktiviert – Experimente, die in Zusammenarbeit mit Malene Hansen, Ph.D., von Sanford-Burnham Medical in La Jolla durchgeführt wurden Forschungsinstitut und mit Hilfe von Andy Dillin, Ph.D., vom Labor für Molekular- und Zellbiologie in Salk.
„Die Wurmexperimente zeigen, dass der Zusammenhang zwischen AMPK, ULK1 und Autophagie über die gesamte Evolution hinweg erhalten bleibt und nicht nur eine neue, für Säugetiere spezifische Anpassung ist“, sagt Egan. „Lebenswichtige Prozesse wie Energieregulierung, Stoffwechsel und Autophagie haben bei Menschen, Mäusen, Würmern und Hefen gemeinsame Komponenten.“
Aber wenn Sie kein Evolutionsbiologe sind, haben Sie immer noch ein persönliches Interesse an der AMPK-Signalisierung, wenn Sie: regelmäßig Sport treiben, ein gutes Gefühl beim Trinken von Rotwein haben, Diabetes-Medikamente einnehmen und/oder in der Hoffnung auf ein langes Leben hungern – allesamt die angeblich AMPK-Signale stimulieren.
Wenn man dazu noch die Möglichkeit hinzufügt, dass AMPK eine Anti-Tumor-Aktivität haben könnte, ist es kein Wunder, dass Pharmaunternehmen sehr daran interessiert sind, mit welchen Proteinen AMPK „kommuniziert“ und wie Medikamente wirken, die diese Konversation anregen.
An der Studie beteiligten sich außerdem: David Shackelford, Maria Mihaylova, Rebecca Kohnz, William Mair, Debbie Vasquez, Dana Gwinn und Rebecca Taylor, alle vom Labor für Molekular- und Zellbiologie am Salk; James Fitzpatrick vom Waitt Advanced Biophotonics Center in Salk; Sara Gelino vom Sanford-Burnham Medical Research Institute; Aashish Joshi und Mondira Kundu vom St. Jude Children's Research Hospital; John Asara von der Harvard Medical School; und Benoit Viollet vom Institut Cochin in Paris.
Diese Arbeit wurde durch Zuschüsse der National Institutes of Health, der American Cancer Society, der American Diabetes Association, des Howard Hughes Medical Institute, des Burroughs Welcome Fund, der American Libanese Syrian Association, der Agence Nationale de la Recherche und von Ellison Medical unterstützt Foundation und dem Leona M. and Harry B. Helmsley Charitable Trust.
Über das Salk Institute for Biological Studies:
Das Salk Institute for Biological Studies ist eine der weltweit herausragenden Grundlagenforschungseinrichtungen, in der international renommierte Dozenten in einem einzigartigen, kollaborativen und kreativen Umfeld grundlegende Fragen der Biowissenschaften untersuchen. Salk-Wissenschaftler konzentrieren sich sowohl auf Entdeckungen als auch auf die Betreuung zukünftiger Forschergenerationen und leisten bahnbrechende Beiträge zu unserem Verständnis von Krebs, Alterung, Alzheimer, Diabetes und Infektionskrankheiten, indem sie Neurowissenschaften, Genetik, Zell- und Pflanzenbiologie und verwandte Disziplinen studieren.
Die Leistungen der Fakultät wurden mit zahlreichen Ehrungen gewürdigt, darunter Nobelpreise und Mitgliedschaften in der National Academy of Sciences. Das 1960 vom Polioimpfpionier Jonas Salk, MD, gegründete Institut ist eine unabhängige gemeinnützige Organisation und ein architektonisches Wahrzeichen.
Das Salk Institute feiert stolz fünf Jahrzehnte wissenschaftlicher Exzellenz in der Grundlagenforschung.
Büro für Kommunikation
Tel: (858) 453-4100
press@salk.edu