
Juli 14, 2011
Ziel der Forschung ist es, aus patienteneigenen Zellen Stammzellen herzustellen, die verlorenes oder erkranktes Gewebe ersetzen können
Ziel der Forschung ist es, aus patienteneigenen Zellen Stammzellen herzustellen, die verlorenes oder erkranktes Gewebe ersetzen können
LA JOLLA, Kalifornien – Wissenschaftler am Salk Institute for Biological Studies haben eine verbesserte Technik zur Erzeugung einer großen Anzahl von Blutzellen aus patienteneigenen Zellen entwickelt. Die neue Technik wird sofort für weitere Stammzellstudien von Nutzen sein und könnte, wenn sie perfektioniert ist, in Stammzelltherapien für eine Vielzahl von Erkrankungen eingesetzt werden, darunter Krebs und Immunerkrankungen.
„Es gibt noch weitere Verbesserungen, die wir vornehmen müssen, aber dies bringt uns einen großen Schritt näher an das Endziel heran, das darin besteht, gewöhnliche Zellen von einem Patienten zu entnehmen, sie zu Stammzellen zu bewegen und diese Stammzellen dann zu verwenden.“ um verlorenes oder erkranktes Gewebe, zum Beispiel das Knochenmark des Patienten, wieder aufzubauen“, sagt Inder M. Verma, PhD, Irwin und Joan Jacobs Lehrstuhl für beispielhafte Biowissenschaften und Professor für Molekularbiologie der American Cancer Society am Salk Institute Laboratory of Genetics. Verma ist leitende Autorin des Berichts, der in der Juli-Ausgabe der Zeitschrift veröffentlicht wird Stammzellen.
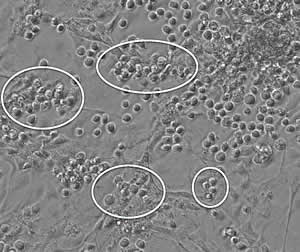
Runde hämatopoetische (Blut-)Zellen entstehen aus differenzierenden menschlichen pluripotenten Stammzellen.
Foto: Mit freundlicher Genehmigung von Aaron Parker, Salk Institute for Biological Studies
Stammzellforscher streben seit 2006, als erstmals über Techniken zur Umwandlung gewöhnlicher Hautzellen in induzierte pluripotente Stammzellen (iPSCs) berichtet wurde, auf dieses Ziel zu. Im Prinzip ahmen iPSCs die embryonalen Stammzellen (ESCs) nach, aus denen sich Organismen entwickeln. Forscher wollen nun die präzisen Mischungen und Sequenzen chemischer Verbindungen finden, die erforderlich sind, um iPSCs dazu zu bringen, zu den gewebespezifischen Stammzellen ihrer Wahl zu reifen. Letztere erneuern sich selbst und können in den Körper transplantiert werden, um die „Vorläuferzellen“ zu produzieren, die sich lokal vermehren und reife Gewebezellen produzieren.
Allerdings wissen Forscher noch nicht, wie man iPSCs mit hoher Effizienz dazu bringen kann, gewebespezifische Stammzellen oder reife Gewebezellen zu werden. „Wir haben diese Zellen in zu geringen Mengen produziert, um sie einfach untersuchen zu können, geschweige denn für Therapien“, sagt Aaron Parker, PhD, ein ehemaliger Doktorand und jetzt Postdoktorand in Vermas Labor. Parker ist Co-Hauptautor des Papiers, zusammen mit Niels-Bjarne Woods, PhD, der zu Beginn des Projekts Postdoktorand im Verma-Labor war und jetzt Assistenzprofessor an der Universität Lund in Schweden ist.
Wie viele andere Stammzellforschungslabore hat auch das Verma-Labor versucht, effizientere Wege zu finden, um iPSCs in blutbildende „hämatopoetische“ Stammzellen (HSCs) umzuwandeln. Diese könnten medizinisch wertvoller sein als alle anderen gewebespezifischen Stammzellen, da sie nicht nur sauerstofftragende rote Blutkörperchen, sondern auch alle weißen Blutkörperchen des Immunsystems versorgen können. „Für echte HSCs gäbe es nahezu unbegrenzte Einsatzmöglichkeiten“, sagt Verma.
Für die vorliegende Studie versuchte das Forschungsteam, die sich ändernden Bedingungen, die ESCs auf natürliche Weise dazu bringen, im Mutterleib HSCs zu werden, besser nachzuahmen. „Wir haben sieben Linien menschlicher ESCs und iPSCs genommen und mit verschiedenen Kombinationen und Sequenzen von Wachstumsfaktoren und anderen chemischen Verbindungen experimentiert, die bekanntermaßen vorhanden sind, wenn ESCs in einem sich entwickelnden Menschen in den HSC-Zustand übergehen“, sagt Parker.
Durch die Anwendung von Cocktails dieser Faktoren veranlassten Parker und Woods und ihre Kollegen die iPSCs und ESCs, Zellkolonien zu bilden, die die charakteristischen molekularen Marker von Blutzellen trugen. Mit ihrem besten Cocktail konnten sie nach drei Wochen blutspezifische Marker auf 84 % ihrer Zellen nachweisen. „Das ist ein großer Effizienzsprung im Vergleich zu dem, was wir noch vor ein paar Jahren in der Praxis gesehen haben“, sagt Parker.
Die Technik hat noch Raum für Verbesserungen. Die Forscher entdeckten Vorläuferzellen und reife Zellen nur aus einer Kategorie oder Linie: myeloische Zellen, zu denen rote Blutkörperchen und primitive Immunzellen wie Makrophagen gehören. „Wir haben keine Zellen aus der Lymphlinie, also T-Zellen und B-Zellen, gesehen“, sagt Parker.
Ein weiterer Nachteil bestand darin, dass die von ihnen aus ESCs und iPSCs erzeugte Blutzellpopulation kurzlebige Vorläuferzellen und reife Blutzellen, aber keine sich unbegrenzt erneuernden, transplantierbaren HSCs enthielt. Sie glaubten, dass ihr Cocktail die Zellen entweder zu schnell über den HSC-Zustand hinaus in den Vorläuferzustand drängte oder die reifenden Zellen dazu brachte, den HSC-Zustand vollständig zu überspringen.
Aufgrund dieser und anderer Laborergebnisse stellte das Team die Hypothese auf, dass es einen intermediären, prähämatopoetischen Stammzelltyp gibt, der von ESCs und iPSCs produziert wird und wiederum HSCs produziert. „Wir wissen, dass HSCs während der Embryonalentwicklung in einer bestimmten Region von Säugetieren auftreten, und unsere Idee ist, dass diese prähämatopoetischen Stammzellen dort sind und irgendwie dazu gebracht werden, zu HSCs zu reifen“, sagt Parker. „Unser Labor wird sich nun darauf konzentrieren, die genauen Reifungssignale dieser embryonalen Region zu finden, um diese echten, transplantierbaren HSCs zu produzieren.“
Sobald dies geschehen ist, müssen die Forscher eine Reihe weiterer Verbesserungen vornehmen, um die Sicherheit von HSCs für menschliche Patienten zu verbessern. „Aber jetzt sind wir unserem Endziel ganz nah“, sagt Verma.
Die anderen Autoren, die zu der Arbeit beigetragen haben, waren Roksana Moraghebi vom Stammzellenzentrum der Universität Lund; Margaret K. Lutz, Amy L. Firth, Kristen J. Brennand, W. Travis Berggren und Fred H. Gage vom Salk Institute Laboratory for Genetics; Juan Carlos Izpisúa Belmonte vom Genexpressionslabor des Salk Institute; und Angel Raya vom Zentrum für Regenerative Medizin in Barcelona, Spanien.
Die Finanzierung dieser Forschung erfolgte durch die National Institutes for Health, das California Institute for Regenerative Medicine, die Leducq Foundation, die Merieux Foundation, die Ellison Medical Foundation, Ipsen/Biomeasure, Sanofi Aventis, die Prostate Cancer Foundation, die HN und Frances C . Berger Foundation, The Royal Physiographic Society of Sweden, die Medizinische Fakultät der Universität Lund und die Lars Hierta Memorial Foundation sowie der HA and Mary K. Chapman Charitable Trust.
Über das Salk Institute for Biological Studies:
Das Salk Institute for Biological Studies ist eine der weltweit herausragenden Grundlagenforschungseinrichtungen, in der international renommierte Dozenten in einem einzigartigen, kollaborativen und kreativen Umfeld grundlegende Fragen der Biowissenschaften untersuchen. Salk-Wissenschaftler konzentrieren sich sowohl auf Entdeckungen als auch auf die Betreuung zukünftiger Forschergenerationen und leisten bahnbrechende Beiträge zu unserem Verständnis von Krebs, Alterung, Alzheimer, Diabetes und Infektionskrankheiten, indem sie Neurowissenschaften, Genetik, Zell- und Pflanzenbiologie und verwandte Disziplinen studieren.
Die Leistungen der Fakultät wurden mit zahlreichen Ehrungen gewürdigt, darunter Nobelpreise und Mitgliedschaften in der National Academy of Sciences. Das 1960 vom Polioimpfpionier Jonas Salk, MD, gegründete Institut ist eine unabhängige gemeinnützige Organisation und ein architektonisches Wahrzeichen.
Büro für Kommunikation
Tel: (858) 453-4100
press@salk.edu