أستاذ جمعية السرطان الأمريكية
معمل البيولوجيا الجزيئية والخلوية
كرسي ريناتو دولبيكو


تشبه الخلايا مخلوقات العادة - فهي تتبع نفس الدورة الخلوية مرارًا وتكرارًا ، وتنسق توقيت تنشيط الجين والبروتين مع النمو والانقسام. إذا تم كسر هذه الدورة ، تبدأ الأشياء في الانهيار: تبدأ الخلايا في نسخ الجينات الخاطئة ، أو تشغيل البروتينات في الأوقات الخاطئة أو الانقسام بسرعة كبيرة أو ببطء شديد. كل هذه الاضطرابات يمكن أن تؤدي إلى الإصابة بالسرطان. إن فهم كيفية تحكم الخلية السليمة في دورة نموها يمكن أن يساعد الباحثين على فهم أفضل للخطأ الذي يحدث في الخلايا السرطانية عندما يخرج نموها عن السيطرة - وكيفية إصلاحه. لكن من الصعب تحديد الجينات والبروتينات الفردية الأكثر أهمية.
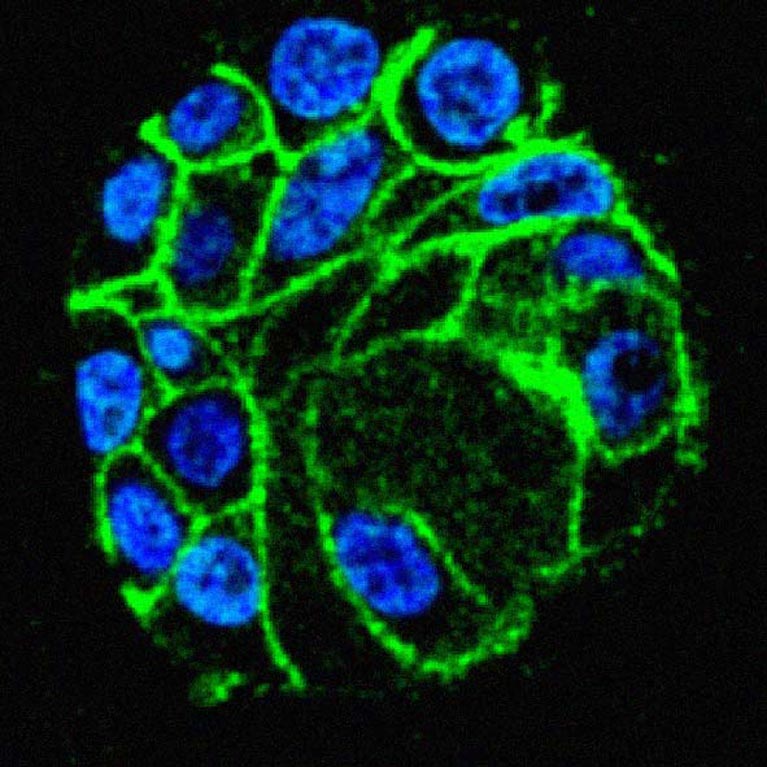
اكتشف توني هانتر ، منذ أكثر من أربعة عقود ، أن إضافة وطرح جزيئات الفوسفات إلى البروتينات الموجودة في التيروزين ، وهو أحد الأحماض الأمينية العشرين ، يسمح للخلايا بالتحكم عندما تكون البروتينات الرئيسية في وضع الاستعداد وعندما تكون نشطة. ومضى ليوضح أنه في حالات السرطان ، تم تحويل النمو إلى الوضع الدائم بسبب الأعطال في هذه الفوسفات. منذ ذلك الحين ، قاد مختبره مجال فهم كيفية تحكم الإضافات الكيميائية للبروتينات في دورة الخلية ونموها. يستخدم Hunter أحدث التقنيات الجزيئية والوراثية والبيولوجية الخلوية لاستكشاف كيفية تفاعل هذه البرامج مع بعضها البعض ، وما تأثيرها على الخلايا وكيف تعطلها السرطانات لتشجيع النمو غير المقيد.
لقد تم بالفعل تصميم عقاقير السرطان - مثل علاج سرطان الدم Gleevec ™ - بناءً على اكتشافات هنتر. يقوم جليفيك بإيقاف عمل إنزيم يضيف الفوسفات إلى التيروزينات في البروتينات ، وبالتالي يمنع السرطان من النمو. بينما يواصل هنتر اكتشاف طرق أخرى تستخدم بها الخلايا الإضافات الكيميائية للبروتينات للتحكم في نموها ، فإنه يهدف إلى إيجاد أهداف علاجية محتملة للسرطانات.
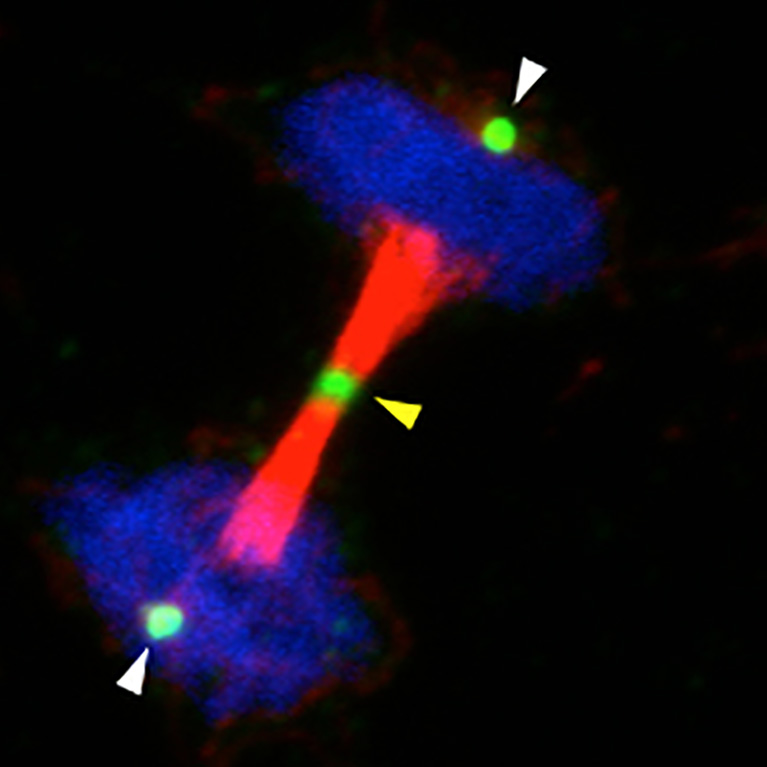
أظهر هانتر أن آلية تسمى فسفرة التيروزين (إضافة جزيئات الفوسفات إلى حمض أميني في البروتينات) تعمل كمفتاح تشغيل / إيقاف رئيسي لعدد من البروتينات الرئيسية. أدى هذا الاكتشاف إلى علاجات جديدة وناجحة للسرطان.
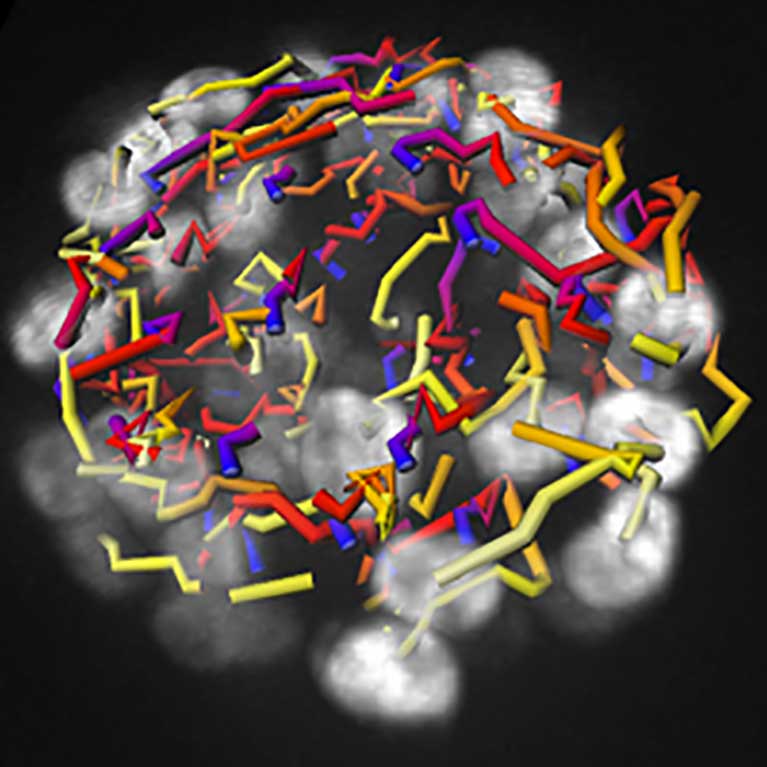
ساعد هانتر في شرح كيفية حشد الخلايا لأطقم الإصلاح الخاصة بها لإصلاح تلف الحمض النووي ، وهي آلية مهمة لمنع الخلايا من التحول إلى خلايا سرطانية.
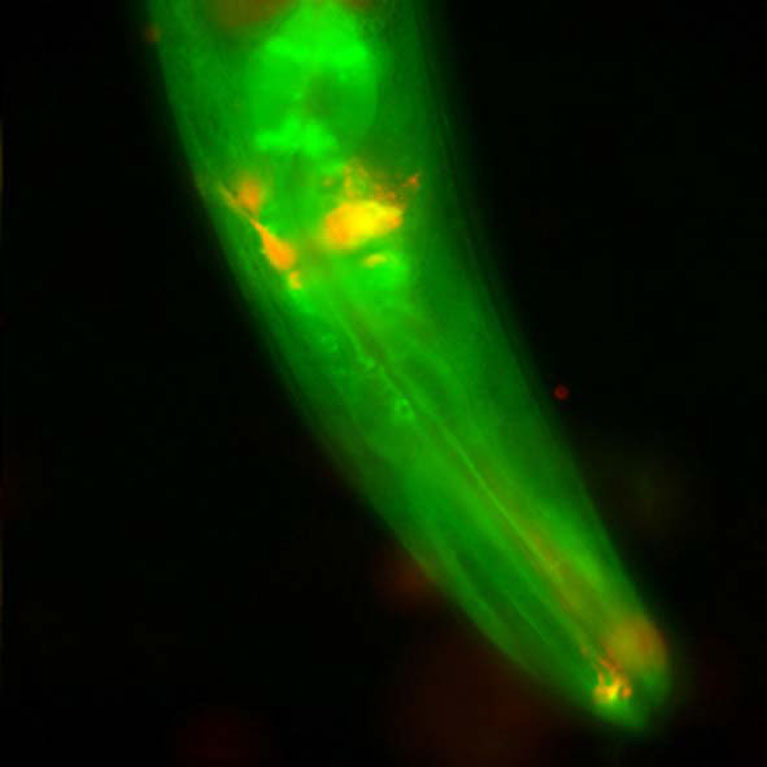
أظهر هانتر كيف تجد بعض السرطانات ثغرة في نظام الأمن الخلوي يجب أن تدمرها ، مما يساعدها على التعافي واستئناف الانقسام بعد العلاج بأدوية السرطان المدمرة للحمض النووي. في سرطان البنكرياس ، لا تستطيع الأدوية الوصول إلى الورم بسبب حاجز التهابي ناتج عن الحديث المتبادل بين الورم وخلايا البنكرياس ، لكن هانتر وجد طريقة لتعطيل هذا الاتصال عبر جزيء إشارات يسمى LIF. يمكن أن يكون LIF علامة بيولوجية مفيدة أو هدفًا لعلاج سرطان البنكرياس.
بكالوريوس ، مع مرتبة الشرف الأولى ، جامعة كامبريدج ، إنجلترا
دكتوراه ، جامعة كامبريدج ، إنجلترا
زميل ما بعد الدكتوراه ، معهد سالك وجامعة كامبريدج