
19 de novembro de 2014
Uma combinação de duas drogas inesperadas visa tumores
Uma combinação de duas drogas inesperadas visa tumores
LA JOLLA – Cientistas do Salk Institute descobriram um poderoso golpe duplo para combater uma mutação genética comum que muitas vezes leva a resistência a medicamentos cancros. A terapia com drogas duplas – com análogos já em uso para outras doenças – dobrou a taxa de sobrevivência de camundongos com câncer de pulmão e interrompeu o câncer nas células pancreáticas.
O câncer de pulmão, que afeta não fumantes e fumantes, é o câncer mais comum em todo o mundo, causando 1.6 milhões de mortes por ano, muito mais do que o câncer de pâncreas, mama e cólon combinados. Cerca de 30 por cento do tipo mais comum de câncer de pulmão (não pequeno) contém uma mutação em um gene chamado KRAS. Essa mutação também pode levar a câncer de difícil tratamento no pâncreas, tireóide e cólon.
“Realmente não houve tratamentos eficazes para atingir a mutação KRAS até agora”, diz Inder Verma, um professor na Laboratório de Genética e Professor de Biologia Molecular da American Cancer Society. “Encontramos uma combinação de medicamentos que atinge com sucesso o KRAS e interrompe o crescimento do tumor no modelo de camundongo”.
A nova descoberta, detalhada em 19 de novembro em Science Translational Medicine, mostra como o ataque em duas frentes impediu com sucesso o KRAS e outros processos celulares para interromper ou diminuir o crescimento do tumor.
Quando ativado, o KRAS mutante se apega às membranas celulares e recruta proteínas para aumentar o crescimento do câncer. Os pesquisadores desenvolveram drogas para desativar as enzimas que prendem o KRAS à membrana celular, mas essas drogas normalmente acabaram sendo tóxicas porque essas enzimas são necessárias no corpo para funções normais.
“O calcanhar de Aquiles do KRAS é seu movimento para a membrana”, diz Verma, que também é titular da Salk's Irwin e da cadeira Joan Jacobs em Exemplar Life Science.

Yifeng Xia e Inder Verma, professor do Laboratório Salk de Genética
Clique aqui para uma imagem de alta resolução.
Imagem: Cortesia do Salk Institute for Biological Studies
Os pesquisadores adotaram uma nova abordagem para direcionar essa interação da membrana quando notaram que uma droga chamada Zometa, normalmente usada para interromper a quebra e o crescimento de células em doenças ósseas, também interferia nas interações da membrana celular. Em trabalhos anteriores, a equipe adicionou cadeias de carbono a uma molécula semelhante ao Zometa, para criar um bisfosfonato (BP) lipofílico que bloqueava a ligação do KRAS à membrana celular.
“Pela primeira vez, conseguimos interferir no KRAS sem ser completamente tóxico”, diz Verma.
Isso, no entanto, não foi suficiente. Os tumores ainda proliferavam, em parte porque a nova BP levou a tentativas fracassadas de um processo chamado autofagia, em que as células, sob estresse, se autodestroem e se decompõem em nutrientes que podem ser usados por outras células.
A autofagia pode ser boa ou ruim no combate ao câncer: em alguns casos, a autofagia faz com que as células cancerígenas morram; em outras configurações, cria um ambiente celular que ajuda os tumores a prosperar. Com o tratamento com BP, as células iniciaram o processo de autofagia, mas falharam, levando ao acúmulo de proteínas inúteis e a um ambiente inflamado que ajudou os tumores a sobreviver.
Mas, como demonstrado no novo trabalho, quando os pesquisadores adicionaram uma substância química chamada rapamicina, as células conseguiram realizar a autofagia com sucesso e impediram a proliferação de células tumorais. A rapamicina, descoberta na década de 1970, é usada na clínica para prevenir a rejeição de órgãos e também tem sido associada a efeitos anticancerígenos.
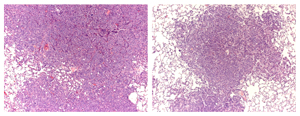
A mutação do gene KRAS leva a um câncer de pulmão comum e difícil de tratar. Uma nova terapia de combinação (bifosfonato lipofílico e rapamicina) administrada a camundongos por 40 dias resultou na redução do tamanho do tumor (à direita).
Clique aqui para uma imagem de alta resolução.
Imagem: Cortesia do Salk Institute for Biological Studies
“Descobrimos que, se também ativássemos a autofagia – com a rapamicina – e a combinássemos com o inibidor da membrana celular – a BP –, havia mortes celulares significativas nos tumores”, diz Yifeng Xia, pesquisador do Salk e primeiro autor do novo trabalho. .
Quando eles injetaram a combinação em tumores de pulmão de camundongos, os tumores encolheram ou pararam de crescer. O estudo também descobriu que uma linha celular de câncer pancreático respondeu ao tratamento duplo. Em seguida, a equipe planeja testar a toxicidade do novo BP. O grupo também está trabalhando com o Universidade da Califórnia, San Diego, Moores Cancer Center para projetar ensaios clínicos humanos para testar a terapia dupla.
“Até onde sabemos, esses dois medicamentos não foram usados juntos para o tratamento de câncer relacionado ao KRAS”, acrescenta Xia. “Estamos entusiasmados com o potencial e com o fato de essas moléculas já estarem sendo usadas em ensaios clínicos de alguma forma”.
Além de Verma e Xia, os autores do artigo incluíam Shen Shen, Narayana Yeddula, Wolfgang Fischer e William Low, do Salk Institute; Yi-Liang Liu, Wei Zhu, Francisco Guerra e Eric Oldfield da Universidade de Illinois em Urbana-Champaign; e Yonghua Xie, Xiaoying Zhou e Yonghui Zhang do Universidade de Tsinghua.
A obra foi financiada pela National Institutes of Health, Ipsen Biomeasure, o Fundação HN e Frances C. Berger e Leona M. e Harry B. Helmsley Charitable Trust.
Sobre o Salk Institute for Biological Studies:
O Salk Institute for Biological Studies é uma das instituições de pesquisa básica mais proeminentes do mundo, onde professores de renome internacional investigam questões fundamentais das ciências da vida em um ambiente único, colaborativo e criativo. Com foco na descoberta e na orientação de futuras gerações de pesquisadores, os cientistas da Salk fazem contribuições inovadoras para nossa compreensão do câncer, envelhecimento, Alzheimer, diabetes e doenças infecciosas, estudando neurociência, genética, biologia celular e vegetal e disciplinas relacionadas.
As realizações do corpo docente foram reconhecidas com inúmeras honras, incluindo Prêmios Nobel e associações na Academia Nacional de Ciências. Fundado em 1960 pelo pioneiro da vacina contra a poliomielite Jonas Salk, MD, o Instituto é uma organização independente sem fins lucrativos e um marco arquitetônico.
JORNAL
Science Translational Medicine
IMERSÃO DE INGLÊS
AUTORES
Yifeng Xia, Yi-Liang Liu, Yonghua Xie, Wei Zhu, Francisco Guerra, Shen Shen, Narayana Yeddula, Wolfgang Fischer, William Low, Xiaoying Zhou, Yonghui Zhang, Eric Oldfield, Inder M. Verma
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu