
12 de março de 2015
Pesquisadores da Salk conseguiram cultivar células saudáveis derivadas de pacientes em laboratório, chegando um passo mais perto de tratar doenças sanguíneas fatais
Pesquisadores da Salk conseguiram cultivar células saudáveis derivadas de pacientes em laboratório, chegando um passo mais perto de tratar doenças sanguíneas fatais
LA JOLLA – Para bebês com imunodeficiência combinada grave (SCID), algo tão simples como um resfriado comum ou infecção no ouvido pode ser fatal. Nascidas com um sistema imunológico incompleto, as crianças que têm SCID – também conhecidas como doença do “menino da bolha” ou do “bebê da bolha” – não conseguem combater nem mesmo o mais brando dos germes. Eles geralmente precisam viver em ambientes estéreis e isolados para evitar infecções e, mesmo assim, a maioria dos pacientes não vive mais de um ano ou dois. Isso acontece porque as células-tronco na medula óssea de pacientes com SCID têm uma mutação genética que as impede de desenvolver células imunológicas críticas, chamadas células T e Natural Killer (NK).
Agora, os pesquisadores da Salk descobriram uma maneira de, pela primeira vez, converter células de pacientes com SCID em um estado semelhante a células-tronco, corrigir a mutação genética e solicitar que as células corrigidas gerem células NK com sucesso no laboratório.
O sucesso da nova técnica sugere a possibilidade de implantar essas células ajustadas de volta em um paciente para que possam gerar um sistema imunológico. Embora o novo trabalho, publicado em 12 de março de 2015 em Cell Stem Cell, é preliminar, poderia oferecer uma abordagem potencialmente menos invasiva e mais eficaz do que as opções atuais.
“Este trabalho demonstra um novo método que pode levar a um tratamento mais eficaz e menos invasivo para esta doença devastadora”, diz o autor sênior Inder Verma, Salk professor e American Cancer Society Professora de Biologia Molecular. “Também tem o potencial de lançar as bases para curar outras doenças sanguíneas raras e mortais”.
Tentativas anteriores de tratar SCID envolveram transplantes de medula óssea ou terapia genética, com resultados mistos. No que começou como ensaios clínicos promissores na década de 1990, os pesquisadores sequestraram a maquinaria do vírus para entregar os genes necessários às células recém-criadas na medula óssea do paciente. Embora essa terapia genética tenha curado a doença no início, a adição artificial de genes acabou causando leucemia em alguns dos pacientes. Desde então, outros métodos de terapia genética foram desenvolvidos, mas geralmente são adequados para formas menos brandas da doença e requerem transplantes de medula óssea, um procedimento difícil de realizar em bebês gravemente doentes.
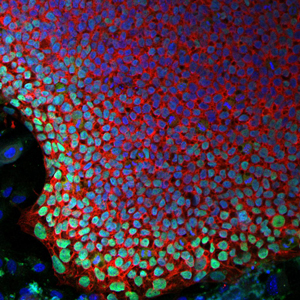
Nesta nova abordagem para tratar a “doença do menino bolha”, uma colônia de células-tronco gerada a partir de células de pacientes SCID-X1 (na foto, com núcleos celulares em azul) pode ser geneticamente corrigida e induzida a desenvolver novas células imunológicas.
Clique aqui para uma imagem de alta resolução.
Imagem: Cortesia do Salk Institute for Biological Studies
Para alcançar o novo método, a equipe Salk obteve uma amostra de medula óssea de um paciente falecido na Austrália. Usando essa pequena amostra, a equipe desenvolveu o novo método em três etapas. Primeiro, eles reverteram as células do paciente em células-tronco pluripotentes induzidas (iPSCs) – células que, como as células-tronco embrionárias, têm a capacidade de se transformar em qualquer tipo de tecido e são uma grande promessa para a medicina regenerativa.
“Uma vez que tivéssemos células-tronco derivadas de pacientes, poderíamos remover a mutação genética, essencialmente consertando as células”, explica um dos primeiros autores e pesquisador de pós-doutorado Salk, Amy Firth.
A segunda inovação foi usar a nova tecnologia de edição de genes para corrigir a deficiência genética relacionada ao SCID nessas iPSCs. Para remover a mutação, os pesquisadores usaram uma tecnologia chamada TALEN (semelhante ao método CRISPR mais conhecido). Esse conjunto de enzimas atua como uma tesoura molecular nos genes, permitindo que os pesquisadores cortem um gene e substituam os pares de bases que compõem o DNA por outros pares de bases.
"Ao contrário dos métodos tradicionais de terapia genética, não estamos colocando um gene totalmente novo em um paciente, o que pode causar efeitos colaterais indesejados", diz Tushar Menon, primeiro autor e pesquisador de pós-doutorado da Salk. “Usamos a edição do genoma baseada em TALEN para alterar apenas um nucleotídeo em um gene para corrigir a deficiência. A técnica é literalmente tão precisa.”
A terceira etapa do trabalho foi fazer com que as células se proliferassem nas células vitais do sistema imunológico - uma tarefa não fácil, mas que poderia oferecer um suprimento potencialmente ilimitado que pode ser transplantado de volta aos pacientes em intervalos. Para fazer isso, os pesquisadores colaboraram com cientistas da Universidade da Califórnia, em Los Angeles, para usar uma mistura de nutrientes e outros fatores que encorajariam as iPSCs a gerar células NK.
E eles conseguiram. Essas células corrigidas em um prato realmente desenvolveram células NK maduras.
Em seguida, a equipe está trabalhando na reprodução de outros componentes imunológicos vitais, as células T. Até agora, eles levaram as iPSCs a se transformarem nos precursores das células T, mas ainda não foram capazes de levá-las à maturidade.

A partir da esquerda: Tushar Menon, Inder Verma e Amy Firth
Clique aqui para uma imagem de alta resolução.
Imagem: Cortesia do Salk Institute for Biological Studies
“Em última análise, esperamos que esses esforços ajudem a alcançar o 'Santo Graal' no campo: a capacidade de criar células-tronco a partir de iPSCs capazes de gerar todos os tipos de sangue e células imunológicas”, diz Verma, que também é o Irwin e Joan Jacobs Chair em Ciências da Vida Exemplar. A capacidade de gerar as próprias células-tronco do sangue corrigidas poderia resultar em um tratamento único que acabaria por repor as células funcionais durante toda a vida do paciente.
“Em vez disso, temos uma alternativa que pode funcionar como um tratamento menos invasivo e com a capacidade de escalar facilmente para grandes quantidades”, diz Firth. Outro benefício de usar células derivadas de pacientes como tratamento é que o corpo do paciente normalmente não as rejeita (ao contrário do tecido de doadores).
Outros autores do artigo incluem: Susan Qualls, William Gilmore,
Eugene Ke, Oded Singer, Leif Anderson e Alexander Bornzin do Salk Institute; Deirdre Scripture-Adams, Zoran Galic e Jerome Zack de UCLA; e Ian Alexander da Instituto de Pesquisa Médica Infantil e O Hospital Infantil de Westmead na Austrália.
Este trabalho foi apoiado em parte por doações da Ipsen/Biomeasure, Sanofi Aventis, the Fundação HN e Frances C. Berger, Leona M. e Harry B. Helmsley Charitable Trust e Instituto de Medicina Regenerativa da Califórnia.
Sobre o Salk Institute for Biological Studies:
O Salk Institute for Biological Studies é uma das instituições de pesquisa básica mais proeminentes do mundo, onde professores de renome internacional investigam questões fundamentais das ciências da vida em um ambiente único, colaborativo e criativo. Com foco na descoberta e na orientação de futuras gerações de pesquisadores, os cientistas da Salk fazem contribuições inovadoras para nossa compreensão do câncer, envelhecimento, Alzheimer, diabetes e doenças infecciosas, estudando neurociência, genética, biologia celular e vegetal e disciplinas relacionadas.
As realizações do corpo docente foram reconhecidas com inúmeras honras, incluindo Prêmios Nobel e associações na Academia Nacional de Ciências. Fundado em 1960 pelo pioneiro da vacina contra a poliomielite Jonas Salk, MD, o Instituto é uma organização independente sem fins lucrativos e um marco arquitetônico.
JORNAL
Cell Stem Cell
AUTORES
Tushar Menon, Amy L. Firth, Deirdre D. Scripture-Adams, Zoran Galic, Susan J. Qualls, William B. Gilmore, Eugene Ke, Oded Singer, Leif S. Anderson, Alexander R. Bornzin, Ian E. Alexander, Jerome A. Zack e Inder M. Verma
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu