
11 de Setembro de 2008
La Jolla, CA – Neurônios que constituem o fio do nervo óptico até o cérebro de forma altamente dinâmica. Os corpos celulares na retina em desenvolvimento brotam processos, chamados axônios, que se estendem em direção aos centros visuais no cérebro, atraídos por pistas atraentes e fazendo inversões de marcha quando seguem o caminho errado. Como eles encontram alvos com tanta precisão é uma questão central da neurociência hoje.
Usando o sistema visual do mouse, uma equipe de pesquisadores do Salk Institute for Biological Studies liderada por Dennis O'Leary, Ph.D., identificou um fator imprevisto que ajuda a evitar que os axônios da retina se desviem. Eles relatam na edição de 11 de setembro da Neurônio que p75, uma proteína previamente conhecida por regular se os neurônios vivem ou morrem, leva uma vida dupla como uma proteína de orientação axônica.
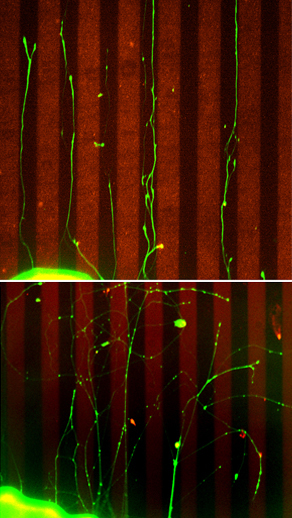
Quando neurônios imaturos são colocados em uma pista de corrida microscópica, onde as pistas laterais são acarpetadas com fatores repelentes, seus axônios em crescimento permanecem em suas pistas (topo). Neurônios de camundongos sem p75 não são receptivos a sinais repulsivos: quando colocados na pista, seus axônios serpenteiam por todo o campo, cruzando pistas e descendo por listras cobertas de repelente (abaixo).
Imagens: Cortesia do Dr. Yoo-Shick Lim, Salk Institute for Biological Studies
“Historicamente, pensávamos que os fatores que medeiam a sobrevivência celular e aqueles que controlam a orientação do axônio faziam parte de dois processos separados”, diz O'Leary, professor do Laboratório de Neurobiologia Molecular, “mas neste estudo mostramos uma interação direta entre esses dois sistemas”.
Colaborando com Kuo-Fen Lee, Ph.D., professor da Clayton Foundation Laboratories for Peptide Biology, a equipe O'Leary observou um defeito em camundongos geneticamente modificados para não ter p75. Por meio de suas conexões sinápticas, os axônios da retina desenvolvem um mapa bidimensional da retina em seus alvos no cérebro. Nos camundongos sem p75, os axônios da retina pararam perto de seu alvo final e formaram um mapa que foi deslocado para frente no colículo superior, um importante centro visual no cérebro.
Tal defeito em camundongos nulos p75 era intrigante: os pesquisadores estudaram o p75 por décadas e o descobriram associado a atividades tão variadas quanto crescimento neuronal, sobrevivência e degeneração. A migração axonal não estava entre eles.
Todd McLaughlin, Ph.D., pesquisador associado sênior no laboratório e co-primeiro autor, diz que a percepção veio em um momento eureca: “Percebemos que o que estávamos observando nesses ratos era semelhante ao que aconteceria se você excluísse um gene chamado ephrin-A da retina.”
Ao contrário de p75, a efrina-A era um transmissor e receptor bem caracterizado de sinais de orientação axônica, mas faltava apêndices normalmente vistos em proteínas que controlam a migração axônica. p75, no entanto, exibiu esses elementos, sugerindo que as proteínas poderiam se emparelhar – uma recebendo o sinal de migração e a outra transmitindo-o.
A equipe de pesquisa voltou-se para as análises bioquímicas e, com a experiência adicional de Tsung-Chang Sung, Ph.D., pesquisador associado do laboratório do Dr. Lee, obteve evidências que sustentavam essa hipótese. O grupo descobriu que a efrina-A e os complexos p75 nas membranas axonais e mostraram que, quando ativados, podiam gerar os sinais necessários para guiar os axônios e desenvolver seu mapa no cérebro.
Mas o argumento decisivo foi o “ensaio de listras”, uma tela clássica para moléculas de orientação que repelem axônios em crescimento. Nele, um neurônio imaturo é colocado em uma pista de corrida microscópica, no momento em que começa a desenvolver um axônio. Quando as pistas laterais são acarpetadas com fatores repulsivos, o axônio emergente sai do bloco, mas permanece em sua pista como um corredor bem treinado, evitando as pistas vizinhas.
Construindo faixas feitas a partir do fator repulsivo detectado pela efrina-A, os pesquisadores confirmaram que os axônios dos neurônios normais da retina permaneceram em suas faixas quando flanqueados pelo repelente. Mas os neurônios de camundongos sem p75 não eram receptivos a sinais repulsivos: quando colocados na pista, seus axônios serpenteavam por todo o campo, cruzando pistas e descendo por listras cobertas de repelente.
Por que os neurônios da retina erraram o alvo nos camundongos p75-menos ficou claro: eles não tinham a maquinaria celular para responder a sinais repelentes críticos encontrados no cérebro e pararam de migrar prematuramente.
Entre suas inúmeras funções, o novo papel do p75 é crítico. “A repulsão é provavelmente a força dominante na orientação do axônio e uma influência mais forte do que a atração”, explica McLaughlin, observando que fornecer aos axônios muitas opções não é o caminho para construir um cérebro. “A atração é como encontrar o melhor lugar em um cinema vazio, mas a repulsa é como escolher o único lugar vazio em um cinema cheio.”
“Mostramos que a efrina-A não pode transduzir um sinal intracelular por si só e, em vez disso, requer o co-receptor p75”, resume Yoo-Shick Lim, Ph.D., pós-doutorado no laboratório O'Leary e co-primeiro autor . “Essa interação pode operar em vários eventos no desenvolvimento neural”.
O'Leary acredita que identificar os mecanismos subjacentes aos eventos de desenvolvimento é fundamental para entender a base de qualquer distúrbio biológico. “Esses estudos estabelecem que dois sistemas moleculares distintos, neurotrofinas e orientação axônica, ambos críticos para o desenvolvimento neural, colaboram diretamente para desenvolver a conectividade neural.
Descobertas como essas fornecem informações críticas sobre como alguém pode reparar danos ao sistema nervoso devido a defeitos genéticos, tumores ou feridas no cérebro ou na medula espinhal”, diz ele. “Esperamos um dia poder reparar esses defeitos e fazer com que as células formem conexões funcionais novamente.”
Alicia Santiago, Ph.D., anteriormente do laboratório O'Leary, também contribuiu para o estudo. Salk professor Tony Hunter e Sourav Ghosh, um ex-colega de pós-doutorado no laboratório Hunter, ajudou com experimentos bioquímicos preliminares. O financiamento veio de uma bolsa do National Eye Institute e da Fundação Joseph Alexander.
Para obter informações sobre a comercialização desta tecnologia, entre em contato com Mike White, Ph.D., Office of Technology Management (mwhite@salk.edu, 858-453-4100 x 1703).
O Salk Institute for Biological Studies em La Jolla, Califórnia, é uma organização independente sem fins lucrativos dedicada a descobertas fundamentais nas ciências da vida, à melhoria da saúde humana e ao treinamento de futuras gerações de pesquisadores. Jonas Salk, MD, cuja vacina contra a poliomielite praticamente erradicou a doença incapacitante poliomielite em 1955, abriu o Instituto em 1965 com uma doação de terras da cidade de San Diego e o apoio financeiro da March of Dimes.
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu