
13 de Junho de 2011
Pesquisadores do Salk Institute seguem as reviravoltas da sinalização de esteróides vegetais
Pesquisadores do Salk Institute seguem as reviravoltas da sinalização de esteróides vegetais
La Jolla - Os pássaros fazem isso, as abelhas fazem isso e, para a maioria das coisas biológicas, até as plantas fazem isso. Mas não necessariamente como suas contrapartes animais. Um estudo liderado por cientistas do Salk Institute mostra que um receptor vegetal faz um dos “issos” celulares mais fundamentais – a entrega de um sinal hormonal de fora da célula para o núcleo – de uma maneira radicalmente diferente de seus primos animais. Saber disso pode ajudar na criação de técnicas para acelerar o crescimento das plantas e aumentar a produção agrícola.
Em um estudo publicado na edição online avançada de 12 de junho de 2011 da revista Natureza, equipe liderada por Joanne chory, Ph.D., professor e diretor do Laboratório de Biologia Molecular e Celular de Plantas e pesquisador do Howard Hughes Medical Institute, relata a estrutura tridimensional de um receptor de hormônio esteróide vegetal conhecido como BRI1.
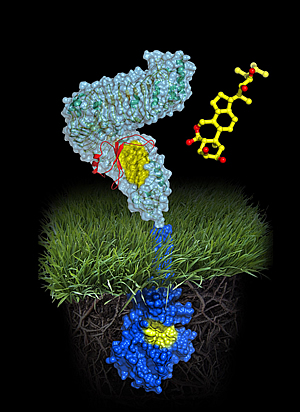
Modelo atômico do receptor de esteróide vegetal BRI1
Uma molécula de brassinolídeo (modelo de fio amarelo) se liga ao domínio extracelular do receptor (em azul claro). A ligação, por fim, causa a fosforilação do domínio citoplasmático da quinase do receptor (em azul escuro), transduzindo assim o sinal através da membrana.
Imagem: Cortesia de Michael Hothorn e Jamie Simon, Salk Institute for Biological Studies
Desde o final dos anos 90, o laboratório Chory realizou estudos de referência revelando que os esteróides vegetais e animais são produzidos por vias semelhantes e que, como os animais, as plantas usam esteróides para aumentar, regular o desenvolvimento sexual e controlar a fisiologia.
O novo estudo encerra esse trabalho com uma análise molecular de um receptor que transduz o sinal do esteroide vegetal. “Nossos estudos genéticos mostraram anteriormente que, ao contrário dos receptores de esteróides animais, que ligam esteróides dentro das células, os receptores de esteróides vegetais são proteínas de membrana, uma classe completamente diferente de proteína”, diz Chory, titular da Howard H. and Maryam R. Newman Chair in Plant Biologia. “Agora que conhecemos os contatos precisos feitos entre o esteróide e seu receptor, podemos propor como o receptor BRI1 funciona.”
O novo trabalho relata a estrutura atômica do BRI1 e a sobrepõe a um primo estrutural distante, a proteína de membrana de mamíferos TLR3, que ativa uma resposta imune inata em camundongos e humanos. A estrutura TLR3 foi determinada em 2005 por Ian Wilson, Ph.D., professor do Departamento de Biologia Molecular e membro do Instituto Skaggs no The Scripps Research Institute (TSRI) e co-autor do estudo atual.
A comparação afirma que, embora um pouco semelhante aos TLRs arquitetonicamente, o domínio de BRI1 que se projeta através da membrana celular e monitora o ambiente extracelular apresenta reviravoltas exclusivas das plantas. "Pensamos que o BRI1 se pareceria com o TLR3, que tem a forma de uma ferradura", diz Michael Hothorn, Ph.D., um pós-doutorando no laboratório Chory e primeiro autor do estudo. “Mas, em vez disso, o BRI1 foi torcido em uma espiral super-helicoidal.”
Para visualizar essas torções, o grupo empregou uma técnica chamada difração de raios-x. Esse método requer que os cientistas primeiro cultivem cristais altamente purificados da “antena” extracelular BRI1 – neste caso, derivados da planta da mostarda Arabidopsis thaliana- e depois bombardear os cristais com raios-x. A maneira como os raios-x saltam ou “difratam” do cristal permite que os pesquisadores construam uma representação tridimensional, semelhante a um Lego, da arquitetura da proteína na presença ou ausência do ativador de esteroides.
Uma previsão foi que as mudanças estruturais causadas pela ligação do esteróide brassinolida poderiam assemelhar-se às alterações de conformação feitas pelo TLR quando este inicia uma resposta imune. “Sabíamos que quando a ferradura TLR3 se liga a um ativador, outra ferradura fica colada em cima dela”, diz Hothorn. “Mas o BRI1 contém um domínio insular que primeiro liga o esteróide à estrutura torcida e depois fornece uma plataforma para uma proteína diferente interagir e retransmitir o sinal.”
Embora o trabalho de proteínas como TLR3 e BRI1 seja alterar os padrões de expressão gênica em resposta a estímulos ambientais, suas diferenças estruturais provavelmente refletem o fato de que esses estímulos são moléculas fundamentalmente diferentes. “Em mamíferos, o TLR3 é um receptor de imunidade inata ativado quando grandes ligantes, como o RNA viral, se ligam a uma área altamente repetida chamada LRR ou domínio de repetição rica em leucina”, diz Wilson. “BRI1 também é uma proteína LRR, mas sua estrutura é altamente especializada para reconhecer e responder a hormônios esteroides vegetais menores”.
“O trabalho estrutural de Michael é o tijolo final na parede”, diz Chory, observando que o BRI1 serve como protótipo para uma grande classe de proteínas semelhantes expressas em plantas. Curiosamente, o BRI1 é uma exceção nessa família: embora seu trabalho seja retransmitir sinais promotores de crescimento, muitos de seus semelhantes realmente estimulam respostas imunes nas plantas, protegendo-as de insetos, vermes ou bactérias. Se os receptores irmãos do BRI1 exibem uma estrutura tão distorcida abre um novo caminho de investigação.
Muitos herbicidas comuns foram projetados para imitar a estrutura dos hormônios vegetais. “Como os brassinosteróides são hormônios, conhecer a estrutura de seu receptor nos permitirá projetar herbicidas racionalmente que possam bloquear a interação entre o hormônio e o receptor”, diz Chory. “Isso nos permitiria manipular a rapidez com que as plantas crescem e o tamanho delas – características importantes em culturas que em breve devem alimentar 10 bilhões de pessoas”.
Também contribuíram para o trabalho Youssef Belkhadir e Tsegaye Dabi do laboratório Chory, Joseph Noel de Salk e Marlene Dreux do The Scripps Research Institute em La Jolla.
O apoio para o trabalho foi do Howard Hughes Medical Institute, National Science Foundation, European Molecular Biology Organization, International Human Frontier Science Program Organization, Philippe Foundation, National Institutes of Health e Skaggs Institute for Chemical Biology no TSRI. .
Sobre o Salk Institute for Biological Studies:
O Salk Institute for Biological Studies é uma das mais proeminentes instituições de pesquisa básica do mundo, onde professores de renome internacional investigam questões fundamentais das ciências da vida em um ambiente único, colaborativo e criativo. Com foco na descoberta e na orientação de futuras gerações de pesquisadores, os cientistas da Salk fazem contribuições inovadoras para nossa compreensão do câncer, envelhecimento, Alzheimer, diabetes e doenças infecciosas, estudando neurociência, genética, biologia celular e vegetal e disciplinas relacionadas.
As realizações do corpo docente foram reconhecidas com inúmeras honras, incluindo Prêmios Nobel e associações na Academia Nacional de Ciências. Fundado em 1960 pelo pioneiro da vacina contra a poliomielite Jonas Salk, MD, o Instituto é uma organização independente sem fins lucrativos e um marco arquitetônico.
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu