
3 de outubro de 2010
LA JOLLA, CA—Assim como os gatos, as células humanas têm um número finito de vidas - uma vez que se dividem um certo número de vezes (felizmente, mais de nove), elas mudam de forma, diminuem o ritmo e, eventualmente, param de se dividir, um fenômeno chamado “celular”. senescência".
Os biólogos sabem que um relógio celular composto de estruturas na extremidade do cromossomo conhecidas como telômeros registra quantas “vidas” uma célula gastou. Até agora, os investigadores ainda não definiram como o tique-taque do relógio sinaliza a aproximação do esquecimento celular.
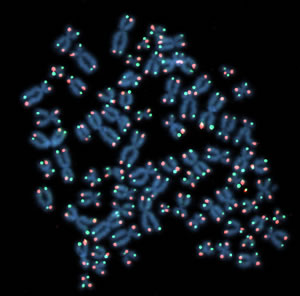
Cada vez que uma célula se divide, as “tampas” protetoras na ponta dos cromossomos (pontos vermelhos e verdes) se desgastam um pouco mais. À medida que os telômeros se desgastam, seu DNA sofre grandes mudanças na forma como é empacotado. Essas mudanças provavelmente desencadeiam o que chamamos de “envelhecimento”.
Imagem: Cortesia do Dr. Jan Karlseder, Salk Institute for Biological Studies
Em um estudo publicado na edição de 3 de outubro de 2010 da Natureza Biologia Estrutural e Molecular, equipe liderada por Jan Karlseder, Ph.D., do Salk Institute for Biological Studies relata que, à medida que as células se tornam senescentes e os telômeros se desgastam, seu DNA sofre grandes mudanças na forma como é empacotado. Essas mudanças provavelmente desencadeiam o que chamamos de “envelhecimento”.
“Antes deste estudo, sabíamos que os telômeros ficam cada vez mais curtos à medida que uma célula se divide e que, quando atingem um comprimento crítico, as células param de se dividir ou morrem”, disse Karlseder, professor associado do Laboratório de Biologia Molecular e Celular. “Algo deve traduzir o sinal local nas extremidades do cromossomo em um grande sinal sentido em todo o núcleo. Mas havia uma grande lacuna no meio.”
Karlseder e seu colega de pós-doutorado Roddy O'Sullivan, Ph.D., começaram a fechar a lacuna comparando os níveis de proteínas chamadas histonas em células jovens - células que se dividiram 30 vezes - com células de "meia-idade tardia", que se dividiram 75 vezes vezes e estavam em declínio para a senescência, que ocorre em 85 divisões. As proteínas histonas ligam os filamentos lineares de DNA e os comprimem em complexos nucleares, chamados coletivamente de cromatina.
Karlseder e O'Sullivan descobriram que as células envelhecidas simplesmente produziam menos proteína histona do que as células jovens. "Ficamos surpresos ao descobrir que os níveis de histonas diminuíram à medida que as células envelheceram", disse O'Sullivan, o primeiro autor do estudo. “Essas proteínas são necessárias em todo o genoma e, portanto, qualquer evento que interrompa essa linha de produção afeta a estabilidade de todo o genoma”.
A equipe então realizou comparações exaustivas de “lapso de tempo” de histonas em células jovens versus envelhecidas e confirmou que diferenças marcantes na abundância e variedade de histonas eram evidentes em cada etapa à medida que as células se moviam através da divisão celular.
O'Sullivan chama o padrão de histonas “padrão” exibido por células jovens de “cromatina feliz e saudável”. Por outro lado, diz ele, as células envelhecidas parecem sofrer estresse à medida que duplicam seus cromossomos em preparação para a divisão celular e têm dificuldade em restaurar um padrão de cromatina “saudável” quando a divisão é concluída.
As comparações de padrões de histonas em células retiradas de seres humanos – uma de 9 versus uma de 92 anos – espelharam dramaticamente as tendências de histonas observadas em linhagens de células. “Esses experimentos importantes sugerem que o que observamos em células cultivadas em um ambiente de laboratório realmente ocorre e é relevante para o envelhecimento de uma população”, diz Karlseder.
A iniciação de doenças associadas ao envelhecimento, como o câncer, é amplamente atribuída ao DNA, ou dano genético. Mas este estudo sugere que o envelhecimento em si é infinitamente complexo: o encurtamento progressivo dos telômeros acelera o envelhecimento cromossômico, alterando a maneira como os genes se entrelaçam com as histonas, as chamadas mudanças “epigenéticas”. A forma como o DNA interage com as histonas tem um enorme impacto sobre a expressão dos genes - daí o intenso interesse atual na relação da paisagem epigenômica com os estados de doença.
Experimentos de resgate nos quais a equipe aumentou cosmeticamente as células envelhecidas confirmaram que os sinais emitidos pela erosão dos telômeros levaram a mudanças epigenéticas. Quando as células envelhecidas foram projetadas para expressar a telomerase, a enzima que restaura e estende os telômeros grossos, essas células rejuvenescidas mostraram níveis de histonas reminiscentes de “cromatina feliz e saudável” e um retorno parcial a um perfil de cromatina jovem.
Para que você não gaste suas economias em esquemas para alongar seus telômeros, cuidado. “O outro lado do alongamento dos telômeros é que você permite que as células cresçam por períodos muito mais longos e podem gerar o que chamamos de células “imortais””, diz Karlseder. “Isso leva você um passo mais perto do desenvolvimento de células cancerígenas.”
Até agora, o laboratório de Karlseder concentrou-se principalmente nas interações entre os telômeros e os mecanismos de reparo do DNA. Este artigo agora os empurra para o campo da epigenética. “Continuaremos a examinar as mudanças epigenéticas nas células em diferentes idades”, diz Karlseder. “Agora queremos determinar se as alterações nas histonas seguem um processo linear ou se ocorrem à medida que envelhecemos”.
Também contribuíram para este trabalho Stuart Schreiber, Ph.D., do Broad Institute of Harvard e MIT e Howard Hughes Medical Institute e seu colega de pós-doutorado Stefan Kubicek, Ph.D.
O estudo foi financiado pelos Institutos Nacionais de Saúde, pela Fundação George E. Hewitt para Pesquisa Médica, pela Fundação de Pesquisa Ernst Schering e pela União Européia.
Sobre o Salk Institute for Biological Studies:
O Salk Institute for Biological Studies é uma das mais proeminentes instituições de pesquisa básica do mundo, onde professores de renome internacional investigam questões fundamentais das ciências da vida em um ambiente único, colaborativo e criativo. Com foco na descoberta e na orientação de futuras gerações de pesquisadores, os cientistas da Salk fazem contribuições inovadoras para nossa compreensão do câncer, envelhecimento, Alzheimer, diabetes e doenças infecciosas, estudando neurociência, genética, biologia celular e vegetal e disciplinas relacionadas.
As realizações do corpo docente foram reconhecidas com inúmeras honras, incluindo Prêmios Nobel e associações na Academia Nacional de Ciências. Fundado em 1960 pelo pioneiro da vacina contra a poliomielite Jonas Salk, MD, o Instituto é uma organização independente sem fins lucrativos e um marco arquitetônico.
O Salk Institute comemora orgulhosamente cinco décadas de excelência científica em pesquisa básica.
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu