
6 de julho de 2022
Visões detalhadas da proteína do HIV podem levar a novos tratamentos contra o vírus
Visões detalhadas da proteína do HIV podem levar a novos tratamentos contra o vírus
LA JOLLA—Entender como o HIV se replica dentro das células é fundamental para o desenvolvimento de novas terapias que podem ajudar quase 40 milhões de pessoas vivendo com HIV em todo o mundo. Agora, uma equipe de cientistas do Salk Institute e da Rutgers University determinou pela primeira vez a estrutura molecular do HIV Pol, uma proteína que desempenha um papel fundamental nos estágios finais da replicação do HIV, ou o processo pelo qual o vírus se propaga. e se espalha pelo corpo. É importante ressaltar que determinar a estrutura da molécula ajuda a responder a perguntas de longa data sobre como a proteína se decompõe para avançar no processo de replicação. A descoberta, publicada na Os avanços da ciência em 6 de julho de 2022, revela uma nova vulnerabilidade no vírus que pode ser alvo de drogas.
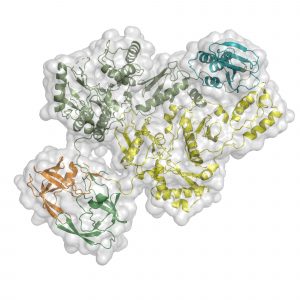
“A estrutura informa a função, e os insights que obtivemos com a visualização da arquitetura molecular do Pol nos dão uma nova compreensão do mecanismo pelo qual o HIV se replica”, diz co-autor sênior Dmitry Lyumkis, professor assistente no Laboratório de Genética e na Cadeira de Desenvolvimento da Fundação Hearst em Salk.
Os cientistas já sabiam que o HIV Pol, uma poliproteína, se divide em três enzimas – uma protease, transcriptase reversa e integrase – que trabalham juntas para montar a forma madura do vírus. A protease desempenha um papel crítico no início desse processo, cortando a molécula para separar os outros componentes. No entanto, não se sabia como a própria protease se liberta, primeiro da maior poliproteína HIV Gag-Pol e depois do HIV Pol, para realizar essa tarefa. O novo artigo sugere que a protease inicia o processo de auto-clivagem ou separação do restante da molécula, auxiliada pela transcriptase reversa e, possivelmente, pela integrase.
“Era conhecido (mas não compreendido) que existe um acoplamento entre essas enzimas antes que o HIV Pol se desfaça. A visualização da estrutura do HIV Pol explica a base desse mecanismo complexo”, diz o co-autor sênior Eddy Arnold, professor do conselho de governadores e professor distinto do Centro de Biotecnologia e Medicina Avançada da Rutgers University.
“O primeiro desafio foi produzir uma versão estável do HIV Pol para que a estrutura pudesse ser analisada, o que nunca havia sido relatado anteriormente”, diz o co-primeiro autor Jerry Joe Harrison, professor sênior da Universidade de Gana.

“Essa era uma peça chave que faltava no quebra-cabeça estrutural do HIV”, acrescenta Arnold.
A equipe usou microscopia eletrônica criogênica, uma técnica de imagem para a qual Lyumkis fez importantes contribuições, para revelar a estrutura tridimensional da molécula da proteína pol do HIV. Isso levou à descoberta de que Pol é um dímero, o que significa que é formado por duas proteínas unidas. A descoberta foi uma surpresa porque outras proteínas virais semelhantes são montagens de proteína única.
O grupo mostrou que nesta estrutura de dois lados, o componente protease de Pol está “frouxamente amarrado” ao componente transcriptase reversa em uma configuração de ligação que mantém a protease ligeiramente flexível.
“É manter a protease à distância, frouxamente, e acreditamos que isso dá à protease um pouco de movimento, o que, por sua vez, permite que ela inicie o corte de poliproteínas que é um pré-requisito para a maturação viral”, diz o co-autor Dario Passos, ex-pesquisador do laboratório de Lyumkis em Salk. “Os tratamentos atuais para o HIV incluem várias classes de inibidores para as três enzimas, e a descoberta também revela uma nova vulnerabilidade que pode ser atacada com medicamentos”.
Os autores dizem que a descoberta abre portas para importantes pesquisas de acompanhamento, incluindo estudos da estrutura da maior e mais complexa poliproteína Gag-Pol, também envolvida na montagem viral, além de examinar mais de perto o papel da integrase na montando a forma madura do vírus HIV durante a replicação.
Outros autores incluíram Jessica F. Bruhn de Salk; Joseph Bauman, Lynda Tuberty e Francesc Xavier Ruiz da Rutgers; e Jeffrey DeStefano da Universidade de Maryland.
O trabalho foi financiado pelos Institutos Nacionais de Saúde, Instituto Internacional de Educação, programa Fulbright, Margaret T. Morris Foundation e Hearst Foundations.
DOI: 10.1126/sciadv.abn9874
JORNAL
Os avanços da ciência
IMERSÃO DE INGLÊS
A estrutura Cryo-EM da poliproteína Pol do HIV-1 fornece informações sobre a maturação do vírion
AUTORES
Jerry Joe EK Harrison, Dario Oliveira Passos, Jessica F. Bruhn, Joseph D. Bauman, Lynda Tuberty, Jeffrey J. DeStefano, Francesc Xavier Ruiz, Dmitry Lyumkis, Eddy Arnold
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu
O Instituto Salk é um instituto de pesquisa independente e sem fins lucrativos, fundado em 1960 por Jonas Salk, criador da primeira vacina segura e eficaz contra a poliomielite. A missão do Instituto é impulsionar pesquisas fundamentais, colaborativas e inovadoras que abordem os desafios mais urgentes da sociedade, incluindo câncer, doença de Alzheimer e vulnerabilidade agrícola. Essa ciência fundamental sustenta todos os esforços translacionais, gerando conhecimento que possibilita o desenvolvimento de novos medicamentos e inovações em todo o mundo.