
22 de janeiro de 2009
La Jolla, CA – Como guardas que controlam o acesso a um condomínio fechado, os complexos de poros nucleares são canais de comunicação que regulam a passagem de proteínas e RNA de e para o núcleo de uma célula. Estudos recentes de pesquisadores do Salk Institute for Biological Studies oferecem novos insights sobre a vida útil dos poros e como sua longevidade afeta sua função.
Suas descobertas, relatadas na edição de 23 de janeiro da Célula, pode fornecer pistas para uma das questões mais duradouras da biologia: como e por que as células envelhecem. Eles também oferecem um novo e promissor caminho de investigação para cientistas que buscam estratégias de intervenção para doenças neurodegenerativas.
“Ainda temos uma compreensão muito pobre dos mecanismos por trás do envelhecimento celular. Já se sabe há algum tempo que o perfil de expressão gênica de uma célula envelhecida muda e, de alguma forma, está ligado a doenças relacionadas à idade, mas ninguém sabe ao certo por quê. Nosso trabalho pode fornecer uma explicação de por que observamos defeitos dependentes da idade nas células”, diz martin hetzer, Ph.D., professor assistente no Laboratório de Biologia Molecular e Celular do Salk.
Formados por 30 proteínas diferentes, os complexos de poros nucleares se montam durante a divisão celular e penetram na membrana que separa o núcleo do citoplasma. O trabalho deles é o controle de tráfego na via mais movimentada do mundo: cada um media aproximadamente 1,000 eventos de transporte por segundo. Como os complexos de poros nucleares são tão essenciais para as células que não se dividem quanto para as que se dividem, a equipe de Salk queria determinar o que acontece com eles ao longo do tempo. Eles se transformam em células que não se dividem ou permanecem no lugar durante toda a vida da célula?
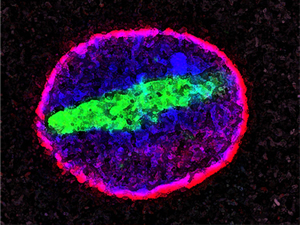
Nas células envelhecidas, uma das proteínas que compõem os poros nucleares é danificada e moléculas que deveriam estar restritas ao citoplasma invadem o núcleo (contorno em vermelho). Em particular, uma proteína chamada tubulina (mostrada em verde), que é estritamente uma proteína citoplasmática, aparece como longos filamentos que cooptam uma grande parte do núcleo.
Imagem: Cortesia do Dr. Maximiliano D'Angelo, Salk Institute for Biological Studies.
Como a maioria das células do nosso corpo não está se dividindo ativamente, a resposta teria implicações para o envelhecimento e doenças relacionadas à idade. “Muitos dos neurônios na área do córtex do cérebro são tão antigos quanto nós; eles não se dividem por muito tempo”, explica Hetzer.
Aproximadamente metade das proteínas no complexo do poro nuclear constituem o andaime central, ou núcleo, enquanto as outras proteínas periféricas se ligam ao andaime. Usando C. elegans, uma minúscula lombriga que, quando adulta, consiste inteiramente de células que não se dividem, Hetzer e seu grupo descobriram que, embora as proteínas periféricas sejam continuamente trocadas, as proteínas que compõem o andaime permanecem no local durante a vida da célula.
Embora as proteínas do andaime sejam detectáveis, seus genes não estão mais ativos. O mesmo ocorreu com neurônios de ratos que não se dividem. “Se as proteínas estão lá, mas as transcrições da informação que fazem a proteína não estão mais lá, elas devem ser muito estáveis”, diz Hetzer, observando que enquanto a maioria das proteínas se transforma em minutos ou horas, as que compõem o andaime no núcleo nuclear O complexo de poros permaneceu intacto durante toda a vida útil de um organismo. “Descobrimos uma das estruturas mais estáveis em nossas células.”
“É um novo conceito”, acrescenta o primeiro autor Maximiliano A. D'Angelo, Ph.D., pesquisador associado do laboratório Hetzer. “Ninguém realmente viu uma estrutura que duraria toda a vida da célula.”
Hetzer e seu grupo então começaram a verificar como essas proteínas estáveis resistem ao longo do tempo. Uma vez que uma das funções do complexo do poro nuclear é estabelecer uma barreira de permeabilidade entre o núcleo e o citoplasma, os pesquisadores desenvolveram um sistema de relatórios que examinaria as barreiras para ver o quão eficientes elas eram em excluir moléculas inapropriadas, assim como os auditores de segurança mantêm o controle. na capacidade dos rastreadores de bagagem do aeroporto de detectar e bloquear o contrabando.
O que eles descobriram foi que, em células envelhecidas, uma das proteínas que compõem a estrutura do andaime é danificada e a barreira de permeabilidade se deteriora; moléculas que deveriam estar restritas ao citoplasma invadem o núcleo.
“Como algumas células vivem por muito tempo, o acúmulo de danos nos complexos de poros nucleares de vida longa pode prejudicar sua função e ter consequências importantes para a homeostase e sobrevivência celular”, diz D'Angelo. “Também pode desempenhar um papel significativo no processo de envelhecimento.”
Em particular, uma proteína chamada tubulina, que é estritamente uma proteína citoplasmática, aparece como longos filamentos que cooptam uma grande parte do núcleo. Por mais de 100 anos, os patologistas estavam cientes desses filamentos, mas suas origens eram desconhecidas. Associados a várias doenças neurodegenerativas, entre elas o Parkinson, os filamentos são encontrados principalmente na substância negra de muitos pacientes com Parkinson, a parte do cérebro envolvida na produção de dopamina e que é afetada pela doença.
A equipe de Hetzer levanta a hipótese de que são os defeitos dependentes da idade nas proteínas do andaime que minam a barreira de permeabilidade nuclear. “Prevemos que, quando a barreira de permeabilidade é prejudicada, as moléculas são perdidas do núcleo ou podem vazar para o núcleo e, assim, alterar os perfis de expressão gênica”, diz Hetzer. “Isso pode ser um mecanismo geral de envelhecimento e fornece uma explicação para a origem desses filamentos, que são conhecidos pelos patologistas há muito tempo”.
Ao encontrar maneiras de prevenir ou reverter o vazamento, os pesquisadores do Salk podem estar no caminho certo para identificar novas abordagens para tratar essas condições desconcertantes, devastadoras e caras.
Além de Hetzer e D'Angelo, a pesquisadora de pós-doutorado Marcela Raices, Ph.D., e o candidato a doutorado Siler H. Panowski, do laboratório do Dr. Andrew Dillin no Salk Institute, contribuíram para este estudo. A pesquisa foi realizada com financiamento do NIH.
O Salk Institute for Biological Studies em La Jolla, Califórnia, é uma organização independente sem fins lucrativos dedicada a descobertas fundamentais nas ciências da vida, à melhoria da saúde humana e ao treinamento de futuras gerações de pesquisadores. Jonas Salk, MD, cuja vacina contra a poliomielite praticamente erradicou a doença incapacitante poliomielite em 1955, abriu o Instituto em 1965 com uma doação de terras da cidade de San Diego e o apoio financeiro da March of Dimes.
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu