
2021 年 4 月 15 日
ソークの科学者は、脳の免疫細胞がアルツハイマー病の防御としていくつかのプラークを形成していることを発見し、新たな治療の方向性を示唆している
ソークの科学者は、脳の免疫細胞がアルツハイマー病の防御としていくつかのプラークを形成していることを発見し、新たな治療の方向性を示唆している
ラホヤ—アルツハイマー病(AD)の特徴的な特徴のXNUMXつは、脳内にアミロイドベータ斑が蓄積することである。 アルツハイマー病を治療するために設計されたほとんどの治療法はこれらのプラークを標的としていますが、臨床試験ではほとんど失敗しています。 ソークの科学者らによる新しい研究は、蔓延している一種のプラークの起源についての従来の見解を覆し、治療が成功しない理由を示しています。
従来の見解では、ミクログリアと呼ばれる脳のゴミを除去する免疫細胞がプラークを「食べる」ことでプラークの増殖を抑制すると考えられています。 ソークの科学者らは代わりに、ミクログリアが高密度コアプラークの形成を促進し、この作用がかすかなプラーク物質をニューロンから一掃し、そこで細胞死を引き起こすことを示した。 に発表された研究は、 自然免疫学 15 年 2021 月 XNUMX 日の論文では、高密度コア プラークは保護的な役割を果たしているため、これを破壊する治療は良いことよりも害を及ぼす可能性があることを示唆しています。
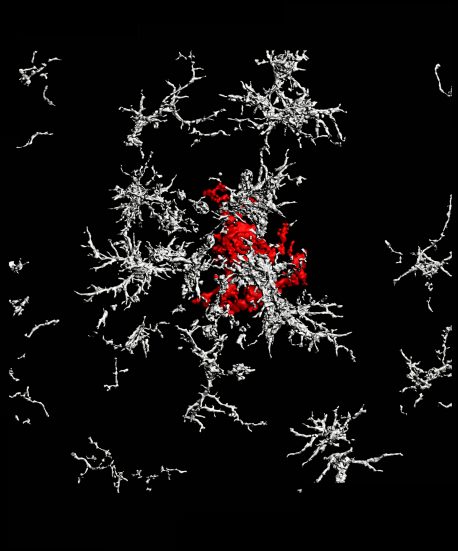
「私たちは、高密度コアプラークが自然発生的に形成されるものではないことを示しています。 私たちは、それらは防御機構としてミクログリアによって構築されていると考えているので、放っておくのが最善かもしれません」と述べています。 グレッグ・レムケ、ソーク分子神経生物学研究所の教授。 「主な臨床効果が高密度コアプラークの形成を減らすことである抗体をFDAに承認させるためにさまざまな取り組みが行われていますが、私たちはプラークの破壊がより大きなダメージを与えている可能性があると主張しています。」
アルツハイマー病は、記憶喪失、思考障害、行動の変化を引き起こす神経疾患であり、年齢とともに悪化します。 この病気は、脳細胞間で異常なタンパク質が凝集して特徴的なプラークを形成し、細胞を生かし続ける活動を妨げることによって引き起こされるようです。
プラークには多数の形態がありますが、最も一般的な XNUMX つは「びまん性」と「密なコア」として特徴付けられます。 びまん性プラークは、緩く組織化された不定形の雲です。 高密度コアプラークは、ハローに囲まれたコンパクトな中心を持っています。 科学者は一般に、どちらのタイプのプラークも、アミロイド前駆体タンパク質(APP)と呼ばれる前駆体分子の過剰産生によって自然発生的に形成されると考えてきました。
しかし、新しい研究によると、細胞浄化の一環として、びまん性のアミロイドベータ線維から高密度コアプラークを形成するのは実際にはミクログリアであるという。
これは、 2016年の発見 レムケ研究室は、脳細胞が死ぬと脂肪分子が細胞の内側から外側に反転し、「私は死んだ、私を食べろ」という信号を送ることを突き止めた。 ミクログリアは、TAM 受容体と呼ばれる表面タンパク質を介して、Gas6 と呼ばれる中間分子の助けを借りて、死んだ細胞を飲み込む、つまり「食べる」のです。 TAM 受容体と Gas6 がなければ、ミクログリアは死んだ細胞に接続してそれらを消費することができません。
研究チームの現在の研究は、イートミーシグナルとGas6を示すのは死んだ細胞だけではないことを示している。アルツハイマー病に蔓延するアミロイド斑も同様である。 研究者らは動物モデルを用いて、TAM受容体を持つミクログリアがイートミーシグナルとGas6を介してアミロイド斑を食べることを初めて実験的に実証することができた。 TAM受容体を欠くように操作されたマウスでは、ミクログリアはこの機能を果たすことができなかった。
さらに深く掘り下げ、ライブイメージングを使用して高密度コアプラークを追跡しました。 非常に驚いたことに、研究チームは、ミクログリア細胞がびまん性プラークを食べた後、飲み込まれたアミロイドベータを高酸性の区画に移動させ、それを高度に圧縮された凝集体に変換し、その後、高密度コアプラークに移動させることを発見した。 研究者らは、これが有益なメカニズムであり、びまん性プラークを高密度コアプラークに組織化し、細胞間環境から破片を除去するものであると提案している。

「私たちの研究は、高密度コアプラークが少なくなると、より有害な影響が生じるようであることを示しているようです」と、この論文の筆頭著者であるYoutong Huang氏は述べています。 「よりびまん性のプラークでは、神経損傷の代用となる異栄養性神経突起が豊富に存在します。 どの形態のプラークが多かれ少なかれ有害であるかについて明確な臨床上の決定はないと思いますが、私たちの研究を通じて、高密度コアプラークはもう少し良性であることがわかったようです。」
彼らの発見は、ミクログリア上のTAM受容体の発現を促進してデンスコアプラークの形成を促進するなど、アルツハイマー病の治療法を開発する新しい方法を示唆している。 研究チームは、ミクログリアのTAM受容体の活性を高めることでアルツハイマー病の影響が緩和されるかどうかを確認するための認知研究を実施したいと考えている。
フランソワーズ・ジロー・ソーク委員長を務めるレムケ氏は、現在のほとんどのアルツハイマー病治療薬臨床試験の失敗率は終わりに近づいていると信じている。 「一部の人々は、高密度コアプラークを除去する試験が相対的に失敗したことは、アミロイドベータが脳に悪影響を与えるという考えを否定していると言っています」とレムケ氏は言う。 「しかし、私たちはアミロイドベータが依然として明らかに悪であると主張します。 ただ、高密度コアプラークが悪いのかどうかを考えなければなりません。」
レムケ教授は、アルツハイマー病の治療法を模索している科学者たちは、コアが密集したプラークを破壊することに重点を置くのをやめ、そもそもアミロイドベータの生成を減らす治療法か、アミロイドベータの外への輸送を促進する治療法のどちらかを検討し始めるべきだと示唆している。完全に脳の。
この研究の他の著者は、Kaisa E. Happonen、Patrick G. Burrola、Carolyn O'Connor、Nasun Hah、Ling Huang、およびソークの Axel Nimmerjahn です。
この研究は米国国立衛生研究所からの助成金によって支援されました。 アルツハイマー病治療基金。 アルツハイマー病研究トラストのコイン。 レオナ・M・ヘルムズリーおよびハリー・B・ヘルムスリー慈善信託。 カリフォルニア大学サンディエゴ・ゲッデル校のマルグリット・フォークト学長、HAおよびメアリー・K・チャップマン慈善信託の大学院生フェローシップ。 アンダーソン氏、NOMIS 財団およびスウェーデン・アメリカ財団博士研究員フェローシップ。
DOI: 10.1038/s41590-021-00913-5
ジャーナル
自然免疫学
作者
ユートン・ファン、カイサ・E・ハッポネン、パトリック・G・バローラ、キャロリン・オコナー、ナスン・ハー、リン・ファン、アクセル・ニンマージャーン、グレッグ・レムケ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。