
2016 年 4 月 6 日
ソークの科学者らは、免疫受容体が死んだ脳細胞や機能不全の脳細胞をどのように除去するのか、また免疫受容体がどのようにして神経変性疾患治療の標的となり得るのかを明らかにしている
ソークの科学者らは、免疫受容体が死んだ脳細胞や機能不全の脳細胞をどのように除去するのか、また免疫受容体がどのようにして神経変性疾患治療の標的となり得るのかを明らかにしている
ラホヤ—思春期までに、あなたの脳には、残りの人生で維持されるニューロンのほとんどがすでに含まれています。 しかし、いくつかの地域では新しい神経細胞が成長し続けており、死んだ細胞や機能不全の細胞を除去して脳の安全を保つ特殊な免疫細胞である細胞番兵の働きが必要です。
今回、ソークの科学者らは、瀕死のニューロンと死んだニューロンの両方が驚くべき範囲で除去されることを明らかにし、このプロセスの鍵となる特定の細胞スイッチを特定した。 作品の詳細は、 自然 4月6、2016に。
「脳内の免疫細胞の受容体が、健康な状態と損傷した状態の両方に不可欠であることを発見しました」と彼は言います。 グレッグ・レムケ、この研究の上級著者であり、分子神経生物学のソーク教授であり、フランソワーズ・ジロー=ソーク委員長の保持者である。 「これらの受容体は、神経変性疾患や炎症関連疾患の潜在的な治療標的となる可能性があります。 パーキンソン病に設立された地域オフィスに加えて、さらにローカルカスタマーサポートを提供できるようになります。」
こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
100年前、レムケ研究室は、免疫細胞がTAM受容体と呼ばれる重要な分子を発現していることを発見し、それ以来、多くの研究室で自己免疫およびがん研究の焦点となっている。 Mer と Axl と呼ばれる XNUMX つの TAM 受容体は、マクロファージと呼ばれる免疫細胞がガベージコレクターとして機能するのを助け、人体の中で毎日生成される XNUMX 億個を超える死んだ細胞を識別して消費します。
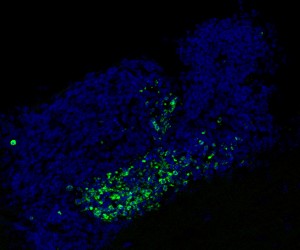
今回の研究で研究チームは、マーとアクセルが脳内で同じ働きをしているかどうかを尋ねた。 ミクログリアと呼ばれる特殊な中枢神経系マクロファージは、脳内の細胞の約 10% を構成し、病原体を検出し、反応し、破壊します。 研究者らは、それ以外は健康なマウスのミクログリアからAxlとMerを除去した。 驚いたことに、この XNUMX つの受容体の欠如により、死んだ細胞が大量に積み重なることになるが、脳のいたるところに存在するわけではないことが判明した。 細胞の死骸は、新しいニューロンの生成(神経新生)が観察される小さな領域でのみ見られました。
多くの細胞は成人の神経新生中に通常は死にますが、それらはすぐにミクログリアによって食べられます。 「正常な脳で死んだ細胞をXNUMXつも検出することは非常に困難です。なぜなら、死んだ細胞はミクログリアによって非常に効率的に認識され除去されるからです」と、この論文の共同筆頭著者で元ソーク研究員のパキ・G・トラベス氏は言う。 「しかし、MerとAxlを欠くマウスの神経形成領域では、そのような細胞が多数検出されました。」
研究者らが、MerとAxlを欠いたマウスのミクログリアで新たに成長するニューロンにタグを付けることでこのプロセスをさらに詳しく調べたところ、別の興味深いことに気づきました。 アクセルとマーがいないと、嗅球、つまり匂い中枢に移動する新しいニューロンが劇的に増加しました。 TAM受容体を欠損したマウスは、正常なマウスよりも嗅球で新たに生成される細胞が70パーセント増加していた。
レムケ氏によれば、この未確認の新しい神経成長がマウスの嗅覚にどのように、そしてどの程度影響を与えるのかはまだ不明だが、それは研究室が調査する領域であるという。 しかし、受容体が存在しないにもかかわらず、より多くの生きた神経細胞が嗅球に移動できたという事実は、MerとAxlには死んだ細胞を除去する以外に別の役割があることを示唆しており、実際には生きているが機能が損なわれた細胞も標的にしている可能性がある。 。

こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
「神経原性領域における細胞死のかなりの部分は、細胞の本質的な死によるものではなく、むしろミクログリア自体の結果であり、飲み込まれて細胞の一部を死滅させているようです」とレムケ氏は言う。 「言い換えれば、これらの生まれたばかりのニューロン前駆細胞の一部は、実際に生きたまま食べられているのです。」
これは脳が健康であれば必ずしも悪いことではない、とレムケ氏は付け加えた。 脳は使用できる量を超えるニューロンを生成し、不要な細胞を切り取って戻します。 しかし、炎症を起こしている脳や病気の脳では、生きている細胞の破壊が逆効果になる可能性があります。
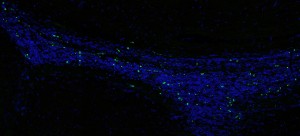
Lemke研究室は、病気におけるTAM受容体の役割を理解するために、もうXNUMXつの一連の実験を行いました。彼らは、パーキンソン病のマウスモデルにおけるAxlとMerの活性を調べました。 このモデルは、脳のゆっくりとした変性をもたらす病気の遺伝型に存在するヒトタンパク質を生成します。 研究チームは、Axlの増加が組織の炎症の信頼できる指標であることを示す他の研究と一致して、この設定ではAxlがはるかに活性であることを確認しました。
こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
しかし、パーキンソン病マウスからアクセルとマーを取り出したとき、研究者たちは驚きを隠せなかった。 この病気はあるがミクログリアが正常なマウスと比べて、アクセルとマーを欠損したマウスの方が症状が悪化するどころか、実際に長生きしたのです。 これは、Axl と Mer が病気で機能不全に陥ったニューロンを標的にして破壊するためである可能性があります。 病気が存在すると、機能不全に陥ったニューロンが通常より多く存在する可能性があるため、Axl と Mer が過剰なニューロンの破壊を促し、事実上病気の進行を早めている可能性があります。
「アクセルとメールを操作することで、動物モデルで病気の経過を変えることができるようです」と、論文の共同筆頭著者で元ソーク研究員のローレンス・フルゴー氏は言う。 研究チームは、TAM受容体の調節がミクログリアが関与する神経変性疾患の有効な治療法となり得るかどうかを判断するには、さらなる研究を行う必要があると警告している。
この論文の他の研究者は、ソーク研究所のユスフ・トゥファイル、ウンベルト・レアル=ベイリー、エリン・D・ルー、パトリック・G・ブローラ、ペリー・キャラウェイ、アンナ・ザゴルスカ、アクセル・ニマージャーンであった。 とイェール大学医学部のカーラ・V・ロスリン。
この作品を支援したのは、 国立衛生研究所 レオナM.とハリーB.ヘルムズリー慈善信託 ハワードヒューズメディカルインスティチュート ノミス, HN とフランシス C. バーガー、フリッツ・B・バーンズ、HKT、 待って, リタ・アレン, ハースト 基礎
ジャーナル
自然
作者
ローレンス・フルジョー、パキ・G・トラベス、ユスフ・トゥファイル、ウンベルト・レアル=ベイリー、エリン・D・ルー、パトリック・G・ブローラ、ペリー・キャラウェイ、アンナ・ザグルスカ、カーラ・V・ロスリン、アクセル・ニンマージャーン、グレッグ・レムケ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。