
2020 年 6 月 11 日
ソークとエール大学のインフルエンザ研究は、新型コロナウイルス感染症や他の肺疾患のワクチンに役立つ可能性がある
ソークとエール大学のインフルエンザ研究は、新型コロナウイルス感染症や他の肺疾患のワクチンに役立つ可能性がある
【ラホヤ】新型コロナウイルス感染症による重大な損傷部位は肺である。 肺の免疫細胞がウイルス感染にどのように反応しているかを理解できれば、科学者がワクチンを開発するのに役立つ可能性がある。
現在、ソーク教授率いる研究者チームは、 スーザン・ケック は、肺の長期免疫を担う細胞が、これまで考えられていたよりも簡単に活性化できることを発見しました。 この洞察は、 実験医学ジャーナル 11年2020月XNUMX日に発表されたワクチンは、インフルエンザと新型コロナウイルスに対する万能ワクチンの開発に役立つ可能性がある。
「私たちの肺の中には、特定のウイルスを認識し、ウイルスに再び遭遇した場合に再感染から私たちを守る長命のキラーT細胞が存在します。 私たちの結果は、これらの細胞が再感染時にウイルスを「認識」し、迅速な免疫を提供する仕組みを解明しました」と、ソークの免疫生物学および微生物病原性の NOMIS センター所長のケーチ氏は述べています。 「また、コロナウイルスに関連する長期免疫を理解するのにも役立つかもしれません。」
私たちが初めて細菌やインフルエンザなどのウイルスにさらされると、キラー T 細胞として知られる免疫細胞の一種が、感染した細胞を破壊して病気の蔓延を防ぎます。 病原体が除去されると、これらの経験豊富なキラー T 細胞 (キラー「メモリー」T 細胞とも呼ばれる) は体内に長期的に残り、以前の侵入者を「記憶」します。 これらのキラーメモリー T 細胞により、私たちの免疫系は二次攻撃により迅速に反応し、侵入者に対する長期的な防御免疫を効果的に提供できるようになります。これはワクチン接種の背後にある基本的な概念です。
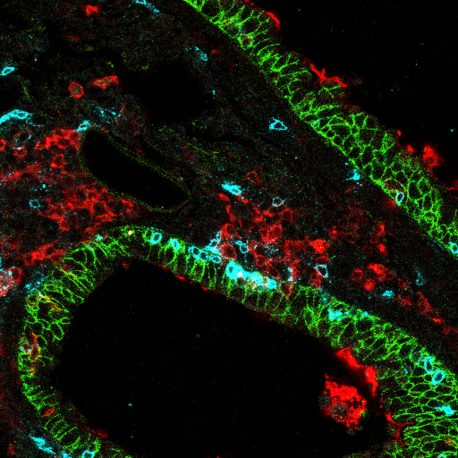
こちらをクリックしてください 高解像度画像の場合。
クレジット:Salk Institute
科学者は、キラーメモリー T 細胞がリンパ器官 (リンパ節など) でどのように活性化されるかについて多くのことを知っています。 樹状細胞と呼ばれる免疫メッセンジャー細胞は、ハンドラーが猟犬に香りを提示するのと同じように、キラーメモリー T 細胞にウイルスの断片を提示してキラー機能をライセンスします。
しかし、これまでの研究では、肺などの重要な臓器におけるこの相互作用は調査されていませんでした。 肺はインフルエンザやコロナウイルスなどの病原体が頻繁に侵入する場所であるため、研究チームは、この長年の定説が肺に存在するキラーメモリーT細胞に当てはまるかどうかを確認することに着手した。
ケチ氏と、この論文の筆頭著者で当時大学院生だったジュン・シオン・ロー氏は、ウイルスの二度目の攻撃に対抗するためにキラーメモリーT細胞を再活性化するには樹状細胞が必要だろうと推測した。 そこで、マウスのさまざまな種類のメッセンジャー細胞を一度に XNUMX つずつ削除して、キラーメモリー T 細胞がインフルエンザの XNUMX 回目の感染を認識するかどうかを確認しました。 研究者らは緑色蛍光レポータータンパク質を使用して、キラーメモリーT細胞がウイルスを認識した場合に光らせるようにした。 しかし、研究者らが特定の細胞型を削除するたびに、肺のキラーメモリーT細胞は輝き続けた。
「最初は、実験がうまくいっていないように見えたので、結果は残念なものでした。 肺のキラーメモリーT細胞は、多くの異なるメッセンジャー細胞タイプを削除した後もウイルスを認識し続けた」と、現在スイスのスヴィッツェラ・イタリア大学生物医学研究所(IRB)の博士研究員であるロー氏は言う。 。 「すぐに、肺に常駐するこれらのキラーメモリー T 細胞は、単一タイプのメッセンジャー細胞に依存していないため、特別なものであることがわかりました。 その代わりに、肺上皮細胞のような非免疫細胞を含む、さまざまな異なるメッセンジャー細胞を介してインフルエンザの二次感染を「観察」することができたのは、非常に興味深い発見でした。」

こちらをクリックしてください 高解像度画像の場合。
クレジット:Salk Institute
対照的に、研究者らがリンパ節(感染時に腫れる腺)のキラーメモリーT細胞を調べたところ、キラーメモリーT細胞がウイルスのXNUMX回目の攻撃を認識するために樹状細胞を必要とすることが判明した。 これは、キラーメモリー T 細胞の解剖学的位置がキラーメモリー T 細胞の再活性化方法を決定することを示唆しており、キラーメモリー T 細胞が再活性化するには樹状細胞を必要とするという長年の定説に疑問を呈します。 この結果は、キラーメモリー T 細胞活性化のパラダイムを再構築するのに役立ちます。
肺常駐キラーメモリー T 細胞は、病原体の侵入部位でほぼあらゆる種類の細胞によってすぐに再活性化される可能性があるため、これらの肺常在キラーメモリー T 細胞を生成できるワクチンを特定することは、肺のウイルス感染に対する優れた免疫にとって重要であると考えられます。 。
「私たちはこの知識を次の研究に取り入れ、コロナウイルス感染後に肺常在キラーメモリーT細胞が形成されるかどうかを調べる予定です」とNOMIS議長のケック氏は言う。 「すべての感染症がキラーメモリーT細胞を誘導するわけではないため、これらの細胞がコロナウイルス感染後に形成されるかどうか、そしてそれらが将来のコロナウイルス感染症から防御できるかどうかを判断する予定です。」
他の著者には、ソークのヤグラム・ファルサコグルが含まれる。 イェール大学医学部のエセン・セフィク、クリスチャン・CD・ハーマン、ルアイドリ・ジャクソン、ジャスティン・シャイアー、シャオドン・ジャン、リチャード・A・フラベル。 アルゼンチンのコルドバ国立大学のマリア・カロリーナ・アメスクア・ヴェセリー氏。 ストーニーブルック大学のジョセフ・B・ケリー氏とコネチカット大学ヘルスセンターのリンダ・S・コーリー氏。
この研究は NOMIS 財団によって支援されました。 国立衛生研究所 (R01 AI123864、R37 AI066232、S10 OD020142、P30 CA106359-39)。 A*STAR 国立科学奨学金博士号; スイス国立科学財団早期ポスドクモビリティフェローシップ (P2BEP3_178444); ジョージ・E・ヒューイット財団のフェローシップ。 ハワード・ヒューズ医学研究所。 エール大学リサーチコンピューティングセンター。 イェール大学ゲノム解析センター。 およびソーク生物学研究所のウェイト先進バイオフォトニクスコア。
DOI: doi.org/10.1084/jem.20192291
ジャーナル
実験医学ジャーナル
作者
Jun Siong Low、Yagmur Farsakoglu、Maria Carolina Amezcua Vesely、Esen Sefik、Joseph B. Kelly、Christian CD Harman、Ruaidhri Jackson、Justin Shyer、Xiaodong Jiang、Linda S. Cauley、Richard A. Flavell、Susan M. Kaech。
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。