
2016 年 8 月 10 日
まれな遺伝的疾患により、非常に社交的な性格を持つ人が生まれるが、研究により自閉症やその他の社会的障害を持つ人の生物学や行動も解明される可能性がある
ラホヤ—分子遺伝学、幹細胞、脳と行動の両方の科学にわたる研究で、研究者らは カリフォルニア大学サンディエゴ校 ソーク研究所とソーク研究所は、人間の社会脳の根底にある神経生物学への新たな洞察を提供する可能性のある、希少な遺伝性疾患の神経発達モデルを作成しました。
この調査結果は、10月XNUMX日のオンライン版に掲載されます。 自然.
科学者が調査した ウィリアムズ症候群 WS、脳内に推定 25 個ある遺伝子のうち、第 7 染色体上の連続する 30,000 個の遺伝子の 10,000 コピーの欠失によって引き起こされるまれな遺伝的状態。 WSは世界中で20,000人にXNUMX人が罹患しており、アメリカ人では推定XNUMX人が罹患しています。 この状態は、性別や文化を問わず等しく発生します。
クリックして表示
クリックしてウィリアムズ症候群に関するその他のリソースを表示します»
ウィリアムズ症候群は、特定の心臓欠陥だけでなく、多くの医学的問題を引き起こします。 欠失のある人は通常、小さく上向きの鼻、広い口、ふっくらした唇、小さな顎といった特徴的な顔を示し、歯や整形外科的な問題を抱えている場合もあります。 神経学的には、発達に遅れがあり、重度の空間障害を伴いますが、言語使用と顔の処理においては相対的に優れています。
「興味深い側面は、典型的な過社会的素質です」と研究の共著者は述べた ウルスラ・ベルージ、EdDは、ソーク大学の認知神経科学研究室の所長であり、カリフォルニア大学サンディエゴ校の非常勤教授であり、長年ウィリアムズ症候群を研究してきました。 「ウィリアムズ症候群の欠失を持つ人は、過度に友好的で、過度に信頼し、見知らぬ人に惹かれますが、不安を感じる傾向があります。」
しかしベルージ氏は、遺伝学がウィリアムズ症候群の行動面とどのように関連しているかは明らかではないと述べた。 「この病気の人体モデルは科学的なギャップを埋め、この病気の背後にあるメカニズムを理解するのに役立つ可能性があります。 WS は、レベルを越えることができるエレガントなモデルです」と彼女は言いました。
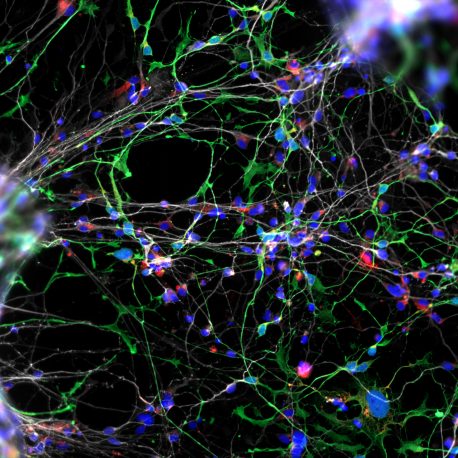
こちらをクリックしてください 高解像度画像の場合。
クレジット: カリフォルニア大学サンディエゴ校
共著者でソーク教授 ラスティ・ゲージ 「最先端の幹細胞技術を使用することで、ウィリアムズ症候群の遺伝的プロファイルを持つ細胞の挙動を直接観察することが初めて可能になりました。 この学際的な研究は、この注目すべき行動症候群に対する潜在的な新しい治療法を示唆するだけでなく、社会的相互作用の根底にある基本的な生物学的プロセスをより深く理解するのにも役立つ可能性があります。」
研究の上級著者 アリソン・ムオトリ博士カリフォルニア大学サンディエゴ医学部の小児科および細胞・分子医学の准教授である彼は、WSに興味をそそられました。なぜなら、その症状が、社交性と言語能力の低下を特徴とする自閉症に焦点を当てた彼の通常の研究とは大きく異なるからです。
「遺伝的欠陥、つまり染色体のXNUMX本の小さな欠失が、どのようにして私たちをより友好的に、より共感的にし、違いをより受け入れることができるようになるのかということに興味を持ちました」とムオトリさんは語った。
近年、ムオトリらは、自閉症児の捨てられた乳歯から採取した再プログラムされた人工多能性幹細胞(iPSC)を用いて、自閉症の体外細胞モデルを作成しており、この研究は「歯の妖精プロジェクト」と呼ばれている。 彼らはここでもまた同じことをした。
研究チームはウィリアムズ症候群の幼児から提供された歯から歯髄細胞を抽出することから始めた。 この細胞は、皿の中の人間の脳の発達中の皮質に似た機能的な神経ネットワークを形成できる神経前駆細胞になるように再プログラムされた。
「私たちは、WS神経前駆細胞が高レベルの細胞死のために増殖できないことを発見しました」とムオトリ氏は述べた。 「そして、前駆細胞の複製が低下した結果、ウィリアムズ症候群の脳は皮質表面積が減少しました。」
培養されたWSニューロンは独特の形態を持っています。 それらは、定型的に発達している個体に由来するニューロンよりも樹枝状(多くの樹状枝を有する樹状)である。 「機能レベルでは、彼らは予想以上に多くのシナプスや他のニューロンへの接続を行っています」とムオトリ氏は言う。 「それはウィリアムズ症候群の超社会的側面と集団的な人間の脳の根底にある可能性があり、社会的脳に影響を与える自閉症やその他の障害についての洞察を与える可能性があります。」
ニューロンの形態は、カリフォルニア大学サンディエゴ校人類学部の共同上級著者であり教授であるカテリーナ・セメンデフェリ博士によって、ウィリアムズ症候群の死後脳組織の希少なコレクションを使用して確認されました。 「XNUMXつの印象的な観察は、ウィリアムズ症候群患者の皮質ニューロンが対照(通常は同年齢の発育中の子供)よりも複雑であるということでした。 おそらくウィリアムズ症候群の妊娠中に現れた形態的変化は、出生後も維持されます。」
ムオトリ教授は、この研究は、他のモデルからのデータを単に複製するのではなく、iPSC と脳イン・ア・ディッシュ技術を使用して疾患プロセスに関する新たな洞察を生み出す最初の取り組みの XNUMX つであると述べた。
しかしそれを超えて、ウィリアムズ症候群の研究は、人間を社会的存在たらしめる理由、つまり人類の進化における重要な発展を説明するのに役立つかもしれないと彼は信じています。 「私たちを協力的な種族にしてくれたのは、私たちの社会的な力でした。詩、音楽、テクノロジーを生み出すことで環境を劇的に変えることができるのです」とムオトリ氏は語った。
共著者には、カリフォルニア大学サンディエゴ校の Thanathom Chailangkarn およびタイ、パトゥムターニーの遺伝子工学およびバイオテクノロジー国立センターが含まれます。 Cleber A. Trujillo、Beatriz C. Freitas、Timothy T. Brown、Branka Hrvoj-Mihic、Lisa Stefanacci、M. Collin Ard、Kari L. Hanson、Sarah Romero、Anders M. Dale、カリフォルニア大学サンディエゴ校。 ロベルト・H・ヘライ、カリフォルニア大学サンディエゴ校、ブラジルのパラナ・カトリカ大学ポンティフィカ大学。 Diana X. Yu、Maria CN Marchetto、Cedric Bardy、Lauren McHenry、Anna Järvinen、Yvonne M. Searcy、Michelle DeWitt、Wenny Wong、Philip Lai、Fred Gage、ソーク生物学研究所。 ボブ・ジェイコブス、コロラド大学。 ユタ大学のリー・ダイ氏とジュリー・R・コレンバーグ氏。
この研究への資金援助の一部は、 カリフォルニア再生医療研究所 国立衛生研究所, ナルサド、エングマン財団、 JPB財団, ヘルムスリー財団 そしてタイ王室政府。
カリフォルニア大学サンディエゴ校が提供するコンテンツ. UCSDのプレスリリースはここをクリックしてください.
ジャーナル
自然
TITLE
作者
タナトム・チャイランカーン、クレバー・A・トルヒーヨ、ベアトリス・C・フレイタス、ブランカ・フルヴォイ=ミヒッチ、ロベルト・H・ヘライ、ダイアナ・X・ユー、ティモシー・T・ブラウン、マリア・C・マルケット、セドリック・バーディ、ローレン・マクヘンリー、リサ・ステファナッチ、アンナ・ヤーヴィネン、イヴォンヌ・M・サーシー、ミシェル・デウィット、ウェニー・ウォン、フィリップ・ライ、M・コリン・アード、カリ・L・ハンソン、サラ・ロメロ、ボブ・ジェイコブス、アンダース・M・デール、リー・ダイ、ジュリー・R・コレンバーグ、フレッド・H・ゲージ、ウルスラ・ベルーギ、エリック・ハルグレン、カテリーナ・セメンデフェリ、アリソン・R・ムオトリ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。