
2018 年 5 月 3 日
ソーク研究者らは、脳の海馬で見つかった複数の種類の細胞を使用して、統合失調症において細胞間の接続がどのようにおかしくなるかをモデル化した。
ソーク研究者らは、脳の海馬で見つかった複数の種類の細胞を使用して、統合失調症において細胞間の接続がどのようにおかしくなるかをモデル化した。
ラホヤ—幹細胞から複数の種類のニューロンを作成し、それらがどのように相互作用するかを観察することにより、ソークの科学者らは、実験室で脳細胞間の接続を研究する新しい方法を開発した。 研究チームは、脳の部分モデルを生成するこの技術を使用して、統合失調症患者のニューロン間のコミュニケーションがどのように変化するかを示した。 作品に登場したのは、 細胞幹細胞 月3、2018に。
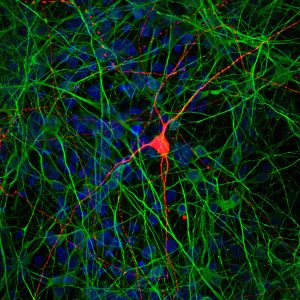
こちらをクリックしてください 高解像度画像の場合。
クレジット:Salk Institute
「多くの精神疾患では、細胞間の接続に機能不全の証拠がある」と上級著者は言う ラスティ・ゲージ、ソーク遺伝学研究所の教授。 「しかし、これまで研究室で人間のニューロン間の機能的接続を研究することは非常に困難でした。」
以前は、統合失調症のような疾患の根底にある分子機構を研究したい研究者は、通常、一度に XNUMX 種類の脳細胞に焦点を当て、疾患細胞内で遺伝子やタンパク質のレベルが変化しているかどうか、あるいはシグナル伝達経路が調節不全になっているように見えるかどうかを研究していました。 。
ゲージ氏のチームは以前、ヒト幹細胞を使用して歯状回(DG)細胞(多くの精神疾患に関与している脳の海馬の重要なニューロン)を作製する方法を開発していた。 新しい研究では、そのアプローチを応用して幹細胞を別の発生経路に誘導し、CA3錐体ニューロン(海馬のDGニューロンから信号を受け取る細胞)を作成した。 研究チームは、得られたCA3ニューロンが多様な分子的アイデンティティを持っていることを示した。
「我々が取得したのは 3 種類の CAXNUMX ニューロンだけではありませんでした」と、この論文の共同責任著者である研究員アニンディタ サーカール氏は述べています。 「人間の脳内で見られる混合物をほぼ再現した混合物が得られました。」 さらに、研究チームが細胞をマウスの海馬に移植すると、細胞はすでにそこにあるニューロンのネットワークに統合されました。
新しい脳細胞が真の CA3 ニューロンであることが確認されたため、研究者らはそれらを DG ニューロンと混合し、細胞がどのように相互作用するかを研究し始めました。 研究者らは、狂犬病ウイルスがニューロン接続を追跡する性質に依存するウイルストレースと呼ばれる方法を使用して、CA3ニューロンが他のCA3ニューロンおよびDGニューロンの両方と物理的な接続を形成していることを示した。

こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
最後に、研究チームは、これらの接続されたニューロンを病気の研究に使用できるかどうかをテストしたいと考えました。 そこで彼らは手順を繰り返し、今度は 3 つの異なる細胞セット (統合失調症患者からの 3 セットと健康な対照からの 3 セット) から始めました。 彼らは細胞を幹細胞の形態に戻すよう誘導し、DG ニューロンと CAXNUMX ニューロンの両方を生成しました。 ニューロンが成熟するにつれて、統合失調症患者から生成されたCAXNUMXニューロンの活動のスパイクが減少することが研究者らは発見した。 DG ニューロンと CAXNUMX ニューロンを混合した場合も同様の結果が得られました。統合失調症グループのニューロンでは活動パターンが弱まり、ニューロンのセット間のシグナル伝達が減少しました。
「海馬とDG細胞が統合失調症の影響を受けているという証拠があります」とサーカー氏は言う。 「したがって、DG 細胞が影響を受けると、CA3 細胞に送信するシグナルが減少することは理にかなっています。」
将来的には、ゲージ氏のグループは、CA1 ニューロンなどの細胞タイプをモデルに追加したいと考えています。 彼らはまた、他の病気で神経結合がどのように変化するのかも研究したいと考えています。
「これは幹細胞を用いた疾患モデリングの次のステップだと思います」とサーカー氏は言う。 私たちは過去 10 年間、個々の細胞をうまく観察してきましたが、うつ病から自閉症、統合失調症に至る一連の精神疾患については、その関連性にも目を向ける必要があります。」
この研究に参加した他の研究者は、アリアナ・メイ、アプア・パコラ、シャニ・スターン、セドリック・バーディ、ジェイソン・クルーグ、ステイシー・キム、ネダ・ネシャット、キム・ヒョンジュン、マンチング・クー、マキシム・ショヒレフ、デビッド・アダモウィッツ、マリア・マルケット、ロベルト・ジャペリ、ジェニファー・アーウィン、クリシュナンであった。ソークのパドマナバン、マシュー・シュトラマン、シン・ジン。
この研究と関与した研究者は、CIRM、ストレイム財団、ヘルムズリー財団、JPB 財団、エングマン財団、国立精神衛生研究所、国立がん研究所、ウェイト財団、および NARSAD 若手研究者からの助成金によって支援されました。アワード。
ジャーナル
細胞幹細胞
作者
アニンディタ・サーカー、アリアナ・メイ、アプア・CM・パコラ、シャニ・スターン、セドリック・バーディ、ジェイソン・R・クルーグ、ステイシー・キム、ネダ・ネシャット、キム・ヒョンジュン、マンチング・クー、マキシム・N・ショヒレフ、デヴィッド・H・アダモヴィッツ、マリア・C・マルケット、ロベルトジャペリ、ジェニファー・A・アーウィン、クリシュナン・パドマナーバン、マシュー・シュトラマン、シン・ジン、フレッド・H・ゲージ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。