
2017 年 9 月 14 日
ソークの科学者は、XNUMXつの重要なタンパク質間の相互作用がニューロンの発達を調節していることを発見した
ソークの科学者は、XNUMXつの重要なタンパク質間の相互作用がニューロンの発達を調節していることを発見した
ラホヤ--ソーク研究所の科学者らは、XNUMXつの重要なタンパク質間の相互作用がニューロンを生成する細胞の調節と維持に役立つことを発見した。 に掲載された作品は、 細胞幹細胞 14 年 2017 月 XNUMX 日の論文は、これらの前駆細胞とニューロンの間の不均衡が精神疾患や加齢に伴う脳疾患の一因となる理由についての洞察を提供します。
「統合失調症、うつ病、アルツハイマー病などの病気にはすべて細胞が原因であることがますますわかってきています」と博士は言う。 ラスティ・ゲージ、ソーク遺伝学研究所の教授であり、新しい研究の上級著者です。 「そのため、私たちは特定の脳細胞がどのように発達するのか、何が脳細胞を健康に保つのか、そしてなぜ加齢やその他の要因が病気につながるのかを理解したいと考えています。」
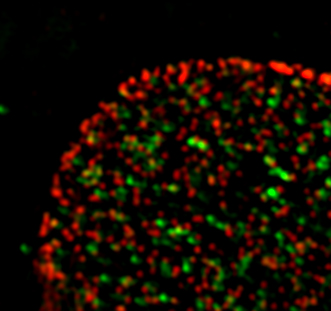
こちらをクリックしてください 高解像度の画像の場合
クレジット: ソーク研究所/ウェイト センター
1998年、ゲージは研究チームを率い、人間は将来すべてのニューロンを持って生まれてくるという数十年にわたる定説に反して、成人の脳が実際に新しいニューロンを生成することを発見した。 それ以来、彼はこの神経発生のさまざまな側面と、さまざまな神経疾患で何が問題になるかを解明してきました。 (たとえば、2015 年に彼の研究室では 双極性障害の細胞基盤を特定した.)
新しい研究では、神経前駆細胞が分裂してニューロンまたはアストロサイトを作成する際に、どのようにして自身の細胞同一性を維持するかを理解しようとしました。 ゲージ氏のチームは、細胞核(ゲノムを含むボール状の膜)の見た目が XNUMX 種類の細胞で大きく異なり、それぞれで活性な遺伝子が異なることをすでに知っていました。 ソーク大学の別の教授で論文の共著者であるマーティン・ヘッツァーは以前、次のことを発見した。 核膜のタンパク質は遺伝子発現に影響を与える さまざまな種類のがん細胞に存在します。 ゲージチームはヘッツァー研究室の専門知識を求めて、脳細胞でも同様のことが起こっているかどうかを調査した。
「私の研究室の研究では、核膜が発生遺伝子制御において重要な役割を果たす動的構造であることが判明しました」と、ソーク大学の最高科学責任者であり、ジェシー・アンド・キャリル・フィリップス財団会長のヘッツァー氏は言う。 「そこで私たちは、まったく異なる種類の細胞を扱うゲージ研究所が何を明らかにするかに非常に興味を持っていました。」
ゲージ氏のチームはマウスとラットの細胞でスクリーニングを実施し、どの遺伝子が前駆細胞、未熟ニューロン、アストロサイトのタンパク質に転写されているかを調べた。 彼らは前駆体中に、Nup153と呼ばれるタンパク質を大量に発見した。これは、核膜にゲートキーピング孔を形成し、出入りを制御する多タンパク質複合体の一部である。 未成熟ニューロンは中程度のNup153レベルを有し、アストロサイトは最も低いレベルを有していた。 153 つの細胞型はすべてほぼ同じ数の核孔を持っているため、研究チームは、Nup153 レベルが細胞型に影響を与え、細胞の前駆体の状態を維持するには高いレベルが必要であると結論付けました。 これは、前駆細胞における NupXNUMX の機能を破壊すると分化が引き起こされるという事実によって裏付けられました。

こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
興味深いことに、Nup153 レベルは、核の周りを浮遊して遺伝子に結合して遺伝子をオンまたはオフにする転写因子である Sox2 と呼ばれる可動性タンパク質のレベルが上昇している細胞でも高いことが知られています。 さまざまな種類の細胞で Nup153 と Sox2 に蛍光タグを付けることにより、Nup153 が Sox2 と相互作用していることが観察されました。
「可動スイッチである転写因子を、非常に安定な構造である細孔複合体に接続することができたという事実は、細胞が遺伝子発現の制御を通じてどのようにアイデンティティを維持するのかについての手がかりを提供します」と戸田智久教授は言う。ソークの研究員であり、論文の筆頭著者。
次に、チームは、細孔複合体と他の転写因子との相互作用が神経機能にどのような影響を与えるかを調査したいと考えており、これにより、特定の神経疾患の根本的な原因についての洞察が得られる可能性があります。
他の著者には、ジョナサン Y. スー、サラ B. リンカー、ローレン フー、サイモン T. シェーファー、ジェローム メルテンス、フェリペ V. ジャシント、マーティン ヘッツァーが含まれます。
この研究は、日本学術振興会、鼎医学振興財団、ポール・G・アレン・ファミリー財団、JPB財団、ドルビー財団、レオナ・M・ヘルムズリーおよびハリー・B・ヘルムスリーからの資金提供を受けた。慈善信託、国立衛生研究所 – 国立がん研究所、チャップマン財団、ウェイト財団、国立神経障害・脳卒中神経科学センター。
ジャーナル
細胞幹細胞
作者
戸田 智久、ジョナサン Y. スー、サラ B. リンカー、ローレン フー、サイモン T. シェーファー、ジェローム メルテンス、フェリペ V. ジャシント、マーティン W. ヘッツァー、フレッド H. ゲージ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。