
2022 年 12 月 1 日
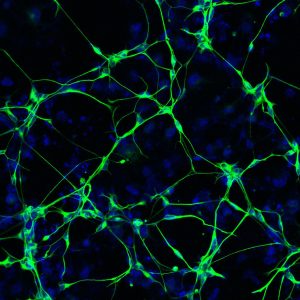
研究室で患者由来のニューロンに施される治療法は、劣化した細胞を除去し、残っている健康な細胞に良い影響をもたらすことができます。
研究室で患者由来のニューロンに施される治療法は、劣化した細胞を除去し、残っている健康な細胞に良い影響をもたらすことができます。
【ラホーヤ】数十年にわたる研究にもかかわらず、アルツハイマー病は依然として衰弱性が高く、最終的には死に至る認知症であり、有効な治療法はない。 アルツハイマー病の95パーセント以上は原因が不明です。 今回、ソーク研究所の科学者らは、アルツハイマー病患者のニューロンが劣化を示し、老化と呼ばれる晩年のストレス過程を経ていることを発見した。 これらのニューロンは機能活動を失い、代謝が障害され、脳の炎症が増加します。
研究者らはまた、悪化しているニューロンを治療薬で標的にすることが、アルツハイマー病の予防または治療に効果的な戦略となる可能性があることも発見した。 調査結果はオンラインで公開されました 細胞幹細胞 12月1、2022に。
「私たちの研究は、これらの非複製細胞が老化の劣化プロセスを経ていること、そしてそれが神経炎症やアルツハイマー病に直接関係していることを明確に示しています」と共連絡著者で教授は述べている。 ラスティ・ゲージ、ソーク研究所の所長であり、加齢に伴う神経変性疾患研究のヴィ・アンド・ジョン・アドラー委員長の保持者。
細胞は老化するにつれて細胞老化を起こす可能性があり、これが組織の機能不全や加齢に関連した障害の一因となります。 老化は、細胞ストレス、分子損傷、癌の発生にも関与していると考えられています。 しかし、科学者たちは以前、老化は主にニューロンではなく、分裂中の細胞で起こると考えていました。 老化した人間のニューロンの老化のような状態についてはほとんど知られていませんでした。
この研究で、ゲージ氏と彼のチームは、アルツハイマー病患者から皮膚サンプルを採取し、研究室でそれらの細胞を直接ニューロンに変換しました。 彼らはこれらのニューロンをテストして老化が起こるかどうかを確認し、その過程に関与するメカニズムを調べました。 彼らはまた、アルツハイマー病患者20人と健康な対照者とを比較し、死後の脳の老化マーカーと遺伝子発現を調査した。 これにより、チームは研究室での結果が実際の人間の脳組織にも当てはまることを確認することができました。
ゲージチームは、老化ニューロンがアルツハイマー病で観察される晩年の脳炎症の原因であることを発見した。 ニューロンが劣化すると、炎症因子が放出され、脳炎症のカスケードを引き起こし、他の脳細胞が混乱する原因となります。 さらに、がんに一般的に関与する遺伝子 KRAS は、老化反応を活性化する可能性があります。
「科学者は通常、人間の脳組織での実験結果を検証しません。 私たちの発見が両方の設定で一貫していたという事実は、これらの老化ニューロンが実際に強力な炎症反応を起こしており、脳に重大な影響を与えているという私たちの結果を裏付けています」と、ゲージ研究室の大学院生で筆頭著者のジョセフ・ハーディは言う。

著者らは、老化した脳における少数の老化ニューロンの影響でさえ、脳機能に重大な影響を与える可能性があると指摘しています。 これは、1,000 つのニューロンが他のニューロンと XNUMX 以上の接続を確立し、脳の通信システムに影響を与える可能性があるためです。
これらの発見に加えて、著者らは皿に入れた患者のニューロンに治療薬(ダサチニブとケルセチンのカクテル)も投与した。 どちらの薬剤も変形性関節症などの症状で体内の老化細胞を除去するために使用されるため、著者らは中枢神経系の老化細胞にも効果があるかどうかを確認したいと考えました。 彼らは、薬物カクテルが老化ニューロンの数を正常レベルまで減少させることを発見した。 したがって、老化細胞を標的とすることは、アルツハイマー病における神経炎症と神経変性を遅らせるための有用なアプローチとなる可能性がある。
研究者らは、この研究でテストされた治療用カクテルは通常は脳に入ることができないことに注意することが重要だと述べている。 しかし、血液脳関門を通過できる既知の薬剤があり、それらは同様の作用をする可能性が高く、将来的には治療の選択肢として使用される可能性があります。
老化ニューロンがどのようにしてアルツハイマー病を引き起こすのか、またこれらのニューロンを脳から除去した場合の影響については、さらに研究が必要です。 著者らは将来、脳に入る可能性のあるいくつかの薬物を試験して、それらが老化ニューロンにどのような影響を与えるかを調べる予定である。 彼らはまた、老化の推進メカニズムを調査し、特定の脳領域が他の領域よりも老化しやすいかどうかを確認する予定です。
他の著者には、Ravi Agarwal、Lukas Karbacher、Dina Zangwill、およびソークの Jerome Mertens が含まれます。 カリフォルニア大学サンディエゴ校のヨハネス・シュラチェツキ氏、ダグ・ガラスコ氏、クリストファー・グラス氏。 オーストリアのレオポルト・フランツェンス大学インスブルック校のラリッサ・トラクスラー氏とレナ・ベーンケ氏。
この研究はブライトフォーカス財団から資金提供を受けました。 国立老化研究所 (AG056306、AG05611、AG057706、K99-AG056679、および AG072502)。 欧州連合 (ERC-STG-2019-852086 および H2020-MSCA-IF-2017-797205); チェン財団。 オーストリア科学基金 (FWF-I5057); ポール G. アレン フロンティア グループ (#19PABHI34610000)。 グレース財団。 JPB財団。 アネット・C・マール・スミス。 リンとエドワード・ストレイム、レイとダグマーのドルビー・ファミリー基金。 天の川研究財団。 ポール・G・アレン家族財団。 スティヒティング ASC アカデミー。 カリフォルニア再生医療研究所 (RT2-01927)。 カリフォルニア大学サンディエゴ校のシャイリー・マルコス・アルツハイマー病研究センター (ADRC; AG062429)。 ウェイト財団。 そしてチャップマン財団。
DOI: 10.1016/j.stem.2022.11.010
ジャーナル
細胞幹細胞
作者
ジョセフ・R・ハーディ、ラリッサ・トラクスラー、ラヴィ・K・アガルワル、ルーカス・カーバッハー、ヨハネス・CM・シュラチェツキ、レナ・ベーンケ、ディナ・ザングウィル、ダグ・ガラスコ、クリストファー・K・グラス、ジェローム・メルテンス、フレッド・H・ゲージ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。