
2016 年 12 月 5 日
ソークの科学者は、幹細胞が健康であるためにはテロメアの長さが適切である必要があることを発見しました
ソークの科学者は、幹細胞が健康であるためにはテロメアの長さが適切である必要があることを発見しました
【ラホーヤ】研究者らがテロメア(染色体の末端にある保護構造)の短縮を老化や病気と結び付けて以来、テロメアの長さを支配する要因の理解に向けた競争が続いている。 今回、ソーク研究所の科学者らは、幹細胞の伸長とトリミングのバランスによって、ゴルディロックス氏が言うように、短すぎず長すぎず、ちょうどよいテロメアが得られることを発見した。
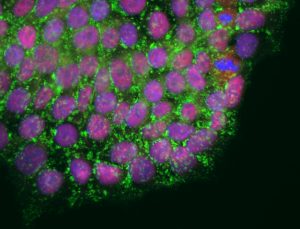
こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
この調査結果は、5 年 2016 月 XNUMX 日号に掲載されています。 自然構造および分子生物学、幹細胞生物学への理解が深まり、特に老化と再生医療に関連した幹細胞ベースの治療の進歩に役立つ可能性があります。
「この研究は、テロメアの最適な長さは、XNUMX つの極端な値の間の慎重に調節された範囲であることを示しています」と述べています。 ヤン・カールセダー、ソーク分子細胞生物学研究所の教授であり、この研究の上級著者でもあります。 「非常に短いテロメアが細胞に害を及ぼすことは知られていました。 しかし、まったく予想外だったのは、テロメアが非常に長い場合にも損傷が発生するという発見でした。」
テロメアは、各染色体の末端にある DNA の繰り返しの部分で、テロメラーゼと呼ばれる酵素によってその長さを伸ばすことができます。 私たちの細胞機構により、細胞が DNA を複製して分裂するたびに、テロメアが少しずつ剥がれ落ちます。 テロメアが時間の経過とともに短縮すると、染色体自体が損傷を受けやすくなります。 最終的には細胞が死んでしまいます。 例外は幹細胞で、幹細胞はテロメラーゼを使用してテロメアを再構築し、分裂能力を維持し、皮膚、心臓、肝臓など、特定の組織や器官のほぼすべての細胞型に発達(「分化」)することができます。または筋肉 - 多能性として知られる性質。 これらの性質により、幹細胞は加齢に伴う細胞損傷や疾患と闘うための再生療法の有望なツールとなります。
「私たちの実験では、テロメアの長さを制限すると多能性が損なわれ、幹細胞の死さえも引き起こしました」と、ソークの研究員で論文の筆頭著者であるテレサ・リベラは言う。 「そこで私たちは、テロメアの長さが増加すると多能性能力が増加するかどうかを知りたかったのです。 驚くべきことに、過度に伸長したテロメアはより脆弱であり、DNA 損傷を蓄積することがわかりました。」
こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
Karlseder、Riveraらは、実験室で培養されたヒト胚性幹細胞(ESC)株におけるテロメアの維持を調査することから始めた。 彼らは分子技術を使用してテロメラーゼ活性を変化させた。 おそらく驚くことではないかもしれませんが、テロメラーゼが少なすぎる細胞はテロメアが非常に短くなり、最終的には細胞が死滅しました。 逆に、テロメラーゼのレベルが増加した細胞は、非常に長いテロメアを持っていました。 しかし、これらの細胞は繁栄する代わりに、テロメアが不安定になりました。
「細胞に非常に長いテロメアを強制的に生成させると、テロメアの脆弱性が生じ、それががんの発生につながる可能性があることを発見して驚きました」と、ドナルド・アンド・ダーリーン・シャイリー委員長も務めるカールセーダー氏は言う。 「これらの実験は、人工的にテロメアを増加させると寿命が延びたり、生物の健康状態が改善したりする可能性があるという一般に受け入れられている概念に疑問を投げかけています。」
研究チームは、非常に長いテロメアが、XRCC3とNbs1と呼ばれる一対のタンパク質によって制御されるトリミング機構を活性化することを観察した。 研究室の実験では、ESCにおけるこれらのタンパク質の発現低下によりテロメアトリミングが妨げられることが示され、XRCC3とNbs1が確かにその役割を担っていることが確認された。
次に、研究チームは、幹細胞様の状態に再プログラムされる分化した細胞(皮膚細胞など)である人工多能性幹細胞(iPSC)に注目しました。 iPSC は、ドナーと遺伝的に一致し、簡単に入手できるため、潜在的な幹細胞治療にとって一般的かつ重要なツールです。 研究者らは、iPSC にはテロメアトリミングのマーカーが含まれており、その存在が細胞の再プログラムがどの程度成功したかを示す有用な指標となることを発見しました。
「幹細胞の再プログラミングは科学上の大きな進歩ですが、その方法はまだ完成の途上にあります。 テロメアの長さがどのように調節されているかを理解することは、幹細胞療法と再生医療の可能性を実現するための重要なステップです」とリベラ氏は言います。
他の著者には、ソーク研究所のキャンディ・ハグブロム氏と、 ナポリの第2大学.
この作業は、によって資金提供されました。 カリフォルニア再生医療研究所 トレーニング補助金 TG2-01158、 ソーク研究所がんセンター コア補助金 (P30CA014195)、 国立衛生研究所 (R01GM087476、R01CA174942)、 ハイランド ストリート財団、フリッツ B. バーンズ財団、エメラルド財団、 グレン老化研究センター.
ジャーナル
自然構造および分子生物学
作者
テレサ・リベラ、キャンディ・ハッグブロム、サンドロ・コスコナーティ、ヤン・カールセーダー
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。