Professor
NOMIS Zentrum für Immunbiologie und mikrobielle Pathogenese
Becky und Ralph S. O'Connor-Stuhl

Das Immunsystem ist ein mächtiges zweischneidiges Schwert. Einerseits ist es gerüstet, um eine Vielzahl von eindringenden fremden Krankheitserregern zu bekämpfen. Andererseits kann es, wenn es nicht kontrolliert wird, auch die eigenen Gewebe eines Organismus angreifen und Entzündungen und Autoimmunerkrankungen wie Allergien, Asthma, rheumatoide Arthritis, Multiple Sklerose und Typ-1-Diabetes verursachen. Es gibt mehrere Schutzmechanismen in unseren Zellen, um eine Autoimmunreaktion zu verhindern, aber diese können außer Kontrolle geraten. Darüber hinaus können einige Krebsarten auch die Erkennung durch das Immunsystem umgehen oder kapern, was das Wachstum von Tumorzellen ermöglicht.
Um zu lernen, wie das Immunsystem gestärkt oder korrigiert werden kann, konzentriert sich Ye Zheng auf eine spezielle Gruppe von Immunzellen, die regulatorischen T-Zellen (Tregs). Tregs steuern die Immunantwort und signalisieren den aggressiveren Immunzellen, wann sie ihren frenetischen Angriff einstellen sollen. Eine abnormale Funktion von Treg-Zellen wird mit mehreren Autoimmunerkrankungen und Tumoren in Verbindung gebracht. Insbesondere ist ein wichtiger molekularer Bestandteil dieser Zellen, ein Protein namens Foxp3, oft für mangelhafte Tregs verantwortlich. Zheng macht Fortschritte im Verständnis der Gene, die Foxp3 steuern – sowie der Gene, die Foxp3 steuert –, um letztendlich Wege zur Regulierung der Treg-Zellfunktion zu finden. Da Eingriffe in Treg-Zellen die Immunantwort entweder schwächen oder stärken können, können seine Ergebnisse möglicherweise neue Wege in der Behandlung von Autoimmunerkrankungen eröffnen, die Überlebenschancen bei Organtransplantationen verbessern und neue Krebsziele aufdecken.
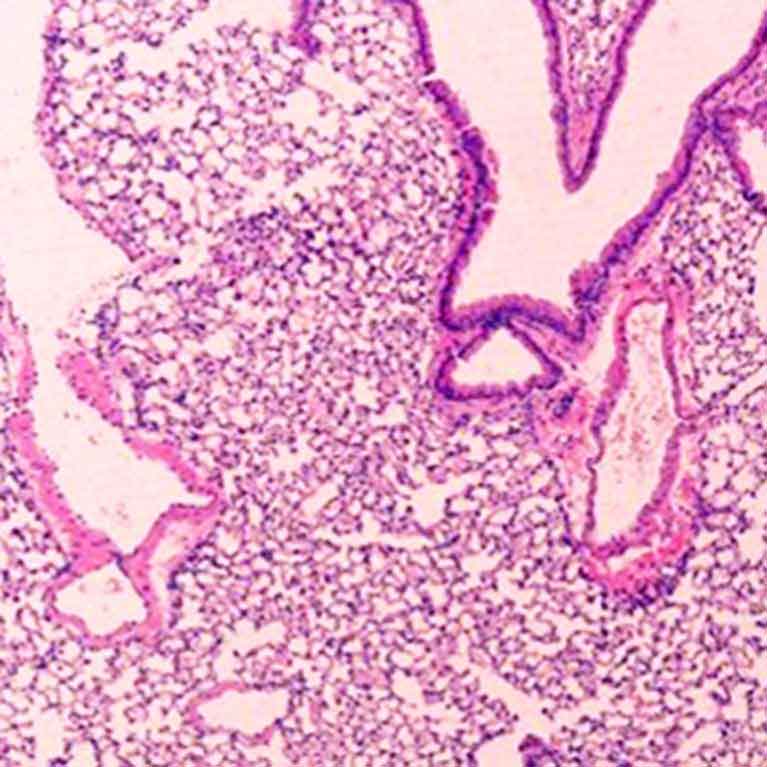
Zheng hat Hunderte von Genen kartiert, die direkt mit dem Foxp3-Protein von Tregs zusammenhängen, um ein umfassenderes Bild davon zu erhalten, wie sich diese zellulären Friedensstifter entwickeln und funktionieren.
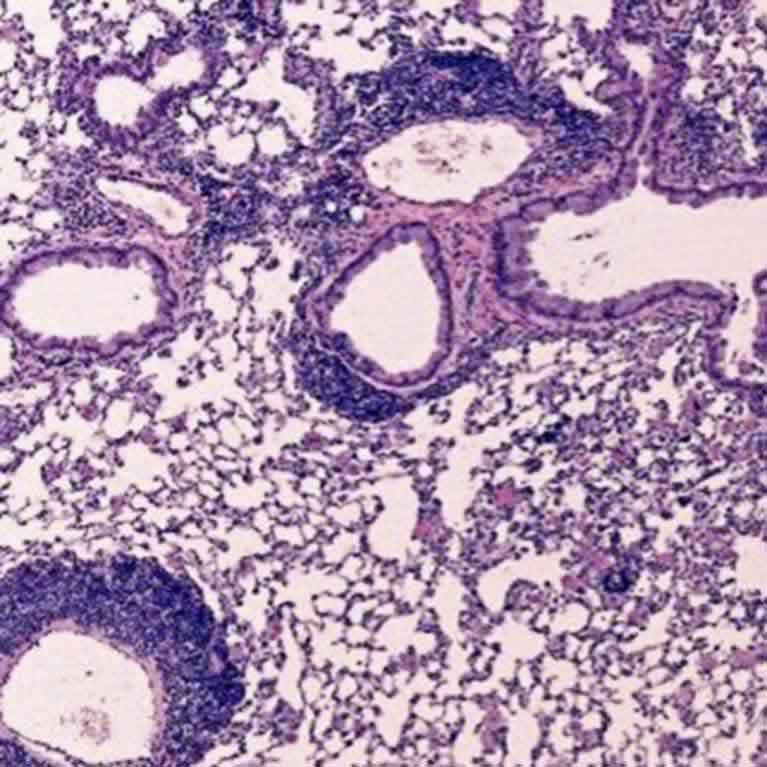
Zhengs Labor entdeckte, dass eine bestimmte genetische Sequenz in Foxp3 (genannt CNS2) für die Stabilität einer Treg-Zelle verantwortlich ist. Wenn das Team CNS2 entfernte, wurden Treg-Zellen instabil und verwandelten sich oft in Killer-T-Zellen – die Art von Zelle, die Tregs eigentlich kontrollieren sollen –, was zu Autoimmunerkrankungen bei Tieren führte.
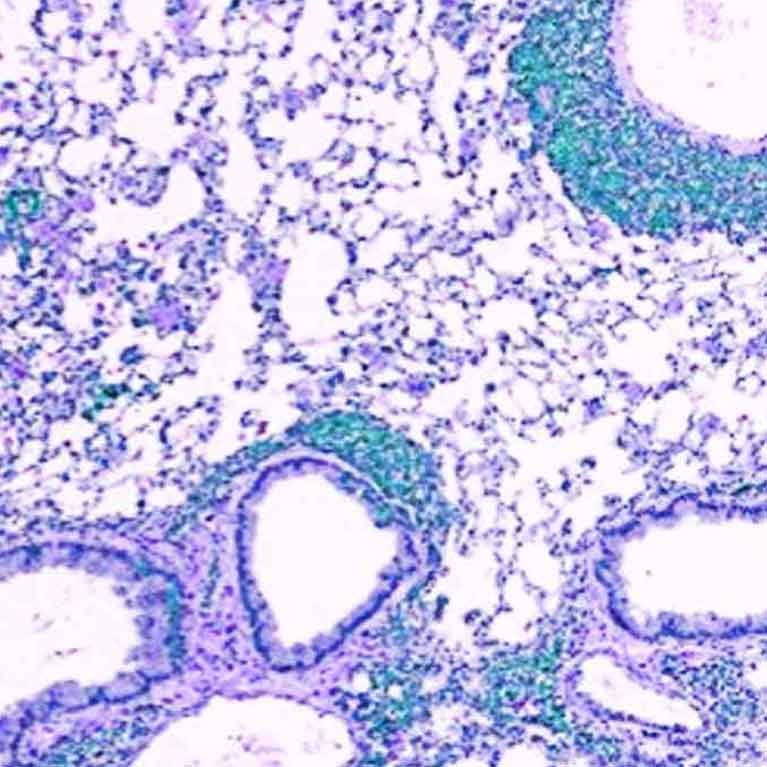
Sein Team identifizierte eine Gruppe von Proteinen, die direkt von Foxp3 reguliert werden und die Funktion von Treg-Zellen steuern. Diese Proteine können gezielt eingesetzt werden, um die Funktion von Treg-Zellen zur Behandlung von Autoimmunerkrankungen wie Typ-1-Diabetes, Allergien und Asthma zu verbessern.
BS, Biochemie und Molekularbiologie, Peking Universität, Peking, China
Promotion, Columbia University
Postdoktorand, University of Washington
Forschungsstipendiat des Memorial Sloan-Kettering Cancer Center
Postdoktoranden-Stipendium des Krebsforschungszentrums