
9 أغسطس 2009
لا جولا ، كاليفورنيا - كشفت دراسة تعاونية أجراها باحثون في معهد سالك للدراسات البيولوجية أن مثبط الورم p53 ، الذي جعل اسمه "حارس الجينوم" ، لا يوقف الخلايا التي يمكن أن تصبح سرطانية في مساراتها فحسب ، بل يتحكم أيضًا إعادة برمجة الخلايا الجسدية.
على الرغم من أن العلماء قد تعلموا كيفية إعادة برمجة الخلايا البشرية البالغة مثل خلايا الجلد إلى ما يسمى بالخلايا الجذعية المستحثة متعددة القدرات (iPSCs) ، إلا أن كفاءة إعادة البرمجة لا تزال منخفضة للغاية. نشرت دراسة Salk في 9 أغسطس طبعة متقدمة على الإنترنت من الطبيعة، يعطي فكرة جديدة عن سبب إقناع عدد قليل فقط من الخلايا من بين العديد من الخلايا بإعادة عقارب الساعة إلى الوراء.

الدكتور خوان كارلوس إيزبيسا بيلمونتي والدكتور جيفري م. وال
"على الرغم من أننا تمكنا من إعادة برمجة الخلايا المتخصصة لفترة من الوقت الآن ، إلا أنه لم يكن هناك شيء معروف عن آليات التحكم التي تمنع حدوث ذلك تلقائيًا في الجسم ولماذا كان من الصعب للغاية تغيير مصيرهم في طبق بتري ،" يقول خوان كارلوس إيزبيسا بيلمونتي، دكتوراه ، أستاذ في مختبر التعبير الجيني ، الذي عمل عن كثب معه جيفري م، دكتوراه أيضا أستاذ في مختبر التعبير الجيني.
وتقترب النتائج التي توصلوا إليها من تقنية iPSCs خطوة أقرب إلى الوفاء بوعدها كمصدر للخلايا الجذعية الخاصة بالمريض ولكنها تجبر العلماء أيضًا على إعادة التفكير في تطور السرطان.
يقول وال: "كانت هناك فكرة عمرها عقد من الزمان مفادها أن السرطان ينشأ من خلال إلغاء التمايز بين الخلايا الملتزمة والمتخصصة بالكامل ، ولكن في النهاية تم إهمالها لصالح نظرية الخلايا الجذعية السرطانية الشائعة حاليًا". "الآن ، بعد أن علمنا أن البروتين p53 يمنع عدم التمايز ، أعتقد أن الوقت قد حان لإعادة النظر في إمكانية أن تلعب إعادة البرمجة دورًا في تطور السرطان نظرًا لأن جميع الخلايا السرطانية تقريبًا تفقد وظيفة p53 بطريقة أو بأخرى."
مع انتقال أجنة الثدييات عبر سلسلة من مراحل النمو ، فإن خيارات الخلايا الجذعية الجنينية ، التي تتمتع بآفاق غير محدودة تقريبًا ، محدودة بشكل تدريجي حتى تؤدي في النهاية إلى ظهور ما يقرب من 200 نوع من الخلايا التي تشكل أجسامنا وتفتقر عمومًا إلى القدرة على العودة. العودة إلى مرحلة أقل تخصصًا.
على الرغم من أن التمايز بشكل عام لا رجوع فيه ، فقد طور العلماء عدة طرق للتغلب على إحجام الخلايا عن إعادة البرمجة. تتضمن التكنولوجيا الأكثر استخدامًا التعبير القسري لأربعة عوامل نسخ - Oct4 و Sox2 و Klf4 و c-Myc- في الخلايا البالغة الملتزمة بالكامل.
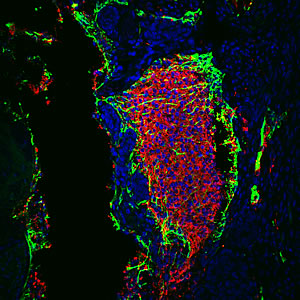
يؤدي تنظيم نشاط p53 إلى زيادة كفاءة إعادة البرمجة للخلايا الجسدية البالغة التي تتطلب فقط عاملين لإعادة البرمجة بدلاً من الأربعة المعتادة.
الصورة: بإذن من الدكتور جوان كارلوس بيلمونتي ، معهد سالك للدراسات البيولوجية
يقول بلمونتي: "لسوء الحظ ، فإن Klf4 و c-Myc هما من الجينات الورمية وإضافتهما يحمل خطر التسبب في السرطان". ومع ذلك ، على الرغم من الدفع الإضافي الذي توفره تلك الجينات المسرطنة القوية ، فإن جزءًا صغيرًا فقط يتحول إلى خلايا iPSCs التي تبدو وتتصرف مثل الخلايا الجذعية الجنينية ، مما دفع بلمونتي إلى التساؤل عما إذا كان ما يفعلونه لجعل الخلايا تعيد البرمجة يسبب استجابة أوقفت الخلايا. من النمو؟
في محادثة مع جاره المجاور ، قدم خبير السرطان وال بعض الأفكار الجديدة التي يمكن اختبارها في المختبر. يقول وال: "في العادة ، لا تُعاد برمجة الخلايا ، لذا يجب أن تكون هناك آلية تمنع ذلك". "علمنا أن c-Myc وبعض الجينات الأخرى المطلوبة لإعادة البرمجة تنشط مثبط الورم p53 وتساءلنا عما إذا كان له أي دور فيه."
وبالتأكيد ، كشفت التجارب التي أجراها باحثو ما بعد الدكتوراه والمؤلفون المشاركون في الدراسة ، Teruhisa Kawamura ، و Jotaro Suzuki ، Ph.D. ، أن إضافة عوامل إعادة البرمجة c-Myc و Klf4 ، بمفردها أو في مجموعات مختلفة ، أدت إلى تنشيط p53 مسار. كمستجيب أول ، يتم استدعاء مثبط الورم p53 للعمل عندما تعاني الخلايا من ظروف مرهقة. اعتمادًا على الموقف ، يقوم p53 بعد ذلك بتشغيل الجينات التي توقف انقسام الخلية لإتاحة الوقت للإصلاحات أو ، عندما تكون جميع محاولات الإنقاذ غير مجدية ، تأمر الخلية بالتوقف عن الانقسام إلى الأبد أو الانتحار.
في الخلايا المعدلة وراثيًا لتفتقر إلى p53 ، زادت كفاءة إعادة البرمجة بمقدار 10 أضعاف على الأقل مقارنة بخلايا التحكم ، مما يدل على أن p53 لعب دورًا مهمًا في السيطرة على الخلايا التي تحاول العودة إلى حالة شبيهة بالجذع.
نظرًا لأن iPSCs التي تم إنشاؤها باستخدام مجموعة كاملة من عوامل إعادة البرمجة معرضة لخطر التحول إلى خبيثة ، أراد Belmonte وفريقه معرفة ما إذا كان يمكن إعادة برمجة خلايا الفئران التي تفتقر إلى p53 باستخدام عاملين فقط ، Oct4 و Sox2. تحولت الخلايا بسهولة إلى iPSCs وأدت إلى ظهور فئران سليمة كاملة المدة كانت قادرة على التكاثر واجتياز الاختبار النهائي للخلايا الجذعية الجنينية متعددة القدرات.
يقول وال: "هذا التعاون الناجح للغاية هو مثال رئيسي على ما يجعل Salk مكانًا خاصًا". "أنا وخوان كارلوس نتحدث كل يوم ونتعامل مع نفس السؤال من وجهات نظر مختلفة للغاية. إنه يأتي من منظور علم الأحياء التطوري ، بينما أتيت من الجانب السرطاني ولكن عندما يتم تجميعها معًا يمكن أن تصنع قصة رائعة ".
للحصول على معلومات حول تسويق هذه التكنولوجيا ، يرجى الاتصال بمكتب Salk لإدارة وتطوير التكنولوجيا على (858) 453-4100 ، تحويلة. 1278.
تم دعم هذا العمل من قبل المعاهد الوطنية للصحة ، ومنح من Tercel و Marato و G. Harold و Leila Y. Mathers Charitable Foundation و Fundacion Cellex.
الباحثون الذين ساهموا أيضًا في العمل هم Yunyuan V. Wang ، Ph.D. في مختبر وال ، دكتوراه سيرجيو مينينديز ، دكتوراه لورا باتل موريرا ، وأنجيل رايا ، دكتوراه ، كل ذلك في مركز الطب التجديدي في برشلونة ، إسبانيا.
عن معهد سالك للدراسات البيولوجية:
معهد سالك للدراسات البيولوجية هو أحد المؤسسات البحثية الأساسية البارزة في العالم ، حيث يقوم أعضاء هيئة التدريس المشهورون دوليًا بالتحقيق في أسئلة علوم الحياة الأساسية في بيئة فريدة وتعاونية وإبداعية. من خلال التركيز على الاكتشاف وتوجيه الأجيال القادمة من الباحثين ، يقدم علماء Salk مساهمات رائدة لفهمنا للسرطان والشيخوخة ومرض الزهايمر والسكري واضطرابات القلب والأوعية الدموية من خلال دراسة علم الأعصاب وعلم الوراثة وبيولوجيا الخلايا والنباتات والتخصصات ذات الصلة.
تم الاعتراف بإنجازات أعضاء هيئة التدريس بالعديد من الأوسمة ، بما في ذلك جوائز نوبل والعضويات في الأكاديمية الوطنية للعلوم. تأسس المعهد في عام 1960 من قبل رائد لقاح شلل الأطفال جوناس سالك ، وهو مؤسسة مستقلة غير ربحية ومعلم معماري.
مكتب الاتصالات
هاتف: (858) 453-4100
اضغط@salk.edu