
14 آذار، 2018
ابتكر علماء سالك مقصًا جزيئيًا جديدًا لتصحيح اختلال توازن البروتين في النموذج الخلوي للخرف
ابتكر علماء سالك مقصًا جزيئيًا جديدًا لتصحيح اختلال توازن البروتين في النموذج الخلوي للخرف
LA JOLLA— لقد سمع معظم الناس عن تقنية تحرير الجينات CRISPR / Cas9 ، والتي تعمل كمقص جزيئي مستهدف لقطع الجينات المسببة للأمراض واستبدالها بالجينات السليمة. لكن الحمض النووي ليس سوى جزء من القصة. تنجم العديد من الأمراض الوراثية عن مشاكل في الحمض النووي الريبي ، وهو نسخة عاملة من الحمض النووي تُترجم إلى بروتينات.
الآن ، ابتكر علماء معهد Salk أداة جديدة لا تستهدف الحمض النووي ، بل الحمض النووي الريبي ، واستخدموها لتصحيح اختلال توازن البروتين في الخلايا من مريض الخرف ، وإعادتها إلى مستويات صحية. تفتح أداة Salk الجديدة ، المسماة CasRx ، الإمكانات الهائلة للحمض النووي الريبي والبروتينات للهندسة الوراثية ، مما يمنح الباحثين طريقة قوية لتطوير علاجات جينية جديدة بالإضافة إلى التحقيق في الوظائف البيولوجية الأساسية. ظهر العمل في الموبايل في مارس 15 ، 2018.
يقول المهندسون الحيويون مثل محققي الطبيعة ، يبحثون عن أدلة في أنماط الحمض النووي للمساعدة في حل ألغاز الأمراض الوراثية. باتريك هسو، زميل Helmsley-Salk ومؤلف رئيسي للورقة الجديدة. "لقد أحدثت تقنية CRISPR ثورة في هندسة الجينوم ، وأردنا توسيع صندوق الأدوات من DNA إلى RNA."
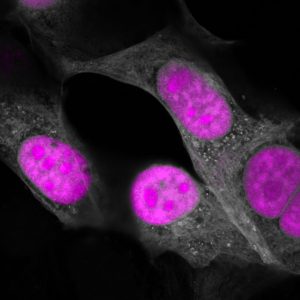
اضغط هنا للحصول على صورة عالية الدقة.
الائتمان: معهد سالك
كريسبر هي أجهزة مناعية بكتيرية تحتوي على العديد من الإنزيمات الدفاعية مثل "المقص الجزيئي" Cas9 ، والذي صممه العلماء بما في ذلك Hsu كأداة قوية لتحرير الجينات لاستهداف الحمض النووي.
قرر فريق Salk البحث في جينومات البكتيريا عن إنزيمات CRISPR الجديدة التي يمكن أن تستهدف الحمض النووي الريبي ، والتي يمكن بعد ذلك هندستها لمعالجة مشاكل الحمض النووي الريبي والبروتينات الناتجة.
يمكن التعبير عن رسالة RNA معينة ، على سبيل المثال ، على مستويات مختلفة وتوازنها بالنسبة إلى RNAs الأخرى أمر بالغ الأهمية لوظيفة صحية. علاوة على ذلك ، يمكن تقطيع الحمض النووي الريبي (RNA) بطرق مختلفة لصنع بروتينات مختلفة ، لكن مشاكل التضفير يمكن أن تؤدي إلى أمراض مثل ضمور العضلات الشوكي والتليف الكيسي اللانمطي والخرف الجبهي الصدغي (FTD). لذا فإن الدواء الذي يستهدف RNAs أو RNAs السامة الناتجة عن التضفير غير السليم يمكن أن يكون له تأثير على حياة الأشخاص المصابين بهذه الأنواع من الأمراض المدمرة.
"لقد بدأنا المشروع بفرضية أن أنظمة CRISPR المختلفة ربما تكون متخصصة خلال سباق تسلح تطوري بين البكتيريا وفيروساتها ، مما يمنحها القدرة على استهداف الحمض النووي الريبي الفيروسي" ، كما توضح سيلفانا كونرمان ، زميلة أبحاث في Salk ، زميلة HHMI Hanna Gray والمؤلف الأول للورقة.
طور الفريق برنامجًا حسابيًا للبحث في قواعد بيانات الحمض النووي البكتيري عن التواقيع المنبهة لأنظمة كريسبر: أنماط تسلسل الحمض النووي المكرر المعين. وبذلك ، اكتشفوا عائلة من إنزيمات كريسبر التي تستهدف الحمض النووي الريبي ، وأطلقوا عليها اسم Cas13d.
أدرك الفريق ، تمامًا مثل عائلة Cas9 ، أن إنزيمات Cas13d التي تنشأ من أنواع بكتيرية مختلفة ستختلف في نشاطها ، لذلك قاموا بتشغيل شاشة لتحديد أفضل نسخة للاستخدام في الخلايا البشرية. تبين أن هذه النسخة من بكتيريا الأمعاء Ruminococcus flavefaciens XPD3002 ، مما دفعهم إلى تسمية أداتهم CasRx.
"بمجرد أن صممنا CasRx ليعمل بشكل جيد في الخلايا البشرية ، أردنا حقًا أن نضعه في خطواته ،"
يقول كونرمان.

اضغط هنا للحصول على صورة عالية الدقة.
وهذا يعني هندسة CasRx لمعالجة حالة مرتبطة بالمرض: في هذه الحالة ، اضطراب التنكس العصبي FTD. في هذا الخرف ، تكون نسبة نسختين من بروتين تاو (المتورط أيضًا في مرض الزهايمر) غير متوازنة في الخلايا العصبية. قام الفريق بهندسة CasRx وراثيًا لاستهداف تسلسل الحمض النووي الريبي لنسخة بروتين تاو التي تزداد وفرة. لقد فعلوا ذلك عن طريق تغليف CasRx في فيروس وتسليمه إلى الخلايا العصبية المزروعة من الخلايا الجذعية لمريض FTD. كان CasRx فعالًا بنسبة 80 في المائة في إعادة التوازن بين مستويات بروتين تاو إلى مستويات صحية.
بالمقارنة مع التقنيات الأخرى التي تستهدف الحمض النووي الريبي ، يعتبر CasRx فريدًا نظرًا لصغر حجمه (مما يسهل حزمه في ناقلات فيروسية ذات صلة علاجياً) ، ودرجة فعاليته العالية ، وحقيقة أنه لم ينتج عنه تأثيرات واضحة خارج الهدف مقارنة بـ RNA التشوش. فريق Salk متحمس بشأن الاحتمالات التي تفتحها أداتهم لاستكشاف أسئلة بيولوجية جديدة حول RNA ووظيفة البروتين ، بالإضافة إلى علاجات لمعالجة RNA والأمراض القائمة على البروتين.
ويضيف هسو: "الطبيعة مليئة بالعديد من الأسرار". "إنه حقًا مورد ثري غير مستغل لابتكار تقنيات جديدة."
ومن بين المؤلفين الآخرين بيتر لطفي ، ونيكولاس ج.بريدو ، وجنيفر أوكي ، وماكسيم إن. شوخيريف ، وجميعهم في معهد سالك.
تم دعم العمل والباحثين المشاركين من خلال جائزة الاستقلال المبكر لمدير المعاهد الوطنية للصحة ، والمعاهد الوطنية للشيخوخة ، وصندوق هيلمسلي الخيري ، وزمالة مؤسسة كاثارينا ، وزمالة هانا جراي التابعة لمعهد هوارد هيوز الطبي ، وجائزة سالك الخاصة للمرأة والعلوم. .
JOURNAL
الموبايل
مؤلفون
سيلفانا كونرمان ، بيتر لطفي ، نيكولاس ج.بريدو ، جينيفر أوكي ، مكسيم ن.شوكيرف ، باتريك د.
مكتب الاتصالات
هاتف: (858) 453-4100
اضغط@salk.edu
معهد سالك هو معهد بحثي مستقل غير ربحي، أسسه جوناس سالك عام 1960، وهو مطوّر أول لقاح آمن وفعال ضد شلل الأطفال. تتمثل مهمة المعهد في قيادة أبحاث أساسية وتعاونية وجريئة تتناول أكثر التحديات إلحاحًا التي تواجه المجتمع، بما في ذلك السرطان ومرض الزهايمر وهشاشة القطاع الزراعي. وتُشكّل هذه العلوم الأساسية ركيزة أساسية لجميع الجهود التطبيقية، إذ تُسهم في توليد رؤى تُتيح تطوير أدوية وابتكارات جديدة على مستوى العالم.