
24 كانون الثاني 2011
لا جولا ، كاليفورنيا — الورم الأرومي الدبقي ، وهو الشكل الأكثر شيوعًا وفتكًا لسرطان الدماغ والمرض الذي قتل عضو مجلس الشيوخ عن ولاية ماساتشوستس تيد كينيدي ، يقاوم تقريبًا كل جهود العلاج ، حتى عندما يتعرض للهجوم في وقت واحد على عدة جبهات. اكتشف باحثون في معهد سالك للدراسات البيولوجية أحد التفسيرات في المرونة غير المتوقعة للخلايا السرطانية.
عند مواجهة نقص الأكسجين الذي يهدد الحياة ، يمكن لخلايا الورم الأرومي الدبقي أن تحول التروس وتتحول إلى أوعية دموية لضمان استمرار الإمداد بالمغذيات ، وفقًا لتقارير فريق بقيادة اندر فيرما، دكتوراه ، في مقال خاص في عدد هذا الأسبوع من وقائع الاكاديمية الوطنية للعلوم.
لا تشرح دراستهم سبب فشل علاجات السرطان التي تستهدف تكوين الأوعية - نمو شبكة من الأوعية الدموية التي تزود الأنسجة السرطانية بالمغذيات والأكسجين - بشكل روتيني في الورم الأرومي الدبقي ، ولكن النتائج قد تحفز أيضًا على تطوير الأدوية التي تستهدف أهدافًا جديدة.
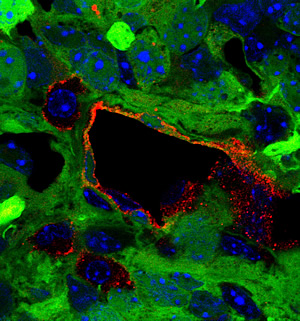
يمكن أن تتحول الخلايا السرطانية للورم الأرومي الدبقي (الموضحة باللون الأخضر) إلى خلايا بطانية (كما هو موضح باللون الأحمر) ، والتي تبطن السطح الداخلي للوعاء الورمي.
الصورة بإذن من الدكتور ياسوشي سودا ، معهد سالك للدراسات البيولوجية
يقول المؤلف الكبير فيرما ، الأستاذ في مختبر علم الوراثة وصاحب كرسي إيروين وجوان جاكوبس في Exemplary Life علوم. لا يكفي تعطيل تكوين الأوعية الدموية للورم. علينا أيضًا أن نمنع تحول الخلايا السرطانية إلى خلايا أوعية دموية ".
لكي تنمو بقطر يزيد عن XNUMX إلى XNUMX مليمتر - حجم رأس الدبوس تقريبًا - تحتاج الأورام إلى إمداد الدم المستقل الخاص بها. لتجنيد الأوعية الدموية الجديدة من الأوعية الدموية الموجودة ، فإن العديد من الأورام تفرط في التعبير عن عوامل النمو ، في الغالب عامل النمو البطاني الوعائي ، أو VEGF. أدى ذلك إلى تطوير عقار Avastin ، وهو جسم مضاد أحادي النسيلة يعترض VEGF.
يوضح فيرما: "في المرحلة الثانية من التجارب السريرية الأخيرة ، استجاب 60 في المائة من المرضى المصابين بالورم الأرومي الدبقي لمزيج من أفاستين وإرينوتيكان ، والذي يتداخل بشكل مباشر مع نمو الخلايا السرطانية ، ولكن في معظم المرضى كان هذا التأثير عابرًا فقط". في الواقع ، أظهرت الدراسات أن الخلايا السرطانية غالبًا ما تصبح أكثر عدوانية بعد العلاج المضاد لتولد الأوعية ، لكن السبب كان غير واضح.
لمعرفة ذلك ، استفاد باحث ما بعد الدكتوراه والمؤلف الأول ياسوشي صودا ، دكتوراه ، من نموذج الفئران للورم الأرومي الدبقي الذي يلخص تطور وتطور أورام الدماغ البشرية التي تنشأ بشكل طبيعي. "الأورام في هذه الفئران تشبه إلى حد بعيد الأورام الأرومية الدبقية ، بما في ذلك الأوعية الورمية الفوضوية وعالية النفاذية ، مما سمح لنا بدراسة الأوعية الدموية للورم بتفصيل كبير" ، يشرح.
فئران الورم الأرومي الدبقي ، التي تم تطوير مفهومها في مختبر فيرما ، تنمو أورام المخ في غضون بضعة أشهر من حقنها بالفيروسات التي تحمل الجينات الورمية النشطة وجين واصم يتسبب في توهج جميع الخلايا المشتقة من الورم باللون الأخضر تحت الضوء فوق البنفسجي. ببساطة عن طريق تتبع التوهج الأخضر تحت المجهر ، يمكن لباحثي Salk متابعة مصير الخلايا السرطانية.
عندما أطل الصودا على الخلايا السرطانية ، وجد - مما أثار دهشته - أن حوالي 30 في المائة من الخلايا البطانية الوعائية - الخلايا المتخصصة التي تبطن السطح الداخلي للأوعية الدموية - تبدو خضراء. يقول: "هذا يشير إلينا على الأرجح أنها نشأت من الخلايا السرطانية".
كشفت تجارب أخرى أن TDECs ، وهي اختصار للخلايا البطانية المشتقة من الورم ، ليست خاصة بأورام الفئران ولكن يمكن العثور عليها أيضًا في العينات السريرية المأخوذة من مرضى الورم الأرومي الدبقي البشري. "كان هذا دليلًا قويًا بالنسبة لنا على أن خلايا الورم الأرومي الدبقي تنتقل بشكل روتيني إلى خلايا بطانية" ، كما يوضح.
يحدث التحول بسبب نقص الأكسجة ، أو انخفاض مستويات الأكسجين ، مما يشير إلى الخلايا السرطانية بأن الوقت قد حان لبدء حيلتها المتغيرة الشكل. ولكن على عكس الخلايا البطانية الوعائية العادية ، لا تتطلب TDECs VEGF لتكوين أوعية دموية وظيفية. يقول فيرما: "قد يفسر هذا سبب فشل العلاج المضاد لتولد الأوعية في نهاية المطاف في الأورام الأرومية الدبقية ، على الرغم من نجاحه في البداية".
يقطع Avastin الأوعية الدموية الطبيعية ، ولكن في النهاية يتم استبدالها بأوعية مشتقة من الورم ، والتي أصبحت الآن مقاومة للعلاج. يقول فيرما: "مرة أخرى ، نواجه تعدد استخدامات الخلايا السرطانية ، مما يسمح لها بالبقاء والنمو في ظل ظروف معاكسة". "ولكن بينما نتعلم المزيد عن المرونة الجزيئية للأورام ، سنكون قادرين على تصميم علاجات مركبة جديدة ومصممة خصيصًا لمكافحة أورام الدماغ المميتة."
ومن بين الباحثين الذين ساهموا أيضًا في العمل توموتشي ماروموتو ، وديناورا فريدمان مورفينسكي ، ومي سودا ، وفي ليو في معهد سالك. Hiroyuki Michiue في قسم علم وظائف الأعضاء في كلية الدراسات العليا للطب وطب الأسنان والعلوم الصيدلانية بجامعة أوكاياما ؛ ساندرا باستورينو وسانتوش كيساري من قسم علوم الأعصاب ، مركز مور للسرطان ، جامعة كاليفورنيا ، سان دييغو ؛ وكذلك منغ يانغ وروبرت إم هوفمان في شركة AntiCancer، Inc. في سان دييغو.
تم تمويل العمل جزئيًا من قبل المعاهد الوطنية للصحة ، ومؤسسة Merieux ، ومؤسسة Ellison Medical Foundation ، و Ipsen / Biomeasure ، و Sanofi Aventis ، و HN and Frances C. Berger Foundation ، ومؤسسة James S. McDonnell Foundation.
عن معهد سالك للدراسات البيولوجية:
معهد سالك للدراسات البيولوجية هو أحد المؤسسات البحثية الأساسية البارزة في العالم ، حيث يقوم أعضاء هيئة التدريس المشهورون دوليًا بالتحقيق في أسئلة علوم الحياة الأساسية في بيئة فريدة وتعاونية وإبداعية. من خلال التركيز على الاكتشاف وتوجيه الأجيال القادمة من الباحثين ، يقدم علماء Salk مساهمات رائدة لفهمنا للسرطان والشيخوخة والزهايمر والسكري والأمراض المعدية من خلال دراسة علم الأعصاب وعلم الوراثة وبيولوجيا الخلايا والنباتات والتخصصات ذات الصلة.
تم الاعتراف بإنجازات أعضاء هيئة التدريس بالعديد من الأوسمة ، بما في ذلك جوائز نوبل والعضويات في الأكاديمية الوطنية للعلوم. تأسس المعهد في عام 1960 من قبل رائد لقاح شلل الأطفال جوناس سالك ، وهو مؤسسة مستقلة غير ربحية ومعلم معماري.
مكتب الاتصالات
هاتف: (858) 453-4100
اضغط@salk.edu