
2010 年 3 月 24 日
カリフォルニア州ラホヤ—小さなゼブラフィッシュのような硬骨魚は、哺乳類が夢見ることしかできない驚くべき能力を持っている。心臓の一部を切り落とすと、数日間はゆっくりと泳ぐが、XNUMXか月以内には完全に正常に見える。 彼らがこれをどのように達成するのか、あるいはもっと重要なことに、なぜそれができないのかは、今日の再生医療における重要な問題の XNUMX つです。
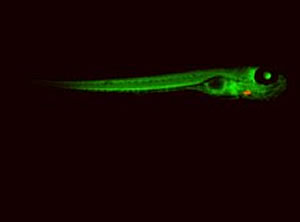
イズピスア・ベルモンテ氏と彼のチームは、心臓が赤く光るゼブラフィッシュを使って、傷ついたゼブラフィッシュの心臓が自己修復する細胞を特定した。
画像: ソーク生物学研究所、Juan Carlos Izpisúa Belmonte 提供
25年2010月XNUMX日号に掲載された論文で 自然ソーク生物学研究所とバルセロナ再生医療センター(CMRB)で働く研究者らは、この驚くべき治癒の偉業の源である魚の心臓細胞集団を特定した。この発見は、哺乳類の心臓がどのように慰められるのかについての洞察を与える可能性がある。心臓発作による怪我の後に自分自身を修復するために。
フアン・カルロス・イズピスア・ベルモンテ遺伝子発現研究室の教授である博士とその同僚らは、傷ついた魚の心臓を修復するのは、「通常の」再生の疑いのある幹細胞ではないと報告している。 代わりに、修復は心筋細胞として知られる分化した心筋細胞によって行われます。心筋細胞は、心臓の収縮力を供給するのが通常の役割である細胞の成長体です。
「私たちの研究結果が示しているのは、母なる自然は、組織や器官を再生するために多能性幹細胞まで遡る以外に、別の方法も利用しているということです」とイズピスア・ベルモンテ氏は述べ、少なくとも魚類では、体が驚くべき修復を進化させた可能性があると指摘した幹細胞よりも味付けされた細胞タイプによって推進される戦略。
切除したゼブラフィッシュの心筋を実際に満たしている細胞を特定するために、イズピスア・ベルモンテのチームはまず遺伝子工学を利用し、顕微鏡下で心筋細胞を緑色に光らせるトレーサー遺伝子を心筋細胞に挿入することによって心筋細胞のみを「トランスジェニック」にした。
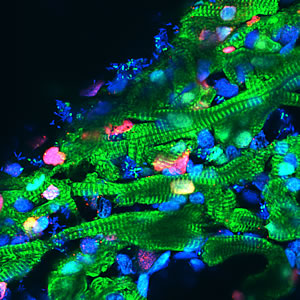
心筋細胞(緑色で表示)は、損傷後により若々しい状態に退行し、失われた細胞を補充するために再び分裂を開始し(赤色のマーカーで示されます)、再び心筋細胞に成熟します。
画像: ソーク生物学研究所、Juan Carlos Izpisúa Belmonte 提供
その後、文字通り各魚の心室の約 20% を切り落とし、心臓が再生するまで数週間待ちました。再生された心筋が光らない場合、それは心筋細胞以外の細胞 (心臓幹細胞集団など) が損傷していることを意味します。損傷した筋肉を置き換えました。
しかし、驚くべき発見として、再生された心筋細胞はすべて緑色に光り、損傷後に残った十分に確立された心筋細胞がより「若い」状態に退行し、失われた細胞を補充するために再び分裂を開始し、その後、再び成熟して新しい心臓になったことを示しています。筋。 同グループはまた、心筋細胞が、細胞増殖に関連するタンパク質の産生を再活性化することによって、部分的には失われた若さを取り戻したことも示した。このタンパク質は、通常、未熟な前駆細胞に発現する因子である。
人間の心臓は、このような再生変化を単独で起こすことはできません。 心臓発作によって損傷を受けると、心筋は収縮できない瘢痕組織に置き換わります。 しかし、心不全に先立って、損傷した哺乳類の心筋細胞は「冬眠」として知られる自分自身を守るための状態に入り、生き残るために収縮を停止します。
CMRBのイズピスア・ベルモンテ氏の博士研究員であり、この研究の筆頭著者であるクリス・ジョプリング博士は、人間の心臓の「冬眠」が重要であると見ている。 同氏は、「ゼブラフィッシュの心臓再生中に、心筋細胞が冬眠中の心筋細胞で観察されるものと同様の構造的変化を示すことを発見した」と述べ、それらの変化は魚の心筋細胞が分裂を開始する前に実際に必要だったと指摘した。 「これらの類似性から、冬眠中の哺乳類の心筋細胞は増殖しようとしている細胞である可能性があると仮説を立てています。」
したがって、良いニュースは、哺乳類の心臓は、細胞分裂の前段階である一種の代謝「ダウンサイジング」を受ける可能性があるということです。 「この考えは、細胞周期調節因子の強制発現が哺乳類の心筋細胞の増殖を誘導する可能性があるという、多くのグループの発見とよく一致します」とジョプリング氏は言う。 「おそらく、彼らに必要なのは、正しい方向への少しの後押しだけなのかもしれません。」
その「推進力」を与える可能性のある要因の探索が続いている。 イズピスア・ベルモンテ氏はこの結果について楽観的だが、この研究は成熟細胞が再生に寄与する可能性がある潜在的な貢献を見落とさないよう研究者に警告すべきだとも感じている。 「分化した細胞を分化プロセスの静的なエンドポイントとみなすことはもはやできません」と、CMRB の所長でもあるイズピスア ベルモンテ氏は言います。 「ゼブラフィッシュで起こっていることを哺乳類の細胞で模倣できれば、おそらくヒトでは再生が起こらない理由を理解できるかもしれません。」
この研究には、スペインの CMRB の Merce Marti 博士、Angel Raya 医学博士、Edward Sleep および Marina Raya も貢献しました。
この研究は、Fundacion Cellex、Ipsen Foundation、G. Harold and Leila Y. Mathers Charitable Foundation、National Institutes of Health、およびサノフィ・アベンティスから一部資金提供を受けました。
-エリーズ・ラマー
ソーク生物学研究所について
ソーク生物学研究所は世界有数の基礎研究機関の XNUMX つであり、国際的に有名な教員がユニークで協力的かつ創造的な環境で生命科学の基礎的な疑問を研究しています。 ソークの科学者は、発見と次世代の研究者の指導の両方に重点を置き、神経科学、遺伝学、細胞生物学、植物生物学、および関連分野を研究することで、がん、老化、アルツハイマー病、糖尿病、感染症の理解に画期的な貢献をしています。
教員の功績は、ノーベル賞や全米科学アカデミーの会員など、数多くの栄誉によって認められています。 ポリオワクチンの先駆者であるジョナス・ソーク医学博士によって 1960 年に設立されたこの研究所は、独立した非営利団体であり、建築上のランドマークでもあります。
通信局
電話:(858)453-4100
press@salk.edu