
2015 年 10 月 8 日
この新しい技術により、科学者は人間の患者から採取した細胞を使ってアルツハイマー病やパーキンソン病などの病気を研究できるようになります。
ラホヤ – 研究者らは初めて、細胞内の若さの時計を最初に巻き戻すことなく、高齢患者の皮膚サンプルを使用して脳細胞を作成することができた。 高齢者の脳に見られる細胞に似た細胞を生成するこの新しい技術は、次のような加齢に関連した病気を研究する科学者にとって恩恵となるだろう。 アルツハイマー とパーキンソン病。
「これにより、年齢に関連した兆候を細胞内に保持できるため、老化が脳に及ぼす影響をより簡単に研究できるようになります」と彼は言います。 ラスティ・ゲージ、ソーク研究所の教授 遺伝学研究室 8 年 2015 月 XNUMX 日に出版された論文の上級著者 細胞幹細胞.
「この強力なアプローチを使用することで、健康的な老化だけでなく、病的な老化についても同様に、人間の神経細胞の生理機能と分子機構に関する多くの疑問に答え始めることができます。」と彼は言います。 マーティン・ヘッツァー、ソーク大学の教授もこの研究に関わっています。
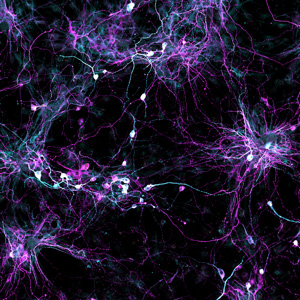
ソークの科学者たちは、患者の皮膚から老化した脳細胞を成長させる新しい技術を開発した。 高齢の人間のドナーからの線維芽細胞(結合組織の細胞)が、誘導ニューロンに直接変換されることが示されています。
こちらをクリックしてください 高解像度画像の場合。
画像: ソーク生物学研究所の提供
歴史的に、ショウジョウバエからマウスに至るまでの動物モデルは、特に脳など生きた人間から簡単に採取できない組織における老化の生物学的影響を研究するための頼りになる手法でした。 ここ数年、研究者はヒトのさまざまな病気を研究するために幹細胞に注目することが増えています。 たとえば、科学者は患者の皮膚細胞を採取して、体内のあらゆる細胞になる能力を持つ人工多能性幹細胞に変えることができます。 そこから、研究者はさらなる研究のために幹細胞を脳細胞に変化させることができます。 しかし、このプロセスは、高齢の人間から皮膚細胞を採取する場合でも、「古い」性質を持つ幹細胞を保証するものではありません。
「研究者がこれらの細胞をさらに使い始めると、幹細胞を作るための再プログラミングの過程で、細胞が他の方法でも若返ることが明らかになりました」と、博士研究員で新しい論文の筆頭著者であるジェローム・メルテンスは言う。
古い細胞のエピジェネティックなサイン(どの遺伝子がいつ発現するかを決定する DNA 上の化学マークのパターン)は、その過程で若いサインと一致するようにリセットされました。 このアプローチでは研究者が「古い」脳細胞を作り出すことができなかったため、人間の脳の老化を研究することが困難になりました。
Gage、Hetzer、Mertensらは、別のアプローチを試みることに決め、皮膚細胞を直接ニューロンに変換し、いわゆる誘導ニューロンを作成できるさらに新しい技術に目を向けた。 「数年前、研究者らは幹細胞前駆体の状態を完全に回避してこれが可能であることを示しました」とメルテンス氏は言う。
科学者らは、誕生から19歳までの89人から皮膚細胞を収集し、人工多能性幹細胞技術と直接変換アプローチの両方を使用して脳細胞への変化を促した。 次に、得られたニューロンにおける遺伝子発現のパターンを、解剖した脳から採取した細胞と比較しました。
人工多能性幹細胞法を使用した場合、予想どおり、若い由来のサンプルと古い由来のサンプルの間でニューロンのパターンが区別できませんでした。 しかし、直接変換技術を使用して作成された脳細胞は、若いドナーから作成されたか高齢者から作成されたかに応じて、異なる遺伝子発現パターンを示しました。
「私たちが抽出したニューロンは、ドナーの年齢に応じた違いを示しました」とメルテンス氏は言います。 「そして、それらは実際に、これまで脳の老化に関係していると考えられていた遺伝子発現の変化を示しています。」 たとえば、RanBP17と呼ばれる核孔タンパク質(その減少は神経変性疾患の一因となる核輸送欠陥に関連している)のレベルは、高齢の患者由来のニューロンでは低かった。
皮膚細胞からニューロンへの直接変換がこれらの年齢の特徴を保持することが示された今、ゲージ氏は、この技術が老化を研究するための貴重なツールになることを期待している。 また、今回の研究は脳細胞の作成における有効性をテストしただけだが、同様の方法で老化した心臓や肝臓の細胞も作成できるようになるのではないかと同氏は疑っている。
この研究の他の研究者は、Apua CM Paquola、Manching Ku、Emily Hatch、Lena Bohnke、Shauheen Ladjevardi、Sean McGrath、Benjamin Campbell、Hyungjun Lee、Joseph R. Hardy、J. Tiago Goncalves、戸田智久、およびソーク研究所の Yongsung Kim でした。 ; フリードリヒ・アレクサンダー大学エアランゲン・ニュルンベルク校のユルゲン・ヴィンクラー氏。 と清ハウ大学の姚淳氏。
この研究と関与した研究者は、 G. ハロルド & レイラ Y. マザーズ慈善財団 JPB財団 レオナM.とハリーB.ヘルムズリー慈善信託アネット・マール=スミス、 サーム ドイツ連邦教育研究省 と グレン医学研究財団.
ジャーナル
細胞幹細胞
作者
ジェローム・メルテンス、アプア・CM・パコラ、マンチング・クー、エミリー・ハッチ、レナ・ボーンケ、シャウヒーン・ラジェヴァルディ、ショーン・マクグラス、ベンジャミン・キャンベル、ヒョンジュン・リー、ジョセフ・R・ハーディ、J・ティアゴ・ゴンサルベス、戸田智久、キム・ヨンソン、ユルゲン・ウィンクラー、ヤオ・ジュン、マーティン・ヘッツァー、フレッド・H・ゲージ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。