
2015 年 4 月 30 日
早老症候群に関するソーク研究所の発見は、老化プロセスを遅らせたり逆転させたりする方法につながる可能性がある
早老症候群に関するソーク研究所の発見は、老化プロセスを遅らせたり逆転させたりする方法につながる可能性がある
ラホヤ – 30 年 2015 月 XNUMX 日の記事で詳述されているように、老化のプロセスを細胞 DNA の密集した束の劣化と結びつける研究は、がん、糖尿病、アルツハイマー病などの加齢に関連した病気の予防と治療方法につながる可能性があります。 科学.
この研究では、ソーク研究所と 中国科学院 彼らは、早期老化と死につながる疾患であるウェルナー症候群の根底にある遺伝子変異が、ヘテロクロマチンとして知られる DNA の束の劣化を引き起こすことを発見しました。
この発見は、最先端の幹細胞技術と遺伝子編集技術の組み合わせによって可能となり、ヘテロクロマチンの損傷を予防または回復することにより、加齢に伴う生理学的衰えに対抗する方法につながる可能性がある。
「私たちの研究結果は、ウェルナー症候群を引き起こす遺伝子変異がヘテロクロマチンの組織化を引き起こし、この正常な DNA パッケージングの破壊が老化の主な要因であることを示しています」と述べています。 フアン・カルロス・イズピスア・ベルモンテ、この論文の上級著者。 「これは、老化の中心的なメカニズムであるヘテロクロマチンの組織の乱れを特定するものであり、可逆的であることが示されているため、ウェルナー症候群を超えた意味を持っています。」
ウェルナー症候群は、通常よりも急速に老化を引き起こす遺伝性疾患です。 米国では約200,000万人に2人が罹患しています。 この障害を持つ人々は、白内障、40型糖尿病、動脈硬化、骨粗鬆症、がんなどの加齢に伴う病気を若くして患い、ほとんどが50代後半からXNUMX代前半で死亡します。
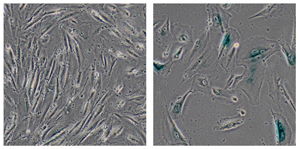
ソーク研究所の研究者らは、若年性老化障害であるウェルナー症候群で変異したタンパク質が、DNAが密にパッケージされた形態であるヘテロクロマチンの安定化に重要な役割を果たしていることを発見した。 より一般的には、この研究結果は、ヘテロクロマチンの組織の乱れが老化の主な要因である可能性を示唆しています。 この画像は、正常なヒト細胞(左)と、ウェルナー症候群をモデル化するためにソークの科学者によって開発された遺伝子組み換え細胞(右)を示しており、サイズが大きいなど老化の兆候が見られました。
こちらをクリックしてください 高解像度画像の場合。
画像: ソーク生物学研究所の提供
この疾患は、WRN タンパク質を生成するウェルナー症候群 RecQ ヘリカーゼ様遺伝子 (略して WRN 遺伝子として知られる) の変異によって引き起こされます。 これまでの研究では、このタンパク質の通常の形態は、人の DNA の構造と完全性を維持する酵素であることが示されています。 ウェルナー症候群でこのタンパク質が変異すると、DNAの複製と修復、遺伝子の発現が障害され、これが早期老化の原因となると考えられていた。 しかし、変異した WRN タンパク質がこれらの重要な細胞プロセスをどのように混乱させるのかは正確には不明でした。
研究の中で、ソークの科学者らは、変異した WRN タンパク質がどのようにしてこれほど多くの細胞混乱を引き起こすのかを正確に解明しようと努めた。 これを行うために、彼らは最先端の遺伝子編集技術を使用してヒト幹細胞のWRN遺伝子を削除することにより、ウェルナー症候群の細胞モデルを作成しました。 この疾患の幹細胞モデルにより、研究者らは研究室で急速に老化する細胞を研究する前例のない能力を得ることができました。 得られた細胞は、実際のウェルナー症候群患者に見られる遺伝子変異を模倣したため、細胞は通常よりも急速に老化し始めました。 詳細な検査により、科学者らは、WRN 遺伝子の欠失が、細胞の核に見られる密に詰まった DNA であるヘテロクロマチンの構造の破壊にもつながることを発見しました。
この DNA の束は、遺伝子の活性を制御するスイッチボードとして機能し、細胞の複雑な分子機構を制御します。 ヘテロクロマチンの束の外側には、ヘテロクロマチンの構造を制御するエピジェネティック タグとして知られる化学マーカーがあります。 たとえば、これらの化学スイッチを変更すると、ヘテロクロマチンの構造が変化し、遺伝子が発現または抑制される可能性があります。

左から:プラディープ・レディ、コンセプシオン・ロドリゲス・エステバン、鈴木えみ、モー・リー、フアン・カルロス・イズピスア・ベルモンテ、アレハンドロ・オカンポ、鈴木圭一郎
こちらをクリックしてください 高解像度画像の場合。
画像: ソーク生物学研究所の提供
ソークの研究者らは、WRN 遺伝子の欠失がヘテロクロマチンの破壊につながることを発見し、ヘテロクロマチンの維持における WRN タンパク質の重要な役割を指摘しました。 そして実際、さらなる実験で、このタンパク質がヘテロクロマチンを安定化することが知られている分子構造と直接相互作用することを示し、突然変異したWRNタンパク質とヘテロクロマチンの不安定化を直接結びつける一種の決定銃のようなものを初めて明らかにした。
「私たちの研究は、ウェルナー症候群とヘテロクロマチンの組織化の間の点を結びつけ、遺伝子変異がエピジェネティックな制御を破壊することによって細胞プロセスの全体的な破壊を引き起こす分子メカニズムを概説しています」とイズピスア・ベルモンテは言う。 「より広範には、ヘテロクロマチン構造の蓄積された変化が細胞老化の主な根本原因である可能性があることを示唆しています。 このことから、古い家や車を改造するような改造を元に戻して、加齢に伴う衰えや病気を予防、あるいは元に戻すことができるかどうかという疑問が生じます。」
イズピスア・ベルモンテ教授は、老化におけるヘテロクロマチンの崩壊の役割を完全に理解するには、テロメアとして知られる染色体の末端の短縮など、老化に関係する他の細胞プロセスとヘテロクロマチンの崩壊がどのように相互作用するかなど、より広範な研究が必要であると付け加えた。 さらに、イズピスア ベルモンテのチームは、人間の老化や病気に関与するエピジェネティックな変化を逆転させるためのエピジェネティック編集技術を開発しています。
この論文の他の著者: Weiqi Zhang、Jingyi Li、鈴木慶一郎、Jing Qu、Ping Wang、Junzhi Zhou、Xiaomeng Liu、Ruotong Ren、Xiuling Xu、Alejandro Ocampo、Tingting Yuan、Jiping Yang、Ying Li、Liang Shi、Dee が含まれます。 Guan、Huize Pan、Shunlei Duan、Zhichao Ding、Mo Li、Fei Yi、Ruijun Bai、Yayu Wang、Chang Chen、Fuquan Yang、Xiaoyu Li、Zimei Wang、相沢恵美、April Goebl、Rupa Devi Soligalla、Pradeep Reddy、Concepcion Rodriguezエステバン、唐フーチョウ、劉光輝。
研究への資金提供は、 グレン財団 G. ハロルド & レイラ Y. マザーズ慈善財団 と レオナM.とハリーB.ヘルムズリー慈善信託.
ソーク生物学研究所について:
ソーク生物学研究所は世界有数の基礎研究機関の XNUMX つであり、国際的に有名な教員がユニークで協力的かつ創造的な環境で生命科学の基礎的な疑問を研究しています。 ソークの科学者は、発見と次世代の研究者の指導の両方に重点を置き、神経科学、遺伝学、細胞生物学、植物生物学、および関連分野を研究することで、がん、老化、アルツハイマー病、糖尿病、感染症の理解に画期的な貢献を行っています。
教員の功績は、ノーベル賞や全米科学アカデミーの会員など、数多くの栄誉によって認められています。 ポリオワクチンの先駆者であるジョナス・ソーク医学博士によって 1960 年に設立されたこの研究所は、独立した非営利団体であり、建築上のランドマークでもあります。
ジャーナル
科学
作者
Weiqi Zhang、Jingyi Li、鈴木慶一郎、Jing Qu、Ping Wang、Junzhi Zhou、Xiaomeng Liu、Ruotong Ren、Xiuling Xu、Alejandro Ocampo、Tingting Yuan、Jijiping Yang、Ying Li、Liang Shi、Dee Guan、Huize Pan、Shunlei Duan 、Zhichao Ding、Mo Li、Fei Yi、Ruijun Bai、Yayu Wang、Chang Chen、Fuquan Yang、Xiaoyu Li、Zimei Wang、相沢恵美、April Goebl、Rupa Devi Soligalla、Pradeep Reddy、Concepcion Rodriguez Esteban、Fuchou Tang、Guang-ホイ・リュー、フアン・カルロス・イズピスア・ベルモンテ
通信局
電話:(858)453-4100
press@salk.edu