
2012 年 2 月 3 日
ソーク研究者らは、成人の脳には生涯続くタンパク質が含まれていることを発見した
ソーク研究者らは、成人の脳には生涯続くタンパク質が含まれていることを発見した
カリフォルニア州ラホヤ発-生物学における大きな謎のXNUMXつは、なぜ細胞が老化するのかということだ。 今回、ソーク生物学研究所の科学者らは、脳内で老化プロセスがどのように起こるかを説明できる可能性のある脳細胞の構成要素の弱点を発見したと報告している。
研究者らは、ニューロンの核の表面にある超長寿命タンパク質(ELLP)と呼ばれる特定のタンパク質が、驚くほど長い寿命を持っていることを発見した。
ほとんどのタンパク質の寿命は合計 XNUMX 日以下ですが、ソークは
研究所の研究者らは、ラットの脳内に同じくらい古いELLPを特定した
彼らが報告した発見は、生物として 科学.
ソークの科学者たちは、この時代のタンパク質を構成要素とする重要な細胞内機械を初めて発見した。 彼らの結果は、タンパク質が交換されることなく一生続くことを示唆しています。
ELLP は核の表面の輸送チャネルを構成します。 どの物質が出入りするかを制御するゲート。 これらのタンパク質が時間の経過とともに経験する磨耗がなければ、その長寿命は利点である可能性があります。 体内の他のタンパク質とは異なり、ELLP は異常な化学修飾やその他の損傷を受けても置換されません。
ELLPが損傷すると、細胞の核を毒素から守るこれらのタンパク質で構成される三次元輸送チャネルの能力が弱まるという。 マーティン・ヘッツァー、ソーク大学の教授 分子細胞生物学研究室、研究を率いました。 これらの毒素は細胞の DNA を変化させ、それによって遺伝子の活性を変化させ、細胞の老化を引き起こす可能性があります。
によって資金を供給された エリソン医療財団 と グレン医学研究財団, ヘッツァーの研究グループは、老化プロセスにおける核孔複合体(NPC)と呼ばれるこれらの輸送チャネルの役割を研究している世界で唯一の研究室です。
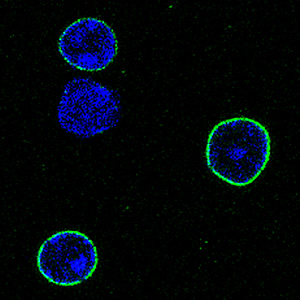
この顕微鏡画像は、ラットの脳細胞の核の外側で緑色に光る、非常に長命なタンパク質、つまり ELLP を示しています。 核内の DNA は青色で描かれています。
ソークの科学者らは、核の壁を通るチャネルを形成するELLPが交換されずにXNUMX年以上持続することを発見した。 これらのタンパク質が劣化すると、毒素が核に侵入し、細胞の老化が引き起こされる可能性があります。
画像: ブランドン遠山氏提供、ソーク生物学研究所
これまでの研究により、遺伝子発現の変化が老化プロセスの根底にあることが明らかになっている。 しかし、ヘッツァー研究室が、哺乳類のNPCがDNAに損傷を与える毒素の核への侵入を可能にするアキレス腱を持っていることを発見するまで、科学界はこれらの遺伝子変化がどのように起こるのかについて確かな手がかりをほとんど持っていなかった。
「老化の基本的な特徴は、心臓や脳などのさまざまな臓器の機能能力が全体的に低下することです」とヘッツァー氏は言います。 「この低下は、それらの臓器を構成する細胞内の恒常性、つまり内部安定性の低下に起因します。 いくつかの研究室での最近の研究では、タンパク質恒常性の破壊と細胞機能の低下が関連付けられています。」
ヘッツァーと彼のチームが本日報告した結果は、ニューロン機能の低下は時間の経過による損傷の結果として劣化するELLPに起因する可能性があることを示唆しています。
「ニューロンではなく、ほとんどの細胞は、タンパク質の代謝回転のプロセスを通じて、タンパク質構成要素の機能低下と闘っています。このプロセスでは、タンパク質の潜在的に障害のある部分が新しい機能的コピーに置き換えられます」とヘッツァー氏は言う。
「私たちの結果はまた、核孔の劣化が、若々しい遺伝子発現プログラムの喪失など、加齢に伴う核機能の欠陥につながる一般的な老化メカニズムである可能性があることを示唆しています」と彼は付け加えた。
この発見は、老化やアルツハイマー病やパーキンソン病などの神経変性疾患の分子的起源の理解に関連する可能性がある。
以前の研究で、ヘッツァーと彼のチームは、老マウスとラットのニューロンの核内に大きなフィラメントを発見し、その起源を細胞質まで追跡しました。 このようなフィラメントは、パーキンソン病を含むさまざまな神経障害と関連付けられています。 間違って配置された分子が病気の原因なのか結果なのかはまだ判明していません。
また、ヘッツァーと彼のチームは、以前の研究で、人間生物学の実験室モデルである健康な老化ラットのニューロンにおけるNPCの機能が年齢に依存して低下することを記録した。
ヘッツァー氏のチームには、ソーク研究所の同僚のほか、スクリップス研究所の化学生理学部門の教授であるジョン・イェーツ三世氏も含まれている。 この研究の共同筆頭著者は、ヘッツァーの研究室の博士研究員であるブランドン・H・トヤマと、イェーツの研究室の博士研究員であるジェフリー・N・サバスでした。
ヘッツァー博士がXNUMX年前、老化や特定の神経変性疾患の発症にNPCが関与しているのか、あるいは発症に寄与しているのかを調査することを決めたとき、科学界の一部のメンバーは、そのような研究は大胆すぎるし、実施するのは困難で費用もかかるだろうと彼に警告した。行為。 しかしヘッツァーは警告にもかかわらず決意を固めた。
同氏は、財団の資金提供がなければ、研究結果が一流雑誌に掲載されるほど研究は進展しなかったであろうと付け加えた。
ソーク生物学研究所について:
ソーク生物学研究所は世界有数の基礎研究機関の XNUMX つであり、国際的に有名な教員がユニークで協力的かつ創造的な環境で生命科学の基礎的な疑問を研究しています。 ソークの科学者は、発見と次世代の研究者の指導の両方に重点を置き、神経科学、遺伝学、細胞生物学、植物生物学、および関連分野を研究することで、がん、老化、アルツハイマー病、糖尿病、感染症の理解に画期的な貢献をしています。
教員の功績は、ノーベル賞や全米科学アカデミーの会員など、数多くの栄誉によって認められています。 ポリオワクチンの先駆者であるジョナス・ソーク医学博士によって 1960 年に設立されたこの研究所は、独立した非営利団体であり、建築上のランドマークでもあります。
詳細については:
科学
著者: ジェフリー・N・サバス、ブランドン・H・トヤマ、タオ・シュー、ジョン・R・イェーツ、マーティン・W・ヘッツァー
ラットの脳における極めて長寿命の核孔タンパク質
ジャーナル
科学
TITLE
作者
ジェフリー・N・サバス、ブランドン・H・トヤマ、タオ・シュー、ジョン・R・イェーツ、マーティン・W・ヘッツァー
通信局
電話:(858)453-4100
press@salk.edu