
2016 年 11 月 16 日
ソークの研究者らは、非分裂細胞の特定の位置に DNA を配置する方法を初めて発見した
ソークの研究者らは、非分裂細胞の特定の位置に DNA を配置する方法を初めて発見した
ラホヤ-ソーク研究所の研究者らは、遺伝子編集の聖杯、つまり成人の器官や組織の大部分を構成する非分裂細胞の標的位置にDNAを挿入する能力を初めて発見した。 研究チームが示したこの技術は、盲目のげっ歯類の視覚反応を部分的に回復することができ、基礎研究や網膜、心臓、神経疾患などのさまざまな治療に新たな道を開くことになる。
「私たちが発見したテクノロジーには非常に興奮しています。なぜなら、これは以前には実現できなかったことだからです」と氏は言います。 フアン・カルロス・イズピスア・ベルモンテ、ソークの遺伝子発現研究所の教授であり、16 年 2016 月 XNUMX 日に出版された論文の上級著者です。 自然。 「初めて、分裂しない細胞に侵入し、意のままにDNAを改変できるようになりました。 この発見の応用可能性は膨大です。」
これまで、CRISPR-Cas9 システムなどの DNA 修飾技術は、細胞の通常のコピー機構を利用して皮膚や腸などの細胞を分割するのに最も効果的でした。 新しいソーク技術は、分裂細胞の培養物に新しい DNA を組み込む際に他の方法よりも XNUMX 倍効率的であり、研究と医療の両方にとって有望なツールとなっています。 しかし、より重要なことは、ソーク技術は、科学者が目、脳、膵臓、心臓など、分裂しなくなった成人細胞の正確な DNA 位置に新しい遺伝子を挿入することに初めて成功したことを意味し、新しい可能性を提供するものである。これらの細胞における治療への応用。
これを達成するために、ソークの研究者らは、元の鎖末端を再結合することによって日常的な DNA 切断を修復する、NHEJ (「非相同末端結合」の略) と呼ばれる DNA 修復細胞経路をターゲットにしました。 彼らはこのプロセスと既存の遺伝子編集技術を組み合わせて、非分裂細胞の正確な位置に新しい DNA を配置することに成功した。
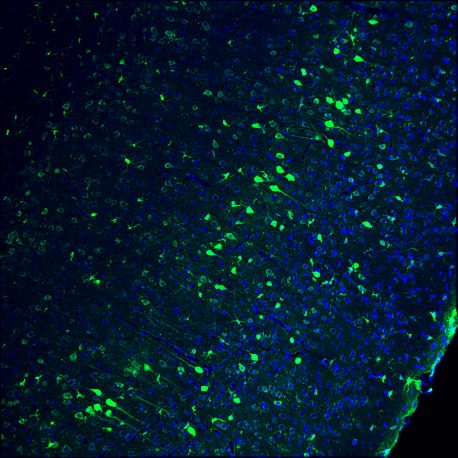
こちらをクリックしてください 高解像度の画像の場合
クレジット:Salk Institute
「このNHEJ経路を利用してまったく新しいDNAを挿入することは、生きた成体生物のゲノム編集にとって革命的です」と、イズピスア・ベルモンテ研究室の上級研究員で論文の筆頭著者の一人である鈴木圭一郎氏は言う。 「これまで誰もこれをやったことがありません。」
まず、ソーク チームは、CRISPR-Cas9 システムで使用するための NHEJ 機構の最適化に取り組みました。これにより、ゲノム内の非常に正確な位置に DNA を挿入できるようになります。 研究チームは、核酸カクテルで構成されるカスタム挿入パッケージを作成しました。これを彼らは HITI (相同性非依存性標的組み込み) と呼んでいます。 次に、不活性ウイルスを使用して、HITI の遺伝子命令パッケージをヒト ES 細胞由来のニューロンに伝達しました。
「これは、HITI が非分裂細胞で機能する可能性があることを示す最初の兆候でした」とスタッフサイエンティストで共同筆頭著者の Jun Wu 氏は述べています。 この偉業を達成して、チームは成体マウスの脳にその構築物を送り込むことに成功しました。 最後に、遺伝子置換療法にHITIを使用する可能性を探るため、研究チームはヒトの失明の原因となる遺伝性網膜変性疾患である網膜色素変性症のラットモデルでこの技術をテストした。 今回、研究チームはHITIを利用して、網膜色素変性症で損傷を受ける遺伝子の3つであるMerctkの機能的コピーを生後8週間のラットの目に送達した。 ラットがXNUMX週齢のときに行われた分析では、ラットが光に反応することができ、網膜細胞の治癒を示すいくつかのテストに合格したことが示されました。
「私たちはこれらの盲目のラットの視力を改善することができました」と共同筆頭著者であり、ソークの研究員であるレイナ・ヘルナンデス・ベニテスは言う。 「この初期の成功は、このテクノロジーが非常に有望であることを示しています。」
チームの次のステップは、HITI 構造の配信効率を向上させることです。 すべてのゲノム編集技術と同様に、新しい DNA を組み込むのに十分な細胞を入手することは困難です。 HITI テクノロジーの利点は、CRISPR-Cas9 だけでなく、あらゆる標的ゲノム工学システムに適応できることです。 したがって、これらのシステムの安全性と効率が向上するにつれて、HITI の有用性も向上します。

こちらをクリックしてください 高解像度画像の場合。
クレジット:Salk Institute
「私たちは現在、分裂していない細胞の DNA を改変し、脳、心臓、肝臓の壊れた遺伝子を修復できる技術を手に入れました」とイズピスア ベルモンテ氏は言います。 「これにより、これまでできなかった病気を治すという夢を初めて見ることができるようになり、とても興奮しています。」
この研究に参加した他の研究者は、Euiseok J. Kim、畑中文之、山本真子、荒岡利和、栗田正和、菱田智明、モー・リー、相沢恵美、エイプリル・ゲーブル、ルパ・デヴィ・ソリガラ、コンセプシオン・ロドリゲス・エステバン、トラビス・バーググレン、エドワード・M・キャロウェイであった。ソーク研究所の。 恒川祐司さんと松崎文雄さん 理化学研究所発生・再生科学研究センター; ピエール・マジストレッティ キングアブドラ科学技術大学; Jie Zhu、Tingshuai Jiang、Xin Fu、Maryam Jafari、Kang Zhang の シャイリー・アイ・インスティテュート の三脚と ゲノム医学研究所, カリフォルニア大学サンディエゴ校; Zhe Li、Shicheng Guo、Song Chen、Kun Zhang の カリフォルニア大学サンディエゴ校医学工学研究所; Jing Qu と Guang-Hui Liu の 中国科学院; ヘロニモ・ラハラ、エストレージャ・ヌニェス、ペドロ・ギレン サンアントニオ・デ・ムルシア・カトリカ大学; とジョセップ・M・カンピストル バルセロナ大学.
この研究と関与した研究者は部分的に次の支援を受けました。 国立衛生研究所, レオナM.とハリーB.ヘルムズリー慈善信託 G. ハロルド & レイラ Y. マザーズ慈善財団, マックナイト財団, モクシー財団 ペドロ・ギレン博士財団 の三脚と サンアントニオ・デ・ムルシア・カトリカ大学、スペイン.
ジャーナル
自然
作者
鈴木圭一郎、恒川祐司、レイナ・ヘルナンデス=ベニテス、Jun Wu、Jie Zhu、Euiseok J. Kim、畑中史之、山本真子、荒岡俊和、Zhe Li、栗田正和、菱田智章、Mo Li、相澤絵美、Shicheng Guo、Songチェン、エイプリル・ゲーブル、ルパ・デヴィ・ソリガラ、ジン・クー、ティンシュアイ・ジャン、シン・フー、マリアム・ジャファリ、コンセプシオン・ロドリゲス・エステバン、トラヴィス・バーググレン、ジェロニモ・ラハラ、エストレリャ・ヌニェス、ペドロ・ギレン、ジョセップ・M・カンピストル、松崎文夫、グァン・ホイ・リウ、ピエール・マジストレッティ、クン・チャン、エドワード・M・キャロウェイ、カン・ジャン、フアン・カルロス・イズピスア・ベルモンテ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。