
2009 年 9 月 30 日
カリフォルニア州ラホヤ—臍帯血細胞は胚性幹細胞のように機能するように再プログラムすることに成功し、組織適合性のある臍帯血由来の人工多能性幹(iPS)細胞の包括的なバンクを作成する基礎となる。 -棚のアプリケーション、スペインのバルセロナにあるソーク生物学研究所および再生医療センターの研究者を報告します。
「臍帯血幹細胞は、簡単に入手でき、免疫学的に未熟で、すぐに胚性幹細胞のような状態に戻るため、安全で「すぐに使える」iPS 細胞の生成源として機能する可能性があります。」 フアン=カルロス・イズピスア・ベルモンテ、博士、ソーク遺伝子発現研究所の教授、ジャーナルのXNUMX月号に掲載された研究を主導 セルステムセル。
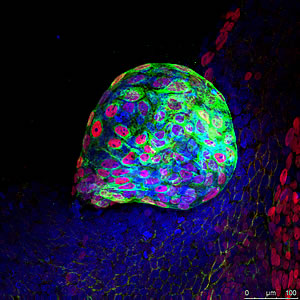
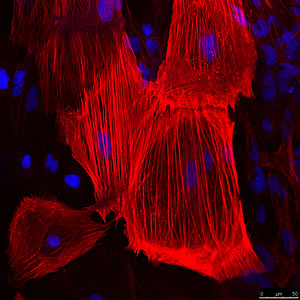
上: 内胚葉層は、ここではマーカー AFP および FoxA2 によって識別され、消化管、肺、膀胱を形成します。
下: ここではASMによって特定された中胚葉層は、骨、筋肉、結合組織、および皮膚の中間層を形成します。
世界中ですでに 400,000 個を超える臍帯血が免疫学的情報とともに保管されています。 臍帯血に含まれる細胞は、その起源が初期であるため、最小限の体細胞変異を含み、新生児細胞の免疫学的未熟性を備えているため、移植に対する免疫拒絶のリスクなしに、HLA ドナーとレシピエントの一致が完全とは言えません。
ヒト白血球抗原 (HLA) タイピングは、骨髄または臍帯血移植の患者とドナーを照合するために使用されます。 HLA は体内のほとんどの細胞に見られる特別な表面マーカーであり、免疫システムが「自己」と「非自己」を区別するのに役立ちます。 「すでにバンクされている臍帯血ユニットの中から一般的な HLA ハプロタイプを選択して iPS 細胞を作成すれば、人口の大部分に HLA 一致を提供するために必要な細胞株の数が大幅に削減されます」と Izpisúa Belmonte 氏は言います。
最初の成人細胞が iPS 細胞に変換されて以来、それらは胚性幹細胞に代わる議論の余地のない代替物として、また患者固有の幹細胞の潜在的な供給源として多くの興奮を引き起こしました。 残念ながら、患者の細胞を過去に戻すことは費用がかかるだけでなく、損傷した脊髄の修復や急性疾患の治療にそれらの細胞がすぐに必要な場合には困難になる可能性があり、また加齢や慢性疾患の影響により回復不能な損傷を受けた場合には全く不可能です。体細胞のプール。
「患者固有の iPS 株は、理論的には組織を再生するための理想的な臨床選択肢として提唱されてきましたが、実用的かつ費用対効果の観点から、このアプローチは実現可能ではない可能性があります」と Izpisúa Belmonte 氏は言います。 同氏は、「公的に利用可能なネットワークで臍帯血由来 iPS 株の大規模な生産と保存が、将来の臨床応用の実行可能な選択肢となる可能性がある」と期待している。
これを念頭に置いて、ベルモンテ氏らは臍帯血から単離した造血幹細胞をiPS細胞に変換することに着手した。 彼らは、最も一般的に使用される 4 つの要素のうちの 2 つ (OCTXNUMX と SOXXNUMX) のみを使用して変換に成功しただけでなく、これまでに公開された他の方法論よりも短い時間で変換することもできました。 研究者らが新たに採取した臍帯血から始めたのか、以前に凍結したサンプルから始めたのかに関係なく、得られたiPS細胞はヒト胚性幹細胞と区別できませんでした。
「再プログラミングに使用される臍帯血細胞の集団は、他の成人の体細胞に見られるものよりも高いレベルで再プログラミング/幹細胞因子を発現しています。これが、なぜ臍帯血細胞がより少ない因子でより短い時間で再プログラムできるのかを説明できる可能性があります」とイズピスア・ベルモンテ氏は言う。 。 「彼らはすでに半分まで到達しているようです。」
さらに、臍帯血由来の iPS 細胞、略して CBiPS 細胞は、多能性に関するすべての標準検査に合格しました。奇形腫として知られる幹細胞腫瘍が生じ、リズミカルに拍動する心筋細胞やドーパミンを含む XNUMX つの胚組織層の派生細胞に分化しました。 -ニューロンを生成します。
イズピスア・ベルモンテ氏の次の目標は、人間の臨床応用に安全と考えられる方法を使用して、臍帯血細胞に時間を燃やしてもらうことです。 ベルモンテ氏と彼のチームが使用したものも含め、iPS 細胞を作製するための元のプロトコールは、外来の「再プログラミング」遺伝子を宿主細胞のゲノムに組み込むことに依存しており、このプロセスには突然変異や iPS 後のがんの発生などのリスクが伴います。細胞移植では、その治療価値が制限されます。
しかし、研究者らは、分化した細胞を小分子にさらすだけなど、遺伝的痕跡を残さずに細胞を再プログラムできる代替方法の開発に懸命に取り組んでいる。 「いくつかの研究で、これが可能である可能性があることがすでに示されています」とイズピスア・ベルモンテ氏は言う。 「それらが臍帯血細胞にも作用することを証明できれば、iPS細胞の臨床応用に向けて確実に前進する可能性があります。 私たちは、少なくとも近い将来、この特定の細胞源であるCBiPS細胞に焦点を当てるべきです。」
この研究に貢献した研究者には、アレッサンドラ・ジョルジェティ、ヌリア・モンセラット、トロン・アーセン、フェデリコ・ゴンザレス、イグナシオ・ロドリゲス=ピサ、リタ・ヴァセナ、アンヘル・ラヤ、ステファニー・ブーエ、マリア・ホセ・バレロ、ベゴーニャ・アラン・コルベラ、アンナ・ベイガが含まれる。スペインのバルセロナとマルタ・トラバデラ、スペインのバルセロナにあるサン・イ・テイクシッツ・バル・デブロン銀行にて。
この研究は、教育省、衛生衛生省、TERCEL、Fundacion Cellex、および G. ハロルドおよびレイラ Y. マザーズ慈善財団によって部分的に支援されました。
ソーク生物学研究所について: ソーク生物学研究所は世界有数の基礎研究機関の XNUMX つであり、国際的に有名な教員がユニークで協力的かつ創造的な環境で生命科学の基礎的な疑問を研究しています。 ソークの科学者は、発見と将来世代の研究者の指導の両方に重点を置き、神経科学、遺伝学、細胞生物学、植物生物学、および関連分野を研究することで、がん、老化、アルツハイマー病、糖尿病、心血管疾患の理解に画期的な貢献を行っています。
教員の功績は、ノーベル賞や全米科学アカデミーの会員など、数多くの栄誉によって認められています。 ポリオワクチンの先駆者であるジョナス・ソーク医学博士によって 1960 年に設立されたこの研究所は、独立した非営利団体であり、建築上のランドマークでもあります。
通信局
電話:(858)453-4100
press@salk.edu