
2025 年 5 月 23 日
ソーク研究所とカリフォルニア大学サンディエゴ校の研究者らが、ダイニンとLis1タンパク質の相互作用を初めて撮影し、神経疾患の将来の医薬品開発を支援する。
ソーク研究所とカリフォルニア大学サンディエゴ校の研究者らが、ダイニンとLis1タンパク質の相互作用を初めて撮影し、神経疾患の将来の医薬品開発を支援する。
ラホヤ—私たちの細胞は、微小な高速道路と特殊なタンパク質輸送手段を利用して移動しています。 everything-細胞小器官の配置からタンパク質の指示の運搬、そして細胞内のゴミの処分まで、これらの高速道路(微小管と呼ばれる)と乗り物(モータータンパク質と呼ばれる)は、細胞の機能と生存に不可欠です。

モータータンパク質とその関連タンパク質の機能不全は、重篤な神経発達障害や神経変性疾患を引き起こす可能性があります。例えば、モータータンパク質ダイニンのパートナータンパク質であるLis1の機能不全は、まれな致死性の先天異常である滑脳症(いわゆる「滑面脳」)を引き起こす可能性があり、治療法はありません。しかし、ダイニンまたはLis1の機能を標的とし、その機能を回復させる治療法は、こうした悲惨な結果を変える可能性があります。そして、そのような治療法の開発は、ダイニンとLis1の相互作用を徹底的に理解することにかかっています。
ソーク研究所とカリフォルニア大学サンディエゴ校による新たな研究で、Lis1がダイニンを「活性化」させる様子を捉えた短い動画が撮影されました。この動画により、研究チームは16つのタンパク質が相互作用する際にとる1種類の形状を分類することができ、その中にはこれまで観察されていなかったものも含まれています。これらの知見は、薬剤がこれらのタンパク質と相互作用する可能性のある正確な部位を明らかにするため、ダイニンとLisXNUMXの機能を回復させる将来の治療薬設計の基礎となるでしょう。
調査結果はに掲載されました 自然構造および分子生物学 月23、2025に。
「私はモータータンパク質にずっと興味を持っていましたが、ダイニンは細胞の中心に向かって移動できる唯一のモータータンパク質であるため、特に興味深いです」と共同責任著者は述べています。 アグニエシュカ・ケンドリックソーク研究所の助教授である、と彼女は言います。「現在、研究室にある素晴らしいツールのおかげで、ダイニンとLis1が相互作用する様子をリアルタイムで動画に記録することができました。この段階的な連携の詳細な観察は、神経発達疾患や神経変性疾患におけるそれらの活性を回復させる方法を見つけるのに役立つでしょう。」
背景:ダイニンの解読
ダイニンは1つの同一の部分から構成され、それぞれに2) 微小管に付着する「柄」、3) ダイニンが運ぶ物質に付着する「尾」、そしてXNUMX) 移動を駆動する「モーター」が含まれています。ダイニンの物理的な動きは、歩行に似ています。モーターがATPと呼ばれる細胞燃料を消費するにつれて、柄は交互に切り離され、前方に振られ、そして下にある微小管に再び付着します。
ダイニンは核という貴重な遺伝子貯蔵庫への一方通行であるため、その活動は厳密に制御されています。何も運んでいないときは、ダイニンは微小管ハイウェイから完全に分離し、「ファイ」と呼ばれるロックされた状態で自由に浮遊しています。ケンドリック氏らはここ数年、ダイニンがどのようにして「ロック解除」されるのかを解明するために懸命に研究を重ねてきました。
これまでの研究で、Lis1は鍵のような役割を果たし、ダイニンの構造に食い込み、「カイ」と呼ばれる開いた形状に解錠することが明らかになっています。しかし、これらの知見は、ダイニンとLis1の相互作用の様々な段階を散発的に撮影した静止画像に基づいています。これらの静止画像から得られるものは多くありましたが、XNUMXつのタンパク質がどのように相互作用するかをより深く理解するには、実際にそれらを観察するしかありませんでした。
重要な発見:Lis1とダイニンの相互作用
「ダイニンとLis1を画像化する私たちのアプローチは、このタンパク質に関するこれまでのどの研究よりも包括的です」と、共同責任著者でカリフォルニア大学サンディエゴ校の教授であるアンドレス・レシュツィナー氏は述べています。「写真ではなく動画を撮影することで、ダイニンがLis16と相互作用する際にとる3の詳細な1D形状を確認しました。そのうちのいくつかは、私たちの研究に全く独自のものです。」
研究チームは、ダイニンとLis1を捉えるために酵母モデルを用いました。これは、ヒト細胞とは異なり、酵母細胞はダイニンとLis1のレベルが変化しても生存できるためです。また、ダイニンの構造はヒト細胞と酵母細胞で機能的に同一であるため、酵母ダイニンについて得られた知見はヒトダイニンにも応用できます。
研究者らはこの酵母モデルを用いて、ダイニンとLis1を単離し、温度を大幅に下げることでダイニンの活動を減速させた。その後、時間分解クライオ電子顕微鏡(クライオEM)を用いて、ダイニンがLis3と相互作用する様子を高解像度の1D動画で撮影し、ダイニンのPhi(ロック)状態とChi(アンロック)状態の間のタイムラインを再現することに成功した。
クライオ電子顕微鏡(クライオEM)は、電子ビームを用いて分子の3D画像を原子レベルの細部まで構築する技術です。これまでの研究では、クライオ電子顕微鏡やその他の画像化手法を用いて、ダイニンのロック状態とロック解除状態の画像を構築してきました。 時間分解 しかし、このコンポーネントは新しいものです。単一の時点における単一の構造を捉えるのではなく、時間分解キャプチャでは、時間の経過に伴う異なる構造を特定し、動画を作成します。これにより、ソークとカリフォルニア大学サンディエゴ校の科学者たちは、ダイニンの構造における1秒未満の変化を追跡し、ロック状態からロック解除状態への移行プロセスを段階的に説明することができました。
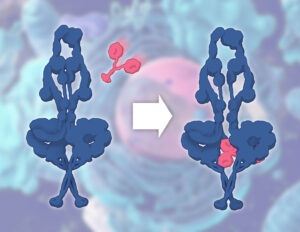
新しいビデオでは、ダイニンを活性化する最初のステップとして、Lis1がダイニンのモーターサブユニットに結合していることが示されています。ダイニンと同様に、Lis1も1つの同一の部分から構成されています。この最初の相互作用では、LisXNUMXの片方がダイニンに結合し、ダイニンのロック状態を解除してモーターを始動させます。これにより、自然界のエネルギー分子であるATPをより迅速かつ効率的に利用できるようになります。このATPを燃料とするエンジンの始動は、ダイニンが細胞内の微小管ハイウェイを移動するための鍵となります。
次に、Lis1のもう一方の半分がダイニンに付着します。今度は柄の部分です。この1回目のLisXNUMXの相互作用により活性化が完了し、ダイニンのカイ状態が固定されます。また、ダイニンの運動活性をさらに高め、活動への準備を整えます。
将来展望:発達障害および神経疾患におけるLis1およびダイニン機能不全の修復
「これらの発見は、Lis1の機能不全がなぜダイニンの活動にそれほど壊滅的な影響を及ぼすのか、そしてそれが将来的にどのように発達障害や神経疾患に寄与するのかを理解する上で、これまで以上に近づくものであることは間違いありません」とケンドリック氏は言う。
ダイニンとLis3に関する新たな高解像度1D構造の知見は、神経発達疾患および神経変性疾患におけるこれらの機能不全の治療への道を開く可能性があります。今後の研究では、Lis1の様々な変異がダイニンとの相互作用にどのような影響を与えるか、そしてそれが滑脳症やその他の希少遺伝性疾患にどのように寄与するかを解明できる可能性があります。最終的には、これらXNUMXつのタンパク質の物理的構造に関する知見が深まるほど、それらの構造に「適合」し、その活性を回復させる薬剤の開発が容易になります。
この論文の詳細
他の著者には、カリフォルニア大学サンディエゴ校のケンドリック・グエン、エヴァ・カラスマニス、ロミー・アマロが含まれます。カリフォルニア大学サンディエゴ校とハワード・ヒューズ医学研究所のサマラ・レック・ピーターソン氏。とバーモント大学のウェン・マー氏。
この研究は、アメリカがん協会(PF-18-190-01-CCG)、国立衛生研究所(P30 CA014195、T32 GM139795、R01 GM107214、R35 GM145296、R35 GM141825)、バーモント心臓血管研究所、ジェーン・コフィン・チャイルズ博士研究員、ハワード・ヒューズ医学研究所の支援を受けて実施されました。
DOI: 10.1038 / s41594-025-01558-w
ジャーナル
自然構造および分子生物学
作者
アグニエシュカ・A・ケンドリック、ケンドリック・H・V・グエン、ウェン・マー、エヴァ・P・カラスマニス、ロミー・E・アマロ、サマラ・L・レック=ピーターソン、アンドレス・E・レシュツィナー
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。