
2008 年 12 月 3 日
カリフォルニア州ラホーヤ — 長い間単なる傍観者だと考えられてきたアストロサイトは、随意的な筋肉の動きを制御する運動ニューロンの生存と健康にとって極めて重要です。 実際、欠陥のあるアストロサイトは運動ニューロンを無駄にする可能性があり、筋肉が消耗する疾患である筋萎縮性側索硬化症(ALS)の主な疑いがあります。
この複雑な関係の根源を解明するために、ソーク生物学研究所の研究者らは、ALS をモデル化するためのヒト胚性幹細胞 (hESC) ベースのシステムを初めて確立しました。 彼らの研究は、機能不全に陥ったヒトのアストロサイトがその電荷に反して、健康な運動ニューロンを破壊することを確認した。 しかし、より重要なのは、培養細胞を強力な抗酸化物質であるアポシニンで処理することで、アストロサイトの機能不全によって引き起こされる運動ニューロンの死を阻止したことです。
彼らの発見はジャーナルの4月XNUMX日号に掲載される 細胞幹細胞、ALS における運動ニューロンの死滅に寄与する毒性経路について新たな洞察を提供し、ヒト ALS を使用した薬物スクリーニング実験の新たな可能性を切り開く ビトロ モデル、およびアストロサイトベースの細胞療法を使用した臨床介入。
「マウスモデルで顕著な効果を示したさまざまな薬剤が、前臨床試験と臨床試験の両方でその約束を果たせませんでした」と同氏は言う。 フレッド・H・ゲージ、研究を主導した遺伝学研究所の教授である博士。 実際、ALS の治療薬として FDA によって承認されているのはリルゾールという XNUMX つの薬だけで、病気の進行を XNUMX か月遅らせるだけです。
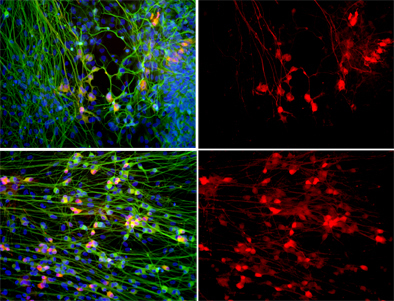
上: 運動ニューロン (赤で表示) が欠陥のある星状細胞の存在下で成長すると、その数は急激に減少します。 下: 強力な抗酸化物質であるアポシニンで培養物を処理すると、運動ニューロンの生存が劇的に増加します。 すべての細胞の核は青色でラベル付けされ、ニューロンは緑色で表示されます。 右パネル: 運動ニューロンのみが表示されています。
画像: ソーク生物学研究所の M. キャロル マルケット博士のご厚意により提供。
「臨床試験に応用できる可能性があり、少なくとも薬物や薬物標的を検証するためにマウスモデルと併用できる新しい ALS モデルが緊急に必要とされています」とゲージ氏は言う。
ルー・ゲーリッグ病としても知られる ALS は、60 年以上前にこの謎の病気に名前を与えたニューヨーク・ヤンキースの伝説的なスラッガーにちなんで命名されました。 通常致命的であるこの神経変性疾患は、随意運動を制御する運動ニューロンを攻撃し、進行性の麻痺や筋萎縮を引き起こします。
ALS は 140 年以上前に初めて病気として分類されましたが、その原因についてはまだほとんど手がかりがありません。 この病気の理解に向けた重要な一歩は、ALS が、スーパーオキシドジスムターゼ 1 の略である SOD1 酵素をコードする遺伝子の遺伝的変異によって誘発される可能性があることを発見したときでした。この酵素は、体内で生成される高反応性分子であるフリーラジカルによって引き起こされる損傷から身体を保護します。正常な代謝中の細胞。
脊髄運動ニューロンは高レベルの SOD1 を発現しており、多くの人は当初、これがその選択的脆弱性を説明しているのではないかと考えていました。 しかしすぐに、マウスの実験により、運動ニューロンの変性は必ずしも運動ニューロンにおける欠陥のあるSOD1の発現と関連しているわけではないことが明らかになりました。 それ自体が むしろ、重要な数の隣接する支持細胞での発現によるものです。
ALSマウスモデルで効果があった治療法のほとんどは前臨床試験や臨床試験で期待に応えられなかったため、博士研究員で筆頭著者のM.キャロル・マルケット博士は代替手段を模索した。「ヒト変異型を含むトランスジェニックマウス」 「SOD1のSODXNUMXは、疾患の発症と進行を研究するのに非常に有用でした。しかし、ヒトのニューロンとアストロサイトの両方を使用した細胞培養モデルは、薬物スクリーニングやある程度の細胞置換療法に潜在的に非常に役立つ可能性があると感じました。」
ヒトの運動ニューロン変性に対するアストロサイトの寄与を明らかにするために、マルケット教授はまず一連の物理的操作と多くの成長因子への曝露を通じてhESCを運動ニューロンに分化させた。 彼女がこれらの細胞を、変異型のSOD1を発現するヒト星状細胞と共培養したところ、ペトリ皿内で生存している運動ニューロンの数が激減した。 「変異が存在すると、アストロサイトは炎症反応を活性化し、ALSの特徴である活性酸素種を生成し始めた」とマルケット教授は言う。
彼女がこれらの細胞を、多くの植物に含まれるアポシニン、緑茶やチョコレートに含まれる有益な成分の一つであるエピカテキン、体内で生成されるアルファリポ酸などの既知の抗酸化物質で処理すると、アストロサイトの撹拌率が低下した。有害な活性酸素が大幅に減少しました。 それだけでなく、彼女が変異アストロサイトの存在下で培養した運動ニューロンを処理したところ、共培養実験で試験された唯一のアポシニンが、運動ニューロンがもはや支持力のなくなった環境に耐えるのを助けた。
「このシステムを酸化損傷の迅速な薬物スクリーニング試験として使用して、その後の長期共培養実験に最適な候補を特定できると考えています」と、Marketto 氏は言います。
SOD1 遺伝子変異の影響に関する研究は、運動ニューロン死の考えられる原因について重要な手がかりを提供していますが、実際にこの変異が原因であるのは、すべての ALS 症例のうちごく一部にすぎません。 まだ特定されていない他の遺伝的原因が明らかに存在します。
「人工多能性幹細胞技術の急速な進歩により、間もなく、ALS のさまざまな原因について新たな洞察を得るために、共培養アッセイで使用できる患者固有の幹細胞を生成できるようになるでしょう」とゲージ氏は言います。
この技術の商業化に関する情報については、ソーク技術管理開発局の Mike White (858-453-4100、x 1703 (mwhite@salk.edu)) までお問い合わせください。
この研究は、プロジェクト ALS、ダナ・アンド・クリストファー・リーブ財団、カリフォルニア再生医療研究所、ルックアウト基金、国立衛生研究所の資金提供を受けました。
この研究にも貢献した研究者には、ゲージ研究室の博士研究員アリソン R. ムオトリ博士とヤンリン ムー博士、博士研究員アラン M. スミス博士、助教授ガブリエラが含まれます。 G. シーザー博士、どちらもウィスコンシン大学マディソン校(マディソン)。
通信局
電話:(858)453-4100
press@salk.edu