
2022 年 10 月 31 日
SGDGと呼ばれるこの分子は、加齢に伴う神経疾患の新たな治療法につながる可能性がある
SGDGと呼ばれるこの分子は、加齢に伴う神経疾患の新たな治療法につながる可能性がある
【ラホーヤ】老化には複雑な展開があり、炎症、ストレス、代謝の変化など多くの登場人物が登場する。 今回、ソーク研究所とカリフォルニア大学サンディエゴ校の科学者チームは、老化プロセスに関与する別の要因、つまりSGDG(3-スルホガラクトシルジアシルグリセロール)と呼ばれる脂質の一種で、加齢とともに脳内で減少し、抗炎症作用がある可能性があることを明らかにした。
この研究は、 自然化学生物学 20年2022月XNUMX日に発表されたこの論文は、脳老化の分子基盤を解明するのに役立ち、加齢に関連した神経疾患の根底にある新たなメカニズムを明らかにし、将来の治療介入の機会を提供する。
「これらのSGDGが老化に重要な役割を果たしているのは明らかであり、この発見は、私たちが見逃してきた他の重要な老化経路がある可能性を開くものです」と共同特派員は述べています。 アラン・サガテリアン、ソークのクレイトン財団ペプチド生物学研究所の教授であり、フレデリック・ポールセン博士の椅子の保持者。 「これは、将来的にさらに掘り下げられるべきことを示す非常に明確な事例です。」
SGDG は脂質の一種であり、脂肪とも呼ばれます。 脂質は健康な脳の構造、発達、機能に寄与しますが、脂質の調節が不十分だと脳の老化や病気につながります。 しかし、脂質は遺伝子やタンパク質とは異なり、十分に理解されておらず、老化研究ではしばしば見落とされてきました。 サガテリアンは、新しい脂質の発見とその構造の決定を専門としています。
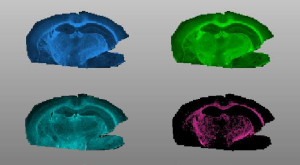
彼の研究室は、カリフォルニア大学サンディエゴ校のディオニシオ・シーゲル教授と協力して、SGDG に関連する XNUMX つの発見を行いました。脳内の脂質レベルは、年老いたマウスと若いマウスでは大きく異なります。 すべての SGDG ファミリーメンバーと関連脂質は年齢とともに大きく変化します。 そしてSGDGは、老化を調節することが知られているプロセスによって調節される可能性があります。
これらの発見に到達するために、チームは、脂質 (リピドミクス) の大規模な研究と構造化学および高度なデータ分析を組み合わせた、珍しい探索的アプローチを採用しました。 彼らは、液体クロマトグラフィー質量分析法を使用して、生後 18 ~ XNUMX か月の XNUMX 歳のマウスの脳の脂質プロファイルを初めて取得しました。 この機器の技術的進歩により、科学者が利用できるデータポイントの数が大幅に拡大し、高度なデータ分析により、膨大な脂質プロファイルの年齢関連パターンを特定できるようになりました。 その後、チームは SGDG 分子を構築し、生物活性をテストしました。
「SGDG は 1970 年代に初めて特定されましたが、その後の研究はほとんどありませんでした。 これらの脂質は本質的に忘れられており、脂質データベースから欠落していました. SGDG が老化に伴って変化したり調節されたりすることは誰も知りませんでした。ましてや、SGDG に生物活性があり、おそらく治療の標的にできる可能性があることは言うまでもありません」
分析は、SGDG が抗炎症特性を持っていることを示しました。これは、神経変性疾患や、脳内の炎症の増加を伴う他の神経学的状態に影響を与える可能性があります。

チームはまた、SGDG がヒトと霊長類の脳に存在することを発見し、SGDG がマウス以外の動物でも重要な役割を果たしている可能性を示唆しています。 SGDGs が人間の神経炎症に寄与するかどうかを示すには、さらなる研究が必要です。
将来的には、チームはSGDGが加齢とともにどのように調節されているか、どのタンパク質がSGDGの生成と分解に関与しているかを調べ、老化に関連する新しい遺伝的活動を発見する扉を開く可能性があります.
「SGDG の構造と実験室でそれらを作成する私たちの能力の理解により、これらの重要な脂質の研究は現在、広く開かれており、発見の機が熟しています」と、研究の共同著者である Siegel は述べています。
追加の著者には、メリック・エリック・エルトゥンク、ジャスティン・ワン、ティナ・チャン、アントニオ・FM・ピント、アンドレア・ロシャ、シンシア・J・ドナルドソン、ジョーン・M・ヴォーン、ピーター・C・グレイ、パメラ・マー、ソークのニコラ・J・アレンが含まれます。 カリフォルニア大学サンディエゴ校のSrihari Konduri; カリフォルニア大学ロサンゼルス校のパン・チャン。 ブラジル、カンピナス大学のライサ G. ルートヴィヒとマルセロ A. モリ。 カリフォルニア大学バークレー校のエリザベス・ウィリーとアンドリュー・ディリン。 スタンフォード大学の Manasi Iyer と Bradley Zuchero。 オレゴン健康科学大学のスティーブン・G・コハマ。
この作品は、Ferring Pharmaceuticals と Frederik Paulsen、国立衛生研究所 (P30 CA014195、R01DK106210、R01NS119823、R01AG069206、RF1AG061296)、オレゴン国立霊長類研究センター (P51 OD 010092)、Wu Tsai Human Performance Alliance、Joe によって資金提供されました。クララ ツァイ財団、アンダーソン財団、ブルース フォード アンド アン スミス バンディ財団、パイオニア フェローシップ、ハワード ヒューズ医学研究所、CZI 神経変性ネットワーク、サンパウロ研究財団 (2017/01184-9)。
DOI: 10.1038/s41589-022-01165-6
ジャーナル
自然化学生物学
作者
ダン・タン、シュリハリ・コンドゥリ、メリック・エリクシ・エルトゥンク、パン・ジャン、ジャスティン・ワン、ティナ・チャン、アントニオ・FM・ピント、アンドレア・ロシャ、シンシア・J・ドナルドソン、ジョアン・M・ヴォーン、ライッサ・G・ルートヴィヒ、エリザベス・ウィリー、マナシ・アイヤー、ピーター・C・グレイ、パメラ・マーハー、ニコラ・J・アレン、J・ブラッドリー・ズケロ、アンドリュー・ディリン、マルセロ・A・モリ、スティーブン・G・コハマ、ディオニシオ・シーゲル、アラン・サガテリアン
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。