
Июль 4, 2013
Открытия Солка раскрывают динамические изменения в эпигеноме, которые происходят во время формирования схемы мозга.
Открытия Солка раскрывают динамические изменения в эпигеноме, которые происходят во время формирования схемы мозга.
LA JOLLA, CA — Изменения в эпигеноме, включая химические модификации ДНК, могут действовать как дополнительный слой информации в геноме и, как считается, играют роль в обучении и памяти, а также в возрастном снижении когнитивных функций. Результаты нового исследования, проведенного учеными из Института биологических исследований Солка, показывают, что ландшафт метилирования ДНК, особый тип эпигеномной модификации, очень динамичный в клетках мозга при переходе от рождения к взрослой жизни, помогая понять, как информация в геномы клеток в головном мозге контролируются от внутриутробного развития до взрослой жизни. Мозг намного сложнее, чем все другие органы тела, и это открытие открывает дверь к более глубокому пониманию того, как формируются сложные схемы связей в мозге.
«Эти результаты расширяют наши знания об уникальной роли метилирования ДНК в развитии и функционировании мозга», — говорит старший автор. Джозеф Р. Экер, профессор и директор Института Солка Лаборатория геномного анализа и председатель Международного совета Солка по генетике. «Они предлагают новую основу для проверки роли эпигенома в здоровом функционировании и патологических нарушениях нейронных цепей».

Слева направо: Марга Беренс, Эран Мукамель, Терри Сейновски, Джозеф Экер
Изображение: предоставлено Институтом биологических исследований Солка.
Здоровый мозг — это продукт длительного процесса развития. Самая передняя часть нашего мозга, называемая лобной корой, играет ключевую роль в нашей способности думать, принимать решения и действовать. Мозг выполняет все это за счет взаимодействия особых клеток, таких как нейроны и глия. Мы знаем, что у этих клеток разные функции, но что придает этим клеткам индивидуальность? Ответ заключается в том, как каждая клетка выражает информацию, содержащуюся в ее ДНК. Эпигеномные модификации, такие как метилирование ДНК, могут контролировать, какие гены включаются или выключаются без изменения букв алфавита ДНК (ATCG), и, таким образом, помогают различать разные типы клеток.
В этом новом исследовании, опубликованном 4 июля 2013 г. НаукаУченые обнаружили, что паттерны метилирования ДНК претерпевают широкомасштабную реконфигурацию в лобной коре головного мозга мыши и человека во время развития, когда синапсы или связи между нервными клетками быстро растут. Исследователи определили точные участки метилирования ДНК по всему геному в мозге от младенцев до взрослых. Они обнаружили, что одна из форм метилирования ДНК присутствует в нейронах и глии с рождения. Поразительно, что вторая форма «не-CG» метилирования ДНК, которая почти исключительно характерна для нейронов, накапливается по мере взросления мозга, становясь доминирующей формой метилирования в геноме нейронов человека. Эти результаты помогают нам понять, как сложный ДНК-ландшафт клеток мозга развивается на ключевых этапах детства.
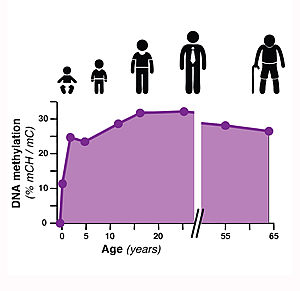
Новое исследование, проведенное исследователями Солка, дает первые исчерпывающие карты эпигеномных изменений в мозге, известных как «метилирование ДНК» — химическая модификация клеточной ДНК, которая может действовать как дополнительный слой информации в геноме.
Исследование дает представление о том, как определенные гены регулируются в эмбриональных, ювенильных и взрослых клетках мозга, а полученные результаты составляют важную основу для изучения того, могут ли изменения в паттернах метилирования быть связаны с заболеваниями человека, включая психические расстройства.
Изображение: предоставлено Эраном Мукамелем, Институт биологических исследований Солка.
Генетический код в ДНК состоит из четырех химических оснований: аденина (А), гуанина (Г), цитозина (Ц) и тимина (Т). Метилирование ДНК обычно происходит в так называемых сайтах CpG, где C (цитозин) находится рядом с G (гуанином) в алфавите ДНК. Примерно от 80 до 90 процентов сайтов CpG метилированы в ДНК человека. Исследователи Солка ранее обнаружили, что в человеческих эмбриональных стволовых клетках и индуцированных плюрипотентных стволовых клетках, типе искусственно полученных стволовых клеток, метилирование ДНК также может происходить, когда G не следует за C, отсюда и «метилирование без CG». Первоначально они думали, что этот тип метилирования исчезает, когда стволовые клетки дифференцируются в определенные типы тканей, такие как клетки легких или жировые клетки. Текущее исследование показывает, что это не относится к мозгу, где метилирование, отличное от CG, появляется после дифференцировки клеток, обычно в детстве и подростковом возрасте, когда мозг созревает.
Путем секвенирования геномов ткани мозга мыши и человека, а также нейронов и глии (из лобной коры головного мозга) на ранних постнатальных, ювенильных, подростковых и взрослых стадиях команда Солка обнаружила, что метилирование, не связанное с CG, накапливается в нейронах на ранних стадиях. детства и юности и становится доминирующей формой метилирования ДНК в зрелых нейронах человека. «Это показывает, что период, в течение которого созревают нервные цепи мозга, сопровождается параллельным процессом крупномасштабной реконфигурации нейронного эпигенома», — говорит Экер. Медицинский институт Говарда Хьюза и Фонд Гордона и Бетти Мура следователь.
В исследовании представлены первые исчерпывающие карты того, как паттерны метилирования ДНК меняются в мозге мыши и человека во время развития, что создает важную основу для изучения того, могут ли изменения в паттернах метилирования быть связаны с заболеваниями человека, включая психические расстройства. Недавние исследования продемонстрировали возможную роль метилирования ДНК при шизофрении, депрессии, суициде и биполярном расстройстве. «Наша работа позволит нам начать задавать более подробные вопросы о том, как изменения в эпигеноме формируют сложную идентичность клеток мозга на протяжении всей жизни», — говорит соавтор Эран Мукамель из Солка. Лаборатория вычислительной нейробиологии.
«Человеческий мозг называют самой сложной системой, о которой мы знаем во Вселенной», — говорит Райан Листер, соавтор новой статьи, ранее работавший научным сотрудником в лаборатории Экера в Солке, а ныне руководитель группы в Университет Западной Австралии. «Поэтому, возможно, нам не следует так удивляться тому, что эта сложность распространяется на уровень эпигенома мозга. Эти уникальные особенности метилирования ДНК, возникающие во время критических фаз развития мозга, предполагают наличие ранее неизвестных регуляторных процессов, которые могут быть критически вовлечены в нормальную функцию мозга и его нарушения».
В настоящее время среди нейробиологов существует консенсус в отношении того, что многие психические расстройства имеют генетическое происхождение и возникают в результате взаимодействия между генетической предрасположенностью и влиянием окружающей среды (например, стресс в раннем возрасте или злоупотребление наркотиками), результатом чего является изменение активности сетей мозга. . Построение и формирование этих мозговых сетей требует длительного процесса созревания, в ходе которого типы клеток центральной нервной системы (нейроны и глия) должны точно настроить способ выражения своего генетического кода.
«Метилирование ДНК выполняет эту роль», — говорит соавтор исследования. Терренс Дж. Сейновски, чтобы Исследователь Медицинского института Говарда Хьюза, владелец кресла Фрэнсиса Крика и глава отдела Солка. Лаборатория вычислительной нейробиологии. «Мы обнаружили, что паттерны метилирования динамичны во время развития мозга, в частности, для метилирования, отличного от CG, в раннем детстве и подростковом возрасте, что меняет наши представления о нормальной функции и дисфункции мозга».
Нарушая экспрессию транскрипции нейронов, добавляет соавтор М. Маргарита Беренс, штатный научный сотрудник Лаборатории вычислительной нейробиологии, «изменения этих паттернов метилирования изменят способ формирования сетей, что, в свою очередь, может привести к появлению психических расстройств в более позднем возрасте».
Другими исследователями, участвовавшими в исследовании, были Джозеф Р. Нери, Марк Урих, Клэр А. Паддифут, Николас Д. Джонсон, Хасинто Лусеро и Мэтью Д. Шульц из Института Солка; Джулиан Тонти-Филиппини из Университета Западной Австралии; Юн Хуан и Анджана Рао из Институт аллергии и иммунологии Ла Хойи; Мяо Юй и Чуань Хэ из Чикагский университет; Эндрю Дж. Дворк и Фатеме Г. Хагиги из Колумбийского университета; Хольгер Хейн и Манель Эстеллер Институт биомедицинских исследований Bellvigte; и Шиджун Ху и Джозеф С. Ву из Стэнфордский университет, факультет медицины.
Работа была поддержана Национальный институт психического здоровья, Медицинский институт Говарда Хьюза, Фонд Гордона и Бетти Мура, Калифорнийский институт регенеративной медицины, Общество лейкемии и лимфомы, Австралийский исследовательский совет, и Центр теоретической биологической физики Калифорнийского университета в Сан-Диего.
О Солковском институте биологических исследований:
Институт биологических исследований Солка является одним из выдающихся в мире институтов фундаментальных исследований, где всемирно известные преподаватели исследуют фундаментальные вопросы науки о жизни в уникальной, совместной и творческой среде. Сосредоточенные как на открытиях, так и на наставничестве будущих поколений исследователей, ученые Солка вносят новаторский вклад в наше понимание рака, старения, болезни Альцгеймера, диабета и инфекционных заболеваний, изучая неврологию, генетику, клеточную и растительную биологию и смежные дисциплины.
Достижения факультета были отмечены многочисленными наградами, в том числе Нобелевскими премиями и членством в Национальной академии наук. Основанный в 1960 году пионером вакцины против полиомиелита Джонасом Солком, доктором медицины, Институт является независимой некоммерческой организацией и памятником архитектуры.
ЖУРНАЛ
Наука
АВТОРЫ
Райан Листер, Эран А. Мукамель, Джозеф Р. Нери, Марк Урих, Клэр А. Паддифут, Николас Д. Джонсон, Хасинто Лусеро, Юн Хуанг, Эндрю Дж. Дворк, Мэтью Д. Шульц, Мяо Ю, Джулиан Тонти-Филиппини, Хольгер Хейн, Шиджун Ху, Джозеф С. Ву, Анджана Рао, Манель Эстеллер, Чуан Хе, Фатеме Г. Хагиги, Терренс Дж. Сейновски, М. Маргарита Беренс и Джозеф Р. Экер
Управление связи
Тел: (858) 453-4100
press@salk.edu