
9 августа 2009
ЛА-ХОЛЬЯ, Калифорния — Совместное исследование ученых из Института биологических исследований Солка показало, что супрессор опухоли p53, получивший название «хранитель генома», не только останавливает клетки, которые могут стать раковыми, но и контролирует перепрограммирование соматических клеток.
Хотя ученые научились перепрограммировать клетки взрослого человека, такие как клетки кожи, в так называемые индуцированные плюрипотентные стволовые клетки (ИПСК), эффективность перепрограммирования все еще крайне низка. Исследование Солка, опубликованное в предварительном онлайн-издании от 9 августа. Природа, дает новое понимание того, почему только несколько клеток из многих можно убедить повернуть время вспять.

Д-р Хуан-Карлос Изписуа Бельмонте и д-р Джеффри М. Валь
«Хотя мы уже давно можем перепрограммировать специализированные клетки, ничего не известно о механизмах контроля, которые препятствуют тому, чтобы это спонтанно происходило в организме, и о том, почему так сложно изменить их судьбу в чашке Петри». говорит Хуан-Карлос Изписуа Бельмонте, доктор философии, профессор лаборатории экспрессии генов, тесно сотрудничавший с Джеффри М. Уол, доктор философии, также профессор лаборатории экспрессии генов.
Их результаты приближают технологию иПСК к выполнению своих обещаний в качестве источника стволовых клеток для конкретного пациента, но также заставляют ученых переосмыслить развитие рака.
«Существовала десятилетняя идея о том, что рак возникает в результате дедифференцировки полностью коммитированных и специализированных клеток, но в конечном итоге от нее отказались в пользу модной в настоящее время теории раковых стволовых клеток», — говорит Уол. «Теперь, когда мы знаем, что p53 предотвращает дедифференцировку, я считаю, что пришло время пересмотреть возможность того, что перепрограммирование играет роль в развитии рака, поскольку практически все раковые клетки так или иначе теряют функцию p53».
По мере того, как эмбрионы млекопитающих проходят ряд стадий развития, выбор эмбриональных стволовых клеток, обладающих почти безграничными перспективами, постепенно сужается до тех пор, пока они в конечном итоге не дадут начало примерно 200 типам клеток, из которых состоит наше тело и которые, как правило, лишены способности возвращаться в прежнее состояние. вернуться к менее специализированной стадии.
Хотя дифференцировка, как правило, необратима, ученые разработали несколько методов преодоления нежелания клеток перепрограммироваться. Наиболее широко используемая технология включает принудительную экспрессию четырех факторов транскрипции - Oct4, Sox2, Klf4 и c-Myc - в полностью коммитированных взрослых клетках.
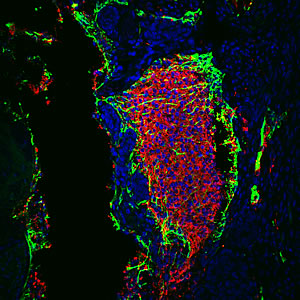
Понижение активности p53 увеличивает эффективность перепрограммирования взрослых соматических клеток, требующих только двух факторов перепрограммирования вместо обычных четырех.
Изображение: предоставлено доктором Хуаном-Карлосом Бельмонте, Институт биологических исследований Солка.
«К сожалению, Klf4 и c-Myc являются онкогенами, и их добавление может вызвать рак», — говорит Бельмонте. Тем не менее, несмотря на дополнительный толчок, обеспечиваемый этими мощными онкогенами, лишь крошечная часть трансмогрифицируется в иПСК, которые выглядят и действуют как эмбриональные стволовые клетки, что заставляет Бельмонте задаться вопросом, индуцировали ли то, что они делали, чтобы заставить клетки перепрограммироваться, реакцию, которая останавливала клетки. от роста?
Разговор со своим ближайшим соседом, экспертом по раку Валом, дал несколько свежих идей, которые можно было проверить в лаборатории. «Обычно клетки не перепрограммируются, поэтому должен существовать механизм, предотвращающий это», — говорит Уол. «Мы знали, что c-Myc и некоторые другие гены, необходимые для перепрограммирования, активируют супрессор опухоли p53, и нам было интересно, играет ли он какую-либо роль в этом».
И, конечно же, эксперименты постдокторских исследователей и соавторов Терухиса Кавамура, доктора философии, и Джотаро Судзуки, доктора философии, показали, что добавление факторов перепрограммирования c-Myc и Klf4, по отдельности или в различных комбинациях, активировало p53. путь. В качестве первооткрывателя супрессор опухоли p53 вызывается к действию, когда клетки испытывают стрессовые условия. Затем, в зависимости от ситуации, p53 включает гены, которые останавливают деление клетки, чтобы дать время на восстановление, или, когда все попытки спасения оказываются тщетными, приказывает клетке прекратить деление навсегда или совершить самоубийство.
В клетках, генетически сконструированных так, чтобы не было p53, эффективность репрограммирования была по крайней мере в 10 раз выше по сравнению с контрольными клетками, демонстрируя, что p53 явно играет важную роль в управлении клетками, пытающимися вернуться в состояние, подобное стволу.
Поскольку ИПСК, созданные с полным набором факторов перепрограммирования, рискуют стать злокачественными, Белмонте и его команда хотели знать, могут ли мышиные клетки, лишенные p53, быть перепрограммированы с использованием только двух факторов, Oct4 и Sox2. Клетки легко превращались в иПСК и давали здоровых, доношенных мышей, способных воспроизводиться, пройдя окончательный тест на плюрипотентные эмбриональные стволовые клетки.
«Это очень успешное сотрудничество — яркий пример того, что делает Солк таким особенным местом», — говорит Валь. «Мы с Хуаном Карлосом разговариваем каждый день и подходим к одному и тому же вопросу с совершенно разных точек зрения. Он исходит из точки зрения биологии развития, а я — со стороны рака, но если собрать их вместе, получится отличная история».
Для получения информации о коммерциализации этой технологии, пожалуйста, обращайтесь в Управление управления и развития технологий Salk по телефону (858) 453-4100, доб. 1278.
Эта работа была поддержана Национальными институтами здравоохранения, грантами от Tercel, Marato, Благотворительного фонда Г. Гарольда и Лейлы Мазерс и Fundacion Cellex.
Среди исследователей, которые также внесли свой вклад в работу, были Юньюань В. Ван, доктор философии. в лаборатории Валя Серхио Менендес, доктор философии, Лаура Батле Морера, доктор философии, и Анхель Рая, доктор философии, все в Центре регенеративной медицины в Барселоне, Испания.
О Солковском институте биологических исследований:
Институт биологических исследований Солка является одним из выдающихся в мире институтов фундаментальных исследований, где всемирно известные преподаватели исследуют фундаментальные вопросы науки о жизни в уникальной, совместной и творческой среде. Сосредоточенные как на открытиях, так и на наставничестве будущих поколений исследователей, ученые Солка вносят новаторский вклад в наше понимание рака, старения, болезни Альцгеймера, диабета и сердечно-сосудистых заболеваний, изучая неврологию, генетику, клеточную и растительную биологию и смежные дисциплины.
Достижения факультета были отмечены многочисленными наградами, в том числе Нобелевскими премиями и членством в Национальной академии наук. Основанный в 1960 году пионером вакцины против полиомиелита Джонасом Солком, доктором медицины, Институт является независимой некоммерческой организацией и памятником архитектуры.
Управление связи
Тел: (858) 453-4100
press@salk.edu