
19 августа 2020
Исследователи Солка разрабатывают пересаживаемые человеческие клетки, которые производят инсулин, контролирующий уровень сахара в крови без иммунодепрессантов на моделях мышей.
Исследователи Солка разрабатывают пересаживаемые человеческие клетки, которые производят инсулин, контролирующий уровень сахара в крови без иммунодепрессантов на моделях мышей.
ЛА-ХОЛЬЯ — Ученые Института Солка добились значительного прогресса в поиске безопасного и эффективного лечения диабета 1 типа, заболевания, от которого страдают примерно 1.6 миллиона американцев, а расходы на лечение составляют 14.4 миллиарда долларов в год.
Используя технологию стволовых клеток, исследователи Солка создали первые кластеры клеток поджелудочной железы, продуцирующие инсулин, способные уклоняться от иммунной системы, как подробно описано в журнале. Природа 19 августа 2020 г. Эти «иммунозащищенные» кластеры клеток контролировали уровень глюкозы в крови без иммунодепрессантов у мышей, однажды пересаженных в организм.
«Большинство диабетиков 1 типа — дети и подростки, — говорит профессор Солк. Рональд Эванс, старший автор и владелец кафедры March of Dimes в области молекулярной биологии и биологии развития. «Это болезнь, с которой исторически трудно справиться с помощью лекарств. Мы надеемся, что регенеративная медицина в сочетании с иммунным щитом может реально изменить ситуацию, заменив поврежденные клетки созданными в лаборатории человеческими островковыми клеточными кластерами, которые производят нормальное количество инсулина по требованию».
Диабет 1 типа — это пожизненное заболевание, которым сложно управлять, даже с помощью автоматических устройств, которые вводят инсулин для регулирования уровня сахара в крови. Трансплантация бета-островков поджелудочной железы — кластеров клеток, вырабатывающих инсулин и другие гормоны, — из донорской ткани может обеспечить излечение, но требует от пациентов пожизненного приема иммунодепрессантов, что сопряжено с серьезными рисками. На протяжении десятилетий исследователи искали лучший способ пополнения потерянных клеток поджелудочной железы. По данным лаборатории, трансплантация таких клеток, продуцирующих инсулин, без использования устройств делает нас на шаг ближе к излечению болезни.
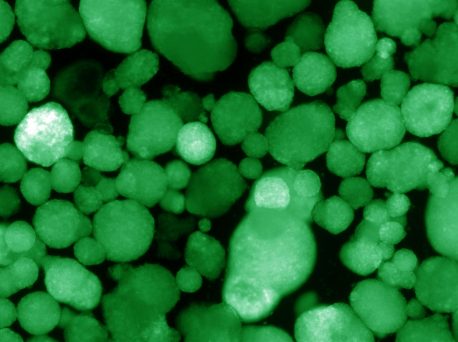
Открыть для изображения с высоким разрешением.
Предоставлено: Институт Солка.
В Предыдущее исследование, лаборатория Эванса преодолела препятствие в этой области, когда бета-подобные клетки, полученные из стволовых клеток, производили инсулин, но не были функциональными. По словам Эванса, клетки не высвобождали инсулин в ответ на глюкозу, поскольку им просто не хватало энергии. Его команда обнаружила генетический переключатель под названием ERR-gamma, который при переключении «турбо-заряжает» клетки.
«Когда мы добавляем ERR-гамма, клетки получают энергию, необходимую им для выполнения своей работы», — говорит Майкл Даунс, старший научный сотрудник Солка и соавтор обоих исследований. «Эти клетки здоровы и крепки и могут доставлять инсулин, когда чувствуют высокий уровень глюкозы».
Важнейшей частью нового исследования была разработка способа выращивания бета-подобных клеток в трехмерной среде, приближенной к поджелудочной железе человека. Это придавало клеткам островковое свойство. Важно отметить, что команда обнаружила, что белок под названием WNT4 способен включать управляемый ERR-gamma переключатель созревания. Эта комбинация шагов генерировала функциональные клеточные кластеры, которые имитируют островки человека: так называемые островкоподобные органоиды человека (HILO).
Затем команда занялась сложной проблемой иммунного отторжения. Трансплантаты нормальных тканей требуют пожизненной иммуносупрессивной терапии для защиты тканей от атак иммунной системы; однако эти методы лечения также увеличивают риск инфекций. Вдохновленные успехами иммунотерапевтических препаратов для лечения рака, команда первоначально показала, что белок контрольной точки PD-L1 защищает трансплантированные клетки. «Экспрессируя PD-L1, который действует как иммунный блокатор, трансплантированные органоиды могут скрываться от иммунной системы», — говорит первый автор Эйдзи Йошихара, бывший научный сотрудник лаборатории.

Открыть для изображения с высоким разрешением.
Предоставлено: Институт Солка.
Затем Йошихара разработал метод индукции PD-L1 в HILO с помощью коротких импульсов гамма-интерферона белка. При трансплантации мышам с диабетом эти иммуноускользающие HILO обеспечивали устойчивый контроль уровня глюкозы в крови у мышей с диабетом и здоровой иммунной системой.
«Это первое исследование, показывающее, что вы можете защитить HILO от иммунной системы без генетических манипуляций», — объясняет Даунс. «Если мы сможем разработать это как терапию, пациентам не нужно будет принимать иммунодепрессанты».
Необходимо провести дополнительные исследования, прежде чем эту систему можно будет довести до клинических испытаний. Трансплантированные органоиды необходимо тестировать на мышах в течение более длительного периода времени, чтобы подтвердить, что их эффекты носят долгосрочный характер. Необходимо проделать дополнительную работу, чтобы гарантировать, что они будут безопасны для использования людьми. «Теперь у нас есть продукт, который потенциально можно использовать у пациентов, не требуя никаких устройств», — заключает Эванс.
Другими исследователями в статье были Кэролин О'Коннор, Эмануэль Гассер, Зонг Вей, Тэ Гю О, Тиффани В. Ценг, Дэн Ван, Фриц Каябьяб, Ян Дай, Рут Т. Ю и Аннет Р. Аткинс из Солк и Кристофер Лиддл. из Вестмидского института медицинских исследований и Сиднейской медицинской школы в Австралии.
Эта работа была поддержана грантами Калифорнийского института регенеративной медицины, грантом DISC2-11175, грантом Национального института здравоохранения 1RO1DK120480-01, Благотворительным фондом Леоны М. и Гарри Б. Хелмсли Эвансу. Лиддл и Даунс финансировались за счет грантов Национального совета по здравоохранению и медицинским исследованиям Австралии. Йошихара получил поддержку гранта DRC P&F. Спасибо также Стивену и Лизе Альтман за поддержку лаборатории.
DOI: 10.1038 / s41586-020-2631-г
Чтобы получить ответы на часто задаваемые вопросы об этой работе, нажмите здесь..
ЖУРНАЛ
Природа
АВТОРЫ
Эйдзи Йошихара, Кэролайн О'Коннор, Эмануэль Гассер, Зонг Вэй, Тэ Гю О, Тиффани В. Ценг, Дэн Ван, Фриц Каябьяб, Ян Дай, Рут Т. Ю, Кристофер Лиддл, Аннет Р. Аткинс, Майкл Даунс, Рональд М. Эванс
Управление связи
Тел: (858) 453-4100
press@salk.edu
Институт Салка — это независимый некоммерческий исследовательский институт, основанный в 1960 году Джонасом Салком, разработчиком первой безопасной и эффективной вакцины против полиомиелита. Миссия Института — проводить фундаментальные, совместные, рискованные исследования, направленные на решение наиболее актуальных проблем общества, включая рак, болезнь Альцгеймера и уязвимость сельского хозяйства. Эта фундаментальная наука лежит в основе всех усилий по внедрению результатов исследований в практику, генерируя знания, которые позволяют создавать новые лекарства и инновации во всем мире.