
7 февраля 2024
Ученые Солка обнаружили, что раковые клетки аденокарциномы легких берут на себя управление и управляют метаболизмом липидов макрофагов, стимулируя прогрессирование опухоли, что указывает на новую цель для препятствий в лечении рака
Ученые Солка обнаружили, что раковые клетки аденокарциномы легких берут на себя управление и управляют метаболизмом липидов макрофагов, стимулируя прогрессирование опухоли, что указывает на новую цель для препятствий в лечении рака
ЛА-ХОЛЛА — Аденокарцинома легких является наиболее распространенным раком легких и причиной большинства смертей, связанных с раком, в Соединенных Штатах. Существует несколько способов возникновения аденокарциномы легких, одним из которых является мутация белка EGFR (рецептор эпидермального фактора роста). Немутированный EGFR помогает клеткам расти в ответ на повреждение, но мутировавший EGFR способствует неконтролируемому росту, который может перерасти в рак. Современные методы иммунотерапии не действуют против аденокарциномы легких, вызванной EGFR, и, хотя существуют некоторые лекарства для лечения рака, у пациентов обычно в течение нескольких лет развивается устойчивость к ним. Этот пробел в наборе инструментов для лечения вдохновил исследователей Института Солка исследовать слабые места на пути роста рака.
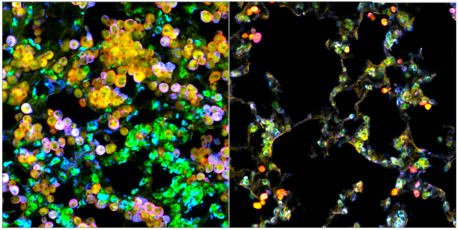
Команда обнаружила, что аденокарцинома легких, управляемая EGFR, захватывает специализированную популяцию резидентных в легких иммунных клеток, называемых макрофагами, которые предназначены для уничтожения больных и поврежденных клеток, а также для поддержания хрупкого баланса защитных липидов (жиров) вокруг альвеол легких. которые необходимы для дыхания. Клетки рака легких втягивают макрофаги в микроокружение опухоли и изменяют их липидный обмен, превращая их в «топлива» рака. Вновь получившие энергию опухолевые клетки затем стимулируют дальнейшую пролиферацию макрофагов, чтобы обеспечить больше топлива — новый механизм самовоспроизводства рака.
Выводы, опубликованные в Открытие Рака 25 января 2024 года, дают новое вдохновение для вмешательств при аденокарциноме легких, которые нарушают эти взаимоотношения опухолевых клеток и макрофагов. Исследователи предполагают, что лечение с использованием ингибиторов EGFR может быть более успешным в сочетании со статинами — классом препаратов, обычно используемых для снижения уровня холестерина.
«Мы открыли новый способ, с помощью которого клетки рака легких манипулируют своей локальной средой и другими типами клеток, окружающими их, чтобы способствовать собственному росту. В этом случае опухолевые клетки используют резидентные в легких макрофаги, ремоделируя их, чтобы обеспечить раковые клетки питательными веществами, такими как холестерин, и стимулировать рост опухоли», — говорит старший и соавтор, ведущий переписку. Сьюзан Кеч, профессор, директор Центра иммунобиологии и микробного патогенеза NOMIS и заведующий кафедрой NOMIS в Солке. «Одним из интересных выводов этой работы является то, что лечение рака легких можно улучшить, просто добавив в план лечения пациента статины, уже широко используемый класс лекарств».

Легкие опираются на крошечные луковицы, называемые альвеолами, которые расширяются и сдуваются при нашем дыхании, чтобы облегчить обмен кислорода и углекислого газа между воздухом и нашей кровью. Альвеолы имеют решающее значение для выживания человека, и их здоровье зависит от богатой липидами среды, создаваемой альвеолярными клетками и поддерживаемой макрофагами. Липиды, такие как холестерин, представляют собой жирные соединения, которые поддерживают функции организма, помогая клеткам двигаться, хранить энергию и усваивать витамины.
Эта уникальная способность резидентных макрофагов легких поддерживать липидный баланс усложняется, когда опухолевые клетки начинают использовать эти липиды для собственного роста. Лучшее понимание механизмов, которые макрофаги используют для регулирования своего метаболизма и производства липидов, может дать представление о том, как опухолевые клетки эгоистично манипулируют этими механизмами, чтобы помочь себе.
«Опухолевые клетки выделяют еще больше фактора роста, называемого GM-CSF (колониестимулирующий фактор гранулоцитов-макрофагов), который затем заставляет макрофаги расти рядом с ними и изменять свой метаболизм, что приводит к избытку липидов, которые опухолевые клетки используют для укрепления себя. ", - говорит первый автор Александра Кульманн-Хоган, бывший постдокторант в лаборатории Кеча и нынешний постдокторант в Калифорнийском университете в Лос-Анджелесе. "Рак эффективно похитил этот нормальный макрофагальный процесс поддержания легких здоровыми липидами, чтобы подпитывать себя".
«Мало того, что опухолевые клетки метаболически перепрограммировали макрофаги, они также запускали петлю обратной связи, которая способствовала оптимальному метаболическому состоянию самих опухолевых клеток», — говорит соавтор Катерина Полити, научный директор Центра рака грудной клетки в Йельском университете. Онкологический центр и профессор патологии Йельской медицинской школы.
Когда клетки аденокарциномы легких, управляемые EGFR, секретировали GM-CSF, это стимулировало ген в макрофагах, называемый PPARγ (гамма-рецептор, активирующий пролифератор пероксисомы), что запускало их метаболическое перепрограммирование и последующую секрецию липидов. Помимо использования этих курируемых макрофагами липидов для роста, опухолевые клетки также используют липиды для обеспечения постоянной активации EGFR-драйва, который помогает раку расти.
Кеч прогнозирует, что разрыв этой петли может стать новым вмешательством в замедление роста рака, вызванного EGFR. Исследователи пока не уверены, как именно доставка липидов, таких как холестерин, в опухолевые клетки влияет на онкогенный путь EGFR.
«Наши результаты открывают новые терапевтические возможности для резистентных к иммунотерапии аденокарцином легких, вызванных EGFR», — говорит соавтор, соавтор. Кристиан Металло, профессор и заведующий кафедрой Дэниела и Мартины Льюис в Солке. «Мы определили ключевую метаболическую связь между макрофагами и альвеолами, которая используется опухолевыми клетками для поддержки метаболических потребностей рака — теперь нам просто нужно нарушить эту эксплуатацию».
В будущих клинических испытаниях исследователи рекомендуют сочетать ингибиторы PPARy, которые могут нарушить захват макрофагов, со статинами, которые будут ограничивать доступный холестерин, наряду с используемыми в настоящее время ингибиторами EGFR. Им также любопытно, происходит ли подобный иммунологический захват в других опухолевых микроокружениях по всему телу, предполагая, что эти результаты могут побудить к дальнейшим открытиям в отношении других типов рака и иммунных клеток.
Среди других авторов - Зиян Сюй, Рамья Куна, Кейси Трейна, Анна-Мария Глобиг и Рубен Шоу из Солка; Текла Кордес из Технического университета Брауншвейга в Германии; Элизабет Квонг и Сандра Лейбель из Медицинской школы Калифорнийского университета в Сан-Диего и Сэнфордского консорциума регенеративной медицины; Мэтью Нобари и Джордж Ченг из медицинского факультета Калифорнийского университета в Сан-Диего; и Камила Роблес-Отейса, Дебора Айени, Стеллар Леви и Роберт Гомер из Йельской медицинской школы.
Работа поддерживалась Национальными институтами здравоохранения (R01CA230275, R01CA195720, R35CA220538, R01CA234245, R01CA216101S1), Йельской программой обучения биологии рака (T32CA193200-01A1), Фондом исследований рака Марка, грантом на обучение междисциплинарной иммунологии Йельского университета (T32AI-007019). XNUMX ), Фонд НОМИС, Фонд Уэйта, Фонд Чепмена, Благотворительный фонд Хелмсли и Центр геномной медицины Хелмсли.
DOI: 10.1158/2159-8290.CD-23-0434
ЖУРНАЛ
Открытие Рака
АВТОРЫ
Александра Кульманн-Хоган, Текла Кордес, Зиян Сюй, Рамия С. Куна, Кейси А. Трейна, Камила Роблес-Отеиза, Дебора Айени, Элизабет М. Квонг, Стеллар Леви, Анна-Мария Глобиг, Мэтью М. Нобари, Джордж З. Ченг, Сандра Л. Лейбель, Роберт Дж. Гомер, Рубен Дж. Шоу, Кристиан М. Металло, Катерина Полити, Сьюзан М. Кеч
Управление связи
Тел: (858) 453-4100
press@salk.edu
Институт Салка — это независимый некоммерческий исследовательский институт, основанный в 1960 году Джонасом Салком, разработчиком первой безопасной и эффективной вакцины против полиомиелита. Миссия Института — проводить фундаментальные, совместные, рискованные исследования, направленные на решение наиболее актуальных проблем общества, включая рак, болезнь Альцгеймера и уязвимость сельского хозяйства. Эта фундаментальная наука лежит в основе всех усилий по внедрению результатов исследований в практику, генерируя знания, которые позволяют создавать новые лекарства и инновации во всем мире.