
4 мая 2017
Новая технология Salk добавляет метильные группы в определенные положения ДНК, что позволяет целенаправленно корректировать гены аберрантных эпигенетических нарушений.
Новая технология Salk добавляет метильные группы в определенные положения ДНК, что позволяет целенаправленно корректировать гены аберрантных эпигенетических нарушений.
ЛА-ХОЛЬЯ — Ученые Института Солка разработали новую технологию для исправления вызывающих болезни аберраций в химических метках ДНК, влияющих на экспрессию генов. Эти типы химических модификаций, в совокупности именуемые эпигенетикой или эпигеномом, все чаще считаются столь же важными, как и сама последовательность генома в развитии и заболевании.
Новая технология Salk, которая описана в журнале Наука 4 мая 2017 года, был использован для моделирования мутаций в эпигеноме, связанных с раком толстой кишки, и для восстановления правильных моделей метилирования в стволовых клетках, полученных от пациентов, страдающих синдромом Ангельмана (АС), редким нейродегенеративным заболеванием, которое часто ошибочно диагностируют как аутизм. В дополнение к моделированию и лечению эпигенетических нарушений технология также может быть использована для изучения человеческого развития и биологии в целом.
«Мы в восторге от того, сколько новых возможностей открывает эта работа для понимания процессов болезни и разработки новых эффективных методов лечения», — говорит профессор Солк. Хуан Карлос Исписуа Бельмонте, старший автор статьи и обладатель кафедры Солка Роджера Гийемена. «Это был гигантский шаг, чтобы узнать, как редактировать геном — эта технология редактирования эпигенома — еще один шаг вперед».
Открыть для изображения с высоким разрешением. Предоставлено: Институт Солка/Центр Уэйта.
Лаборатория Изписуа Бельмонте недавно впервые применил метод модифицировать гены в неделящихся клетках, которые составляют большинство взрослых тканей. Новый метод выходит за рамки генов и нацелен на наиболее распространенный тип эпигенетических изменений, называемый метилированием ДНК, при котором химические метки, называемые метильными группами, прикрепляются к ДНК. Обычно эти теги помечают ген как готовый к включению или выключению. Все больше и больше ученых узнают, что метилирование ДНК участвует в ряде физиологических и патологических процессов, от эмбрионального развития до возникновения определенных заболеваний в более позднем возрасте, включая рак. Исследователи открыли способы изменения статуса метилирования коротких последовательностей ДНК, но до сих пор никому не удавалось добиться того, чтобы изменения сохранялись в широком диапазоне (необходимое условие для правильной активации или инактивации генов).
Поскольку 80 процентов ДНК млекопитающих метилированы, лаборатории Изписуа Бельмонте было любопытно узнать об участках, которые не метилированы. Как это ни парадоксально, эти области часто богаты потенциальными сайтами метилирования и имеют тенденцию быть близкими к областям генов, где начинается транскрипция генетической информации. Тем не менее, каким-то образом эти области, называемые CpG-островками, обычно остаются неметилированными.
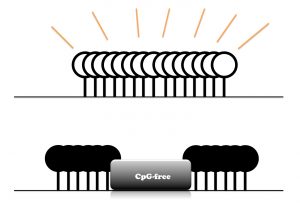
Открыть для изображения с высоким разрешением
Предоставлено: Институт Солка.
Исследователи предположили, что вмешательство в островки CpG может вызвать новое метилирование. Чтобы проверить эту гипотезу, команда сначала использовала молекулярные инструменты, чтобы вставить ДНК без CpG в островок рядом с MLH1 ген. MLH1 обычно неметилирован, но приводит к повышенному риску рака толстой кишки, если он становится метилированным. Команда смогла имитировать аберрантное метилирование в гене рака толстой кишки в качестве доказательства принципа, чтобы начать понимать, как аномальное метилирование связано с раком.
«Что интересно в CpG-островках, так это то, что они устойчивы к метилированию», — говорит Юта Такахаши, научный сотрудник Солка и первый автор статьи. «Но, вводя ДНК, свободную от CpG, мы можем обойти механизм, который блокирует ее, и затем вызвать метилирование ДНК всего острова».
Зная, что они могут индуцировать метилирование там, где оно неуместно, команда затем попыталась прикрепить метильные метки к тем местам генома, которым они действительно принадлежат, но отсутствуют, например, при некоторых заболеваниях. Синдром Ангельмана (АС) возникает в результате аберрантного метилирования ДНК, которое вызывает потерю белка UBE3A в нейронах. Это приводит к когнитивному дефициту у пациентов. Используя свою технологию, команда исправила аномальное метилирование ДНК и восстановила уровни белка UBE3A в нейронных клетках АС в чашке.

Открыть для изображения с высоким разрешением. Предоставлено: Институт Солка.
По словам исследователей, самым интересным был тот факт, что все введенные ими модели метилирования оставались стабильными с течением времени, чего нельзя было сказать о других эпигенетических технологиях. Даже удаление ДНК, свободной от CpG, не повлияло на новое метилирование. Открытие предлагает способ переписать эпигенетические метки на CpG-островках, а также дает представление о механизме, с помощью которого CpG-островки защищены от метилирования ДНК.
«Замечательно, что мы разработали новую технологию, которая позволяет надежно редактировать метилом ДНК на CpG-островках в плюрипотентных стволовых клетках, что поможет разработать терапию замещения клеток для эпигенетических расстройств», — говорит Джун Ву, штатный научный сотрудник Солка и один из соавторов статьи. «Но, обнаружив основные механизмы метилирования ДНК, мы надеемся сделать еще больше с помощью этой технологии».
Среди других авторов были Кейичиро Судзуки, Палома Мартинес Редондо, Мо Ли, Синь-Кай Ляо, Мин-Зу Ву, Рейна Эрнандес-Бенитес, Томоаки Хисида, Максим Николаевич Шохирев, Консепсьон Родригес Эстебан и Игнасио Санчо-Мартинес из Института Солка.
Работа финансировалась за счет NIH – Национальный институт рака (NCI), Фонд Чепмена, и Леона М. и Гарри Б. Хелмсли Благотворительный фонд, УКАМ и Благотворительный фонд Г. Гарольда и Лейлы Ю. Мазерс.
ЖУРНАЛ
Наука
АВТОРЫ
Юта Такахаши, Джун Ву, Кейчиро Судзуки, Палома Мартинес-Редондо, Мо Ли, Хсин-Кай Ляо, Мин-Зу Ву, Рейна Эрнандес-Бенитес, Томоаки Хисида, Максим Николаевич Шохирев, Консепсьон Родригес Эстебан, Игнасио Санчо-Мартинес, Хуан Карлос Изписуа Бельмонте
Управление связи
Тел: (858) 453-4100
press@salk.edu
Институт Салка — это независимый некоммерческий исследовательский институт, основанный в 1960 году Джонасом Салком, разработчиком первой безопасной и эффективной вакцины против полиомиелита. Миссия Института — проводить фундаментальные, совместные, рискованные исследования, направленные на решение наиболее актуальных проблем общества, включая рак, болезнь Альцгеймера и уязвимость сельского хозяйства. Эта фундаментальная наука лежит в основе всех усилий по внедрению результатов исследований в практику, генерируя знания, которые позволяют создавать новые лекарства и инновации во всем мире.